ファイザー (NYSE:PFE)2021年第4四半期決算説明会の日本語訳です。
ワクチンの売り上げが凄いですね。mRNAの技術は画期的なので今後も期待ができます。
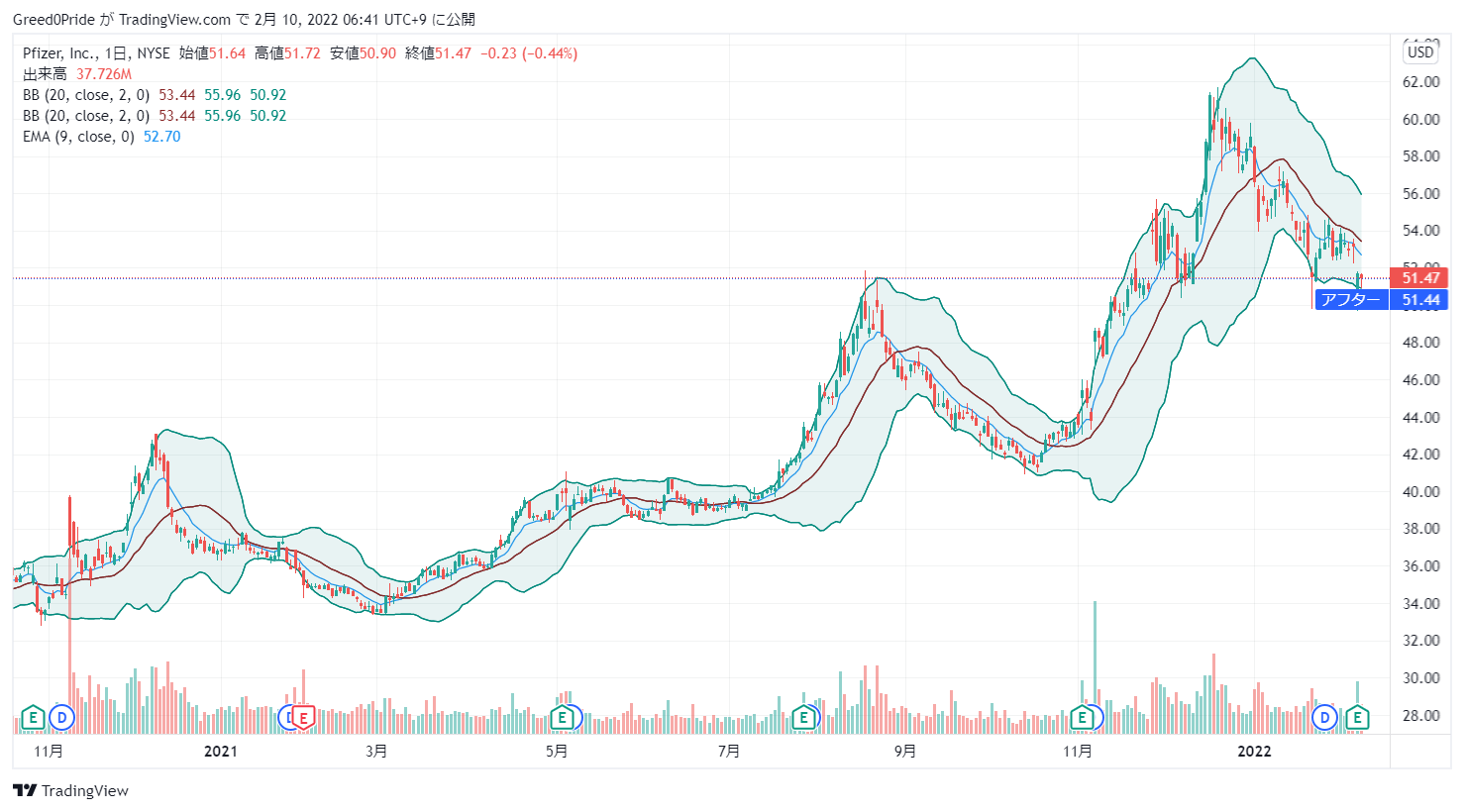
ファイザー (NYSE:PFE)株価
ファイザー (NYSE:PFE)2021年第4四半期決算説明会
2022年02月08日 午前10時00分(日本時間)
Call participants:
Chris Stevo — Senior Vice President and Chief of Investor Relations
Albert Bourla — Chairman and Chief Executive Officer
Mikael Dolsten — President of Worldwide Research and Development and Medical
Frank D’Amelio — Chief Financial Officer
Geoff Meacham — Bank of America Merrill Lynch — Analyst
Angela Hwang — Executive Team and Group President of the Pfizer Biopharmaceuticals Group
Aamir Malik — Executive Vice President, Chief Business Innovation Officer,
Mohit Bansal — Wells Fargo Securities — Analyst
Evan Seigerman — BMO Capital Markets — Analyst
Doug Lankler — General Counsel — Analyst
Umer Raffat — Evercore ISI — Analyst
Louise Chen — Cantor Fitzgerald — Analyst
Steve Scala — Cowen and Company — Analyst
Tim Anderson — Wolfe Research — Analyst
Andrew Baum — Citi — Analyst
Chris Schott — JPMorgan Chase and Company — Analyst
Chris Shibutani — Goldman Sachs — Analyst
Vamil Divan — Mizuho Securities — Analyst
Kerry Holford — Berenberg — Analyst
Carter Gould — Barclays — Analyst
More PFE analysis
オペレーター
皆さん、こんにちは!ファイザーの 2021 年第 4 四半期決算カンファレンスコールへようこそ。本日の通話は録音されています。ここで、電話を上席副社長兼最高IR責任者のクリス・スティーボ氏にお繋ぎしたいと思います。
どうぞよろしくお願いします。
Chris Stevo — 上席副社長兼最高投資家対応責任者
シルビアさん、ありがとうございます。皆さん、おはようございます。ファイザーの第4四半期決算説明会にようこそ。本日は、Dr.
Albert Bourla、CFOのFrank D’Amelio、世界研究開発・医療担当社長のMikael Dolsten、ファイザー生物医薬品グループ社長のAngela Hwang、最高事業・イノベーション責任者のAamir Malik、法務担当のDoug Lanklerが参加します。この電話会議は 90 分間行われる予定です。この電話会議の資料およびその他の収益関連資料は、pfizer.com の投資家向け情報セクションに掲載されています。スライド 3 の将来予測に関する記述の免責条項をご覧ください。
また、これらの記述および当社の非GAAP財務指標に関する追加情報は、当社の決算発表およびSECフォーム10-Kおよび10-Qの「リスク要因」に記載されています。この発表文に記載されている将来の見通しに関する記述は、重大なリスクや不確実性を含んでおり、発表文の日付時点のものであり、当社はこれらの記述の更新や修正を行う義務を負いません。それでは、アルバートに電話をお繋ぎします。
アルバート・ブーラ — 会長兼最高経営責任者
クリスさん、ありがとうございます。皆さん、こんにちは。2021年はファイザーにとって分岐点となる年であり、ファイザーの主要な注力分野すべてで過去最高を記録した年でした。私たちは、推定14億人の患者さんに、私たちの医薬品とワクチンをお届けしました。
これは、地球上の6人に1人以上の割合にあたります。ファイザーの患者への影響がこれほど広範に及んだことは、かつてありませんでした。当社は、PatientView Global Survey において、大規模なバイオ製薬企業の中で 4 位から 2 位へと順位を上げました。Morning Consult によると、アメリカ人の 61% がファイザーを好意的に見ており、これは 2020 年 1 月から 33 ポイント上昇しています。
つい先週、フォーチュン誌が毎年発表する「世界で最も賞賛される企業」のランキングで、当社は4位にランクインしました。同僚の95%が社内アンケートで、ファイザーで働くことを誇りに思うと回答しており、これはアメリカ企業で最高のランクに入ります。研究開発への投資を2020年の89億ドルから2021年には105億ドルに増やし、ファイザー史上最多となる13の重要な臨床試験を開始しました。最後になりましたが、売上高は業務上92%増の813億ドル、調整後希薄化後EPSは業務上92%増の4.42ドルとなりました。
COVID-19との戦いをリードしてきた私たちの成功は、世界に前向きな変化をもたらしただけではありません。私たちの会社や企業文化を根本から永久に変えたと信じています。ファイザーの全社員は、私たちが達成したことに刺激を受けており、ほとんどの社員が、ゲームを変える可能性のある次のブレークスルーに参加することをこれまで以上に強く決意しています。そのため、COVID-19 で開発した Lightspeed の原則を他の治療分野にも適用し、すべての患者さんの利益のために科学のスピードで前進し続けることを確実なものにしています。
その結果、2022年には、これらの指標のそれぞれについて、さらに良い結果を出すことができると考えています。例えば、2022年通年の財務ガイダンスには、これまでで初めて、売上高の中間値、つまり3桁の1000億ドル、調整後希薄化後EPSの中間値6.45ドルが含まれています。コミルナティはファイザーの業績に大きなプラスの影響を与えていますが、最も重要なのは、COVID-19ワクチンが社会に与えた多大な影響です。米国では
2021年12月のコモンウェルス基金の報告書によると、米国だけでも、COVID-19ワクチン接種プログラムは100万人以上の命を救い、1000万人以上の入院を防いだと推定されています。経済的な影響も同様に驚くべき、驚異的なものです。2021年12月のハートランド・フォワードのレポートによると、米国におけるCOVID-19ワクチンの迅速な展開と幅広い利用が、2021年だけで4380億ドルの推定経済的節約を生み出し、これは米国に相当するものである。
GDPが2.3%、2.3ポイント高くなることになります。2022年2月6日現在、米国で投与された10回分のうち約6回分がComirnatyであることを考えると、ファイザーはこれらの恩恵に大きく貢献したと自負しています。これは、私たちの科学の価値であり、私たちの文化が可能にしたものであり、私たちの社員を動かすものなのです。
さて、今後の成長の原動力となる3つの要因についてお話したいと思います。1つ目は、COVID-19の長期的な見通しと、当社がこの病気との闘いをリードし続けることができる立場にあると考える理由です。2つ目は、当社の熟慮された資本配分戦略と、それが10年後半における当社の成長の原動力となりうると考える理由です。そして 3 つ目は、ESG 原則に対する当社の取り組みが、ファイザーが患者さんと社会に有意義な価値を提供するために、どのように持続可能な成長を実現するように設計されているかということです。
まず、COVID-19のパンデミックについてお話します。当社の科学者たちは、SARS-CoV-2ウイルスの監視を続けていますが、当面は完全に根絶されることはないだろうと考えています。このように考えているのには、いくつかの理由がある。このウイルスは世界的に分布しているため、封じ込めが困難である。
このウイルスは頻繁に変異する能力を示しており、その先手を打つことは困難です。また、自然感染では、すべての感染やウイルスの変異を防ぐために必要な耐久性のある防御ができないことを示すデータもあるようだ。その結果、人々は時間の経過とともに同じ株や異なる株に再感染する可能性があるのです。とはいえ、私たちは現在、ワクチンや治療法という手段を手に入れました。これは、パンデミックの管理を改善するだけでなく、各国が流行期に移行するのを手助けするのに役立つと信じています。
言い換えれば、これらのツールは、世界中の病院や医療システムに過度の負担をかけるリスクを下げながら、私たちが日常に戻り、家族や友人と過ごし、旅行し、屋内の食事やコンサートに参加し、その他多くの活動を楽しむことを可能にするものだと信じているのです。ファイザーの社員一同は、これらのツールを世に送り出すために、当社が果たし続けてきた役割を非常に誇りに思っています。2021年を通じて、当社はCOVID-19ワクチンをより多くの人々に提供し、製造・流通能力をさらに高める努力を続けました。その結果、当社のコミルナティワクチンの市場シェアは拡大し続け、米国全体で配布される全用量の70%を占めています。
の70%を占めています(2月5日現在)。パックスロビドについては、’22年第1四半期に600万コースの生産を見込んでいます。全体では、2022年上半期に3,000万コース、通年では1億2,000万コースを、もちろん世界のニーズに合わせて生産する予定です。パックスロビド」は、先般、欧州医薬品庁から条件付販売承認を取得したことにより、現在までに約40カ国で特定の集団に対する緊急承認または条件付使用承認を取得しています。
現在、世界各国政府と協議を進めており、承認件数が増えれば増えるほど、この治療薬の契約件数が増え、まさにゲームチェンジャーとなることが期待されます。ファイザーでは、これらのツールやその他の有意義なソリューションを世界に提供するリーダーシップを維持するために、研究開発への投資を継続する責任を痛感しています。このため、私たちは、懸念される変異型が出現した場合に対処できるよう、異なるバージョンのワクチンの開発とテストを続けています。また、現在、新しいオミクロン・ベースのワクチン候補と二価のCOVID-19ワクチン候補に取り組んでいます。また、米国から緊急使用許可を得てからわずか2カ月で承認されたのも、このためです。
また、「パックスロビット」が米国食品医薬品局から緊急使用許可を得てからわずか2カ月で、すでに次世代の経口COVID-19治療薬の開発に取り組んでいるのもそのためです。研究開発への多大な投資と、品質や安全性に妥協することなく科学の進歩に対応する能力、政府、医療関係者、消費者から得た強い信頼性、そしてグローバルなフィールドでの幅広い存在感と大規模かつ高品質の製造における比類のない能力によって、今後もこのリーダー的地位を維持できると確信しています。次に、資本配分をどう考えるかについて触れ、もう一度、私たちの戦略を説明したいと思います。私たちは、2025年まで事業全体が堅調なトップラインの成長軌道を実証し続けると考えています。
コンセンサス予想も、この勢いを徐々に認識し始めています。しかし、現在のコンセンサス予想では、2025年から2030年にかけて当社のトップラインは縮小すると見ています。これは、私たち自身の計画と矛盾していることを繰り返しお伝えしたいと思います。当社の目標は、この期間に予想されるLOEの影響にもかかわらず、’25年から2030年まで成長企業であり続けることです。
この目標を達成するための当社の自信は、当社の事業の勢い、先ほど説明したCOVID-19の耐久性、過小評価されている当社の社内パイプライン、そしてもちろん、外部の科学にアクセスするための成長に焦点を当てた事業開発への資本投入能力に裏打ちされています。それについて少しお話します。私たちは、事業戦略や目標を推進するために事業開発の機会を活用しています。当社のバランスシートとキャッシュフローの強さにより、今後新たな事業開発の機会を追求することができ、2030年のトップライン予想に少なくとも250億ドルのリスク調整後収益を上乗せできる可能性があります。
私たちは、成長する配当を維持し、他のキャッシュの使用に対する柔軟性を保ちながら、これを実現することを期待しています。当社の事業開発努力の焦点は、後期段階の資産や、患者さんにとって画期的な進歩をもたらす可能性のある初期の医療技術革新など、魅力的な外部科学に引き続き焦点を当てることにあります。また、当社が高い付加価値を生み出し、最も成功するターゲットを選択できる科学的スキルと洞察力を有する治療領域とプラットフォームに重点を置いています。また、当社は、世界最高水準の臨床開発力、卓越した製造・販売能力を有しており、様々な取引形態において非常に魅力的なパートナーとなることができると考えています。
このようなアプローチを実現する機会が存在すると考えており、私自身、この実行に注力していくつもりです。資本的に大きな柔軟性があるにもかかわらず、事業開発において適用する科学的・財務的基準を決して下げないということを強調したいと思います。これらの機会を追求する際、私たちは評価と優先順位付けのプロセスにおいて、高い規律性を保ち続けます。2019年以降、私たちはすでに事業開発取引に250億ドル近くを投資し、コンセンサスで130億ドル以上、繰り返しますが、2030年のコンセンサスで収益を追加しています。
現在、130億ドルのコンセンサスには、Trillium資産、Biohavenとの提携、最近発表したmRNAの取引は何も含まれていないことを指摘しておきますが、これらはすべて大きな可能性を持っています。私は、このような事業開発のペースが今後加速されると見ており、この10年の後半にファイザーが成長企業であることを確実にする重要な推進力になると確信しています。mRNA は、多くの感染症、癌、希少な遺伝性疾患、さらには自己免疫疾患にも応用できる汎用性の高い技術として注目されています。
mRNAは聖杯ではありませんが、私たちはこの技術がグローバルヘルスに画期的な影響を与える可能性があると信じています。だからこそ、私たちは強固なmRNA戦略を策定し、積極的にプラットフォームを構築しているのです。パンデミックによって、mRNAワクチンを大規模に提供することはそれほど簡単ではないことが明らかになりましたが、ファイザーはこの分野のリーダーとして台頭してきました。数十年にわたる経験を味方に、私たちは間違いなく世界で最も効率的な臨床開発およびワクチン製造能力を開発しました。また、9ヶ月の間にこれらの機能で2,400人近くを新たに雇用し、記録的な速さで新しい機能を拡張、構築してきました。
今後も、mRNAの研究開発と製造の両面で築き上げたリーダーシップを生かすべく、投資を続けていく予定です。もちろん、こうした社内での投資や改善に加えて、この分野での能力を強化するための社外投資も行っています。例えば、ファイザーは最近、mRNA戦略の推進に役立つ4つの重要な事業開発契約を締結しました。バイオテック社との提携を拡大し、既存のプラットフォームを利用して帯状疱疹を予防するための帯状疱疹ウイルスのmRNAワクチン候補を共同開発します。
ビーム・セラピューティクスとの契約により、当社のmRNAへの取り組みは、ファイザーのもう一つの中核的治療分野である希少疾患にも拡大し、肝臓、筋肉、中枢神経系の希少遺伝性疾患に関する3つのターゲットについて4年間の研究協力が結ばれました。これにより、病気の予防だけでなく、病気の治療にもmRNAを活用できる可能性が出てくると考えています。アキュイタス社との契約により、mRNAワクチンおよび治療のための最大10個の標的について、同社独自の脂質ナノ粒子技術の共同研究およびライセンス供与が可能になりました。これにより、この分野での独立性が高まると考えています。
また、遺伝子とmRNAのオンデマンド合成のための自動化ソリューション開発のリーダーであるCodex DNAと戦略的提携およびライセンス契約を締結し、mRNA生産工程の前工程でDNAを酵素的に組み立てることができる可能性が出てきました。これにより、新しいワクチンの製造にかかる時間が3カ月から2カ月に短縮される可能性があります。これが成功すれば、例えばインフルエンザのワクチン開発において重要な差別化要因となり、インフルエンザの流行開始時期により近い時期に菌株を選択することが可能になります。これらの取引は、より大きな戦略的パズルの4つのピースに過ぎません。
mRNA戦略の実行を継続する中で、この分野に的を絞った活動を期待したい。もちろん、前四半期の事業開発活動は、mRNA戦略の実行にとどまりません。これは前四半期にお見せしたスライドのアップデート版ですが、その他の最近の案件をいくつかご紹介したいと思います。このスライドでは、新規案件としてマークしています。
Trillium社の買収は、がん領域における当社の強力なリーダーシップの実績に基づいており、世界中の血液がんと共に生きる人々の転帰を改善するために、当社の血液学ポートフォリオが強化されることになります。Biohaven社との戦略的提携により、疼痛と女性の健康における当社の優れた商業能力を活用することができます。[申し訳ありません。私たちは戻ってきました。
技術的な問題をお詫びします。この最後のスライドの原稿をもう一度書いて、次に進みます。もちろん、前期の事業開発活動は、mRNA戦略の実行にとどまりません。これは前四半期にお見せしたスライドのアップデートですが、その他の最近の案件をいくつか紹介したいと思います。
新規という表示でご覧いただけます。Trillium社の買収は、がん領域における当社の強力なリーダーシップの実績に基づいており、世界中の血液がんと共に生きる人々の転帰を改善するために、当社の血液学ポートフォリオを強化するものです。Biohaven社との戦略的提携は、疼痛と女性の健康における当社の優れた商業能力を活用し、片頭痛の急性期および予防治療薬として米国で唯一承認されているBiohaven社の画期的な経口CGRP受容体拮抗剤により、米国外でこの消耗性神経疾患に苦しむ患者様に価値ある新しい治療オプションを提供できる可能性が出てきました。
また、アリーナ社の買収により、ファイザー社の優れた研究力とグローバルな開発力を活用し、免疫炎症性疾患の患者さんに対するエトラシモドの臨床開発を加速させる予定です。さて、ファイザーの強化されたESG戦略について、いくつか詳細をご紹介したいと思います。この戦略は、今後 10 年間に有意義で測定可能な影響を生み出す機会があると考えられる 6 つの分野に焦点を当てています。すなわち、製品のイノベーション、公平なアクセスと価格設定、製品の品質と安全性、多様性、公平性と包摂、気候変動および企業倫理です。今後、四半期ごとに、私たちがどのようにESGを事業のすべての中核分野に組み込んでいるか、事例をご紹介していきます。
今期は、臨床試験の多様性を向上させ、従業員の多様性を改善し、当社のCOVID-19ワクチンと治療への公平なアクセスを確保するための取り組みに焦点を当てたいと思います。昨年、ファイザーは、2011年から2020年までに登録を開始した当社の介入型臨床試験213件の米国人参加者の人口統計データについて、業界初のレトロスペクティブ分析を発表しました。この分析では、黒人またはアフリカ系アメリカ人の全体的な臨床試験への参加は、米国と同じレベルであることが示されました。
ヒスパニック系またはラテン系アメリカ人の参加率は15.9%対18.5%、女性の参加率は51.1%対50.8%で、いずれも米国国勢調査レベルであった。この分析結果は、透明性を確保し、この分野での進捗を測定する際の基準値とするために発表しました。
当社は、臨床試験における多様性は公平性と優れた科学性の問題であると考え、臨床試験における多様性を改善することを目的とした断固とした措置をとっています。私たちの目標は、すべての試験において、人種や民族の多様性を、米国の国勢調査や疾患の有病率レベル以上(適切な場合)にすることです。第二に、特に上級職において、従業員の多様化が大きく進展していることを強調したいと思います。
例えば、過去3年間で、全世界の副社長クラス以上の女性の比率は32%から42%に増加しました。また、同じ期間に、米国では副社長クラス以上のマイノリティの割合が19%から25%に増加しました。3つ目に紹介したいのは、当社のCOVID-19ワクチンと経口治療薬を、世界中の誰もが利用できるようにするための取り組みです。
2021年末までに最初の10億回分のワクチンを届けるという目標を達成したばかりですが、2022年末までに少なくとも20億回分のワクチンを中低所得国に届けるという世界的な目標を達成し、それを上回る勢いであることをお伝えできるのは、とても喜ばしいことです。また、私たちの20億回接種のコミットメントについて、2つのデータを強調したいと思います。このうち10億本は、最貧国に対して完全に無償で提供されます。米国との契約により、このうち10億回分は最貧国に完全無料で提供されます。
米国政府との契約により、ファイザーは米国政府に非営利の価格でこれらの用量を提供し、米国政府はそれを最貧国に無償で提供しています。また、2021年にお届けした10億回分の投与は、この昨年お届けした全投与回数の37%に相当します。経口治療薬COVID-19に関しては、Medicines Patent Poolと任意ライセンス契約を締結し、世界の人口の約53%を占める95の低・中所得国において、各国の規制当局の承認または認可を経て、アクセスの拡大につながることを期待しています。
最後に、取締役会の報酬委員会が、役員報酬とESGパフォーマンスを連動させる方法を検討し、本年中に開始する予定であることをお知らせします。当社のESG戦略が2021年に当社のビジネスに与えた影響の詳細については、3月中旬にオンラインで公開されるファイザーの2021年ESGレポートにご期待ください。要約すると、2021年はファイザーにとって素晴らしい年であり、COVID-19から学んだ教訓を引き続き適用して、当社のすべての治療領域で患者さんにブレークスルーを提供することを楽しみにしています。私たちは引き続き、機動的であること、研究開発組織への投資、そして私たちの科学の力を十分に発揮できるようなダイナミックなパートナーシップの探求に重点を置いています。
これらは、世界で最も深刻な疾病に対処するために挑戦し続ける、素晴らしい目的を持った同僚の貢献なしには実現できません。2021年、私たちの仲間は期待を上回る活躍をしてくれました。そこで、ボーナス支給対象の同僚と役員に対して取締役会が承認したボーナスプールの一部を再び使用し、ボーナス支給対象外の同僚に対して、その努力に報いるため、またCOVID-19パンデミックのために発生した個人、家族、生活費をカバーするために、全社員に1回限りの特別なCOVID-19状況対応ボーナスを支給する予定です。それでは、ミカエルから研究開発の進捗状況についてご説明します。
ミカエルの後は、フランクが第4四半期の財務の詳細と2022年の見通しについて説明します。それでは、ミカエルさん?
Mikael Dolsten — ワールドワイド研究開発・メディカル担当プレジデント
アルバート、ありがとうございます。ファースト・イン・クラスのサイエンスを提供し続ける当社にとって、今期の最新情報をお伝えできることを嬉しく思います。本日は、COVID-19プログラムおよび当社のパイプラインにあるその他の資産に関する最新情報をお伝えします。まず、パックスロビドから始めましょう。
COVID-19の流行が公衆衛生に負荷を与え続ける中、当社は新規の経口抗ウイルス治療薬に関する科学を発展させてきました。重要なのは、デルタとオミクロンの両方を含む、現在懸念されているすべての亜種に対して、in vitroで一貫した強力な抗ウイルス活性が確認されたことです。これは、この化合物が設計された経緯から予想されることです。左の図は、ニルマトルビルがオミクロン変異体の活性部位に強く結合していることを示す結晶構造です。
HIVプロテアーゼの分野では、治療薬が基質に近い形で設計されればされるほど、耐性が出現しにくくなることが歴史的に知られています。このことは、プロテアーゼの本質的な性質、短い治療期間、リトナビルとの併用により、in vitroの試験でウイルスを殺すのに必要な化合物の量の5倍から6倍以上の薬物曝露があることと相まって、耐性化のリスクを低減できることを示唆しているのです。外部データも我々の知見を裏付けています。このスライドでは、数値が低いほど強い活性を示し、ニルマトルビルは左のY軸の下端にあり、最も強い活性を持っていることが示されています。
ニルマトルビルはin vitroで低ナノモル域の活性を維持しており、このグラフは他の承認・認可されている治療薬も含めてご覧いただいています。左は、マウントサイナイ大学アイカーン医科大学とファイザー社との共同研究によるin vitroデータです。ニルマトルビルは、薬効の指標であるIC50(感染を半分に抑制するのに必要な濃度)で測定したところ、強力な抗ウイルス活性を示しました。これは、右図に示すベルギーのKUルーヴェンのレガ研究所の知見と一致しています。
ハイリスク集団でのFDAによる新薬承認申請は’22年後半、家庭内接触者試験と標準リスク試験はそれぞれ’22年第2四半期と後半に主要な結果が得られ、6歳から18歳の小児での試験開始は’22年第1四半期に予定されています。標準リスク研究では、症状のあるCOVID-19の非入院患者750人の登録を拡大します。標準リスク患者には、スクリーニングの12カ月以上前にSARS-CoV-2ワクチンの最終接種を受けていることが条件となりますが、ワクチン接種済みの患者も登録可能です。この拡大により、中間解析で見られた副次的評価項目(プラセボと比較して、治療群では入院が70%減少し、死亡はなかった)をさらに評価することができます。また、次世代型SARS-CoV-2抗ウイルス剤については、良好な安全性プロファイルで活性を維持し、潜在的なウイルス耐性に対応する汎コロナウイルス設計特性で、リトナビルの昇圧を必要とせず、同様の高い臨床効果を達成することを目指して研究を進めています。
ヒトでの最初の試験は、’22年後半に予定されています。現在、ワクチン開発も進めており、5歳児への緊急使用許可を取得しました。12歳以上を対象とした3回接種の有効性データと、デルタやオミクロンを含む懸念される他の変異型について観察された初期の実験データから、コミルナティを3回接種した人は、2回接種した場合に比べて、症状および重症化に対する高い防御力を持つ可能性があることが示唆されています。このデータに基づき、当社は、免疫ブリッジングデータに加えて、生後6カ月から4歳までの小児を対象とした試験において、3回目の3マイクログラムの投与が最適である可能性があると考え、評価を行っています。
しかし、小児科領域の患者数および入院数が過去最高となっていることから、FDAは、3回目の投与も含めたデータ収集を継続しながら、これまでに蓄積した2回投与の有効性、免疫原性、安全性データでローリングEUA承認申請を開始するよう促しました。3回目の投与データについては、入手可能になり次第、提出する予定です。一方、FDAは2月15日に諮問委員会を開催し、本日収集した小児用2回投与データを検討する予定です。2回分の緊急時使用許可が下り、CDCが使用を推奨した場合、保護者は3回目の投与の許可の可能性を待つ間、生後6カ月から4歳までの子どもたちにコビド19の接種シリーズを始める機会が与えられることになります。
次に、成人の場合です。オミクロンの患者数が急増したことを受け、1月に、コミルナティの3回目の接種が生ウイルス中和に及ぼす影響について、ラボでの分析が完了しました。その結果、3回目投与当日から1ヵ月後までの間に、オミクロンの生ウイルス中和価が25倍以上上昇することが確認され、大変うれしく思っています。また、野生型とオミクロンの変異型では、投与3日目から4カ月後に抗体の減衰が緩やかであることが確認された。
投与1ヶ月後から4ヶ月後までの中和価は、野生型が1.6倍、omicronが2倍に低下していた。3回目の投与でオミクロンに対する高い防御力を維持する効果が、現実の世界で確認され始めているのです。Kaiser Permanente Southern Californiaのデータで、上が入院を伴わないオミクロン関連の救急外来受診、下が入院を示す。コミルナティの3回投与は、2回投与よりもオミクロンに対して優れたワクチン効果を発揮しました。
そして、デルタ関連の入院と同様に、オミクロン関連の入院に対しても、3回接種の高いワクチン効果がありました。しかし、3回目の接種から3カ月以上経過すると、オミクロンによる救急外来受診に対して効果が低下することが確認され、現在のワクチンまたはオミクロンをベースにしたワクチンの再増量の必要性が示唆されました。当社は、18歳から55歳の成人を対象としたオミクロンベースのワクチン候補の臨床試験を開始しました。この試験では、3つのコホートにわたって1,400人以上の参加者を評価する予定です。
登録の90〜180日前に現行のワクチンを2回接種している人は、ベースとなるオミクロンベースのワクチンを1回または2回接種する。登録の90日から180日前に現在のワクチンを3回接種している人は、現在のワクチンまたはオミクロンベースのワクチンを1回接種します。また、ワクチン未治療の方は、オミクロンベースのワクチンを3回接種します。この試験は、科学的根拠に基づいたバリアントベースのワクチン開発への取り組みの一環であり、現行ワクチンの野生型および初期のバリアントと同レベルのオミクロンに対する防御を達成し、より長い防御期間を持つことを期待しています。
さて、次に次世代のCDK阻害剤についてです。進行性あるいは転移性乳がんの患者さんの多くは、内分泌療法とCDK4/6阻害剤の両方に対して、その変革的な有効性にもかかわらず、最終的には抵抗性を獲得します。CDK選択的活性薬剤またはCDK2/4/6トリプル活性薬剤でCDK2を阻害することにより、抵抗性を予防、遅延、逆転させ、生存期間を延長させることができるかもしれません。これらは、ホルモン受容体陽性の転移性乳がん患者を対象としたCDK2/4/6阻害剤の第1相用量漸増および抗腫瘍活性試験におけるサブセットからのデータです。
腫瘍サイズの縮小という点では、単独療法またはフルベストラントとの併用療法を受けた患者さんで最も改善が見られました。また、3名の部分奏効が確認され、3名の患者さんで12ヶ月以上病勢が安定していることが確認されました。1名の患者さんは28ヶ月以上継続して治療を受けています。推奨される第2相用量である25ミリグラム1日2回投与で、安全性プロファイルは許容範囲内でした。
今後、第1相用量設定を行う予定であり、本年第4四半期に完了する見込みです。CDK2のみの阻害剤による選択的CDK2阻害は、用量漸増が可能であり、パルボシクリブや他の次世代CDK選択的阻害剤など、承認済みのCDK阻害剤と併用する可能性があります。選択的CDK2阻害剤の第1相試験では、CDK4/6阻害剤および内分泌療法を受けた/進行したホルモン受容体HER2陰性の進行・転移性乳がん患者において、部分奏効が2例確認されました。CDK2阻害剤を約8カ月間投与した結果、1人の患者さんでは最大54%の腫瘍縮小が認められ、2人目の患者さんでは約9カ月間の投与ですべての標的病変の縮小が100%認められました。
最初の患者さんのベースラインと8週目のスキャンをお見せします。単剤での安全性プロファイルは許容範囲内であり、現在、併用療法を検討している。第1/2相試験は、’23年第2四半期に完了する予定です。次に、Valneva社と共同開発している6価のライム病ワクチン候補について説明します。
第2相概念実証試験からさらに良好なデータが得られ、今年の第3四半期に第3相試験を開始する予定です。投与レジメンは0ヵ月、2ヵ月、6ヵ月とプライムで、その後ライムの季節が始まる前に定期的にブースターを投与することになっています。当社の第2相試験は、5歳から17歳までの小児科患者を対象としており、引き続き実施しています。ライム病は季節性があるので、私たちの目標は、各シーズンの初めに高い抗体価が得られるようなレジメンを確立することです。そこで、プライマリーシリーズの1年後のブーストを検討しました。
その結果、北米とヨーロッパに存在する6つの血清型すべてに対して、3回の一次接種スケジュール後に、シーズン1で14〜31倍、シーズン2で51〜69倍という大幅な抗体上昇を第2相試験で確認した。このワクチン候補は、試験したすべての用量レベルで概ね良好な忍容性を示し、今後の開発とこの衰弱した疾患の予防に役立つ可能性に期待を寄せています。前四半期には、デュシェンヌ型筋ジストロフィーの遺伝子治療第1b相試験において、1年後までジストロフィンの強固な発現が確認されたことをお伝えしました。また、運動機能に関するデータをお見せしたいと思います。
先日、非常に悲しいお知らせがありました。第1b相試験の歩行不能コホートで進行したDMDの患者さんが、低酸素血症と心原性ショックを呈し、亡くなられたのです。この患者さんは16歳で、歩行不能コホートの中で初めて、免疫抑制レジメンの一部としてステロイドとともにラパミューンを投与されました。第3相外来試験では、ラパムーンは使用されていません。ほとんどの非歩行型DMD患者と同様に、この患者も基礎疾患として心機能障害があり、より進行した疾患でした。
活動性のウイルス感染の証拠があり、これがどのように結果に寄与したかを調査しています。より進行した歩行不能の患者さんを対象とした第1b相試験を再開するための次のステップを明確にするために、さらなる評価が必要となります。それでは、この試験で得られたデータをご紹介します。外来患者コホート — すみません、ここでもう1つ言いたいことがありました。
この試験には19名の患者さんが登録され、そのうち16名は第3相プログラムで選択された用量を投与され、3名は以前研究された低用量が投与されました。治療後1年で、年齢とベースライン機能をマッチさせた外部コントロールと比較して、North Star Ambulatory Assessmentで測定した歩行機能に5.6ポイントの改善が見られました。この年齢と病期の患者さんでは、外部コントロールで示されるように、通常、歩行機能がかなり低下することを考えると、これは特に励みになります。右側には、治療期間が3年に近づいている、あるいは3年を超えている参加者が6人いることが示されています。
第1b相試験の外来患者コホートは、第3相CIFFREO試験の患者集団と類似していますが、平均年齢は若干高くなっています。本試験における良好なベネフィット・ツー・リスクのプロファイルと外来患者集団で観察されたことを考慮し、データモニタリング委員会と協議した結果、当社のDMD遺伝子治療の安全性プロファイルはこの患者集団において管理可能であると確信しています。eDMCや他の医療専門家と相談しながら、追加の緩和を我々の試験に追加しているところです。規制当局からのフィードバックを待って、今後数ヵ月以内に第3相臨床試験施設の再開を開始し、トップライン結果を報告し、臨床試験の成功を条件として、23年末までにBLAを提出する可能性があると予想しています。
次に、癌による悪液質に対する当社の候補である内科とponsegromabについて説明します。これはGDF-15をターゲットにしています。GDF-15はがん患者さんで頻繁に上昇し、食欲減退や体重減少を引き起こし、予後不良と関連します。また、心不全やCOPDなど他の慢性疾患に伴う悪液質も治療できる可能性があります。
次にお見せするのは、心強い第1b相のデータです。Ponsegromabは、抗腫瘍治療を受けているがん患者で、過去6ヶ月間に5%以上の体重減少、または2%以上の体重減少で肥満度が20kg/m2未満、またはサルコペニアと診断された10名の患者を対象に評価されたものである。Ponsegromabの投与により、がん性悪液質患者における循環GDF-15濃度が、健常者で観察されるレベル以下に抑制されることが確認されました。第1b相試験の予備データでは、ponsegromab投与により、過去のプラセボと比較して有意に体重が増加することが示されています。
12週目に投与を中止した後も、体重増加の良好なトレンドが維持されていることがわかります。グレーの点線は、生存率の改善に関連する過去のカットオフ値を示しています。当社は、プレシジョン・メディシンを実現するために、ロシュ・ダイアグノスティックス社とコンパニオン診断薬を共同開発中です。また、がん性悪液質を対象とした第2相試験を本年第4四半期に開始する予定です。
注射用GLP-1受容体作動薬は、糖尿病や肥満の患者さんにおいて血糖値や体重を強力に低下させ、心血管への効果も証明されていますが、注射という投与経路のためにこの薬効は十分に利用されていません。当社の低分子経口GLP-1受容体作動薬であるダヌグリプロンは、注射剤に代わる便利な経口剤を提供する可能性があり、2型糖尿病、肥満、NASHの治療薬として評価されています。この強力で投与が容易なGLP-1薬物群の使用をプライマリーケアに拡大することをビジョンとして、私たちの内科学研究グループで開発されました。ここでは、2型糖尿病を対象とした第2相試験のデータを紹介します。
本試験では、長期的な血糖値の推移を表すHbA1cと体重が、プラセボと比較して用量依存的に減少することが確認されました。200ミリグラムを1日2回投与した12週間後、HbA1cは約1.6%減少し、体重は5.4キログラム減少しました。安全性および忍容性プロファイルはGLP-1クラスと同様であり、最も頻繁に発生した有害事象はGI関連でした。当社は、22年半ばに200ミリグラム1日2回までの用量で第2b相漸増最適化試験を開始し、来年の第1四半期に肥満症を有する非糖尿病患者を対象とした第2b相試験を完了する予定です。
最後に、パイプライン全体の最近のマイルストーンと今後のマイルストーンをご紹介します。青い実線は達成されたマイルストーン、青い点線は予想されるマイルストーンを示しています。太字のプログラムは、今後期待される主要なイベントです。右のプログラムのいくつかは、すでにLightspeedに指定されており、開発スケジュールが加速されているか、Lightspeedの指定が検討されていることを意味します。
最後に、内科学研究部門の最高科学責任者を退任されるMorrie Birnbaum氏に対し、この7年間にわたる多大な貢献に感謝の意を表したいと思います。薬理学副学長、医学部教授、血管生物学・治療学プログラムディレクターなど、10年にわたる学術界でのキャリアを経て、イェール大学医学部からビル・セッサを迎えます。ビルはこの分野の傑出したリーダーであり、画期的な科学者であり、名高い革新者です。彼はその素晴らしいビジョンと洞察力を、私たちの心血管疾患と代謝性疾患の研究に活かしてくれることでしょう。ご清聴ありがとうございました。
ご質問をお待ちしています。では、フランクにお願いします。
Frank D’Amelio — 最高財務責任者
ミカエルさん、ありがとうございます。リリースをご覧いただいていると思いますので、財務に関するハイライトをいくつかご紹介させていただきます。COVID-19ワクチンは、今回も四半期業績にプラスの影響を与えましたが、COVID-19の状況については、すでにアルバートとミカエルが重要なポイントについて述べています。損益計算書に目を向けると
21年第4四半期の売上高は、COVID-19ワクチンの売上とその他の主要な成長要因の好調な業績により、事業ベースで106%増加しました。収益を見ると、COVID-19ワクチンの直接販売とアライアンス収入、パックスロビドの貢献を除くと、第4四半期は年初来の9ヵ月間より鈍化し、営業的に2%減少しました。第3四半期の電話会議で説明したように、米国および海外における販売日数の減少による4%のマイナス影響、約5億ドルのマイナス影響がありました。
この影響を除けば、営業利益成長率は2%となり、残りの期間で経験した1桁台半ばから後半の成長率を下回る ことになります。これは通期見通しにも織り込み済みですが、簡単にご説明します。バイオ医薬品事業では、21年第4四半期は、COVID-19ワクチンの供給に先立ち肺炎球菌ワクチンの接種が好調だったため、プレブナールの2020年第4四半期からの厳しいコンプに直面したことをご記憶にあると思います。今期と比較期のワクチンを除外すると、5%ポイントの成長が加わります。
ワクチンと販売日数に関連する異常なコンプ期間の差異を調整すると、当社の収益成長率は約7%となり、最近の業績とほぼ同じになります。通期では、営業収益の成長率は92%でした。コミルナティの直販・アライアンス収入とパックスロビッドを除くと、2021年の営業収益の伸びは6%でした。これは、2020年から2025年末までの収益CAGRが少なくとも6%であるという当社の予測と一致しています。
もちろん、様々な要因で四半期や年間の成長率に多少の変動はありますが、2025年まで少なくとも6%のCAGRを引き続き見込んでいます。ここに示した調整後売上原価の増加により、今期の売上総利益率は2020年第4四半期と比較して約16ポイント低下しましたが、これはほぼすべてCOVID-19ワクチンの影響によるものです。第4四半期の調整後SI&A費は、主にComirnatyを含む製品レベルの支出の増加および医療制度改革の売上ベースの手数料の増加により増加しました。今期の調整後研究開発費の増加は、主に当社の経口COVID-19治療薬に関連する追加支出を含む後期パイプラインプロジェクトへの投資の増加によるものです。
[【技術的困難]アルバート・ブーラ — 会長兼最高経営責任者
フランク、接続が切れたようですね。
Chris Stevo — 上席副社長兼投資家対応部長
はい、聞こえていますよ、フランクさん。どうぞ。
フランク・ダメリオ — 最高財務責任者(CFO
OK。どこから話したかわからないのですが、22年度の財務ガイダンスからお話しします。このガイダンスには、COVID-19ワクチンのビジネスが含まれています。コミルナティの予想売上高については、今後も引き続きお知らせしていきます。
また、今回初めてパクスロビドに関する予想収益についてもお知らせします。ただし、コミルナティを除く事業については、EPSガイダンスを提供する予定はありません。同様に、パクスロビドについてもEPSのガイダンスを行いません。当社の収益ガイダンスはファイザーにとって記録的なものであり、会社全体の収益は9800万ドルから1020億ドルの範囲になると予想しており、中間値の業務成長率は24%に相当するものと思われます。
この収益範囲には、外貨の変動による約11億ドルのマイナス影響と、メリディアンの売上喪失による約3億ドルの影響が予想されますが、これらはいずれも貴社のモデルでは考慮されていない可能性があることをご考慮ください。COVID関連の売上については、COVID-19ワクチンの年間売上を約320億ドルと予想しており、12月17日に発表したガイダンスから約10億ドルの増収となりました。パクスロビドについては、約220億ドルの売上を見込んでいます。つまり、COVID関連収入を除いた売上高は、中間値で460億ドル、営業利益で5%の成長を見込んでいます。
これは、2020年から2025年の間に引き続き見込んでいるCAGR6%を若干下回っていますが、途中で変動があることをお断りしておきます。コストと経費のガイダンスについて、少し詳しくご説明します。調整後売上原価については、32.2%から34.2%のレンジを見込んでいます。コミルナティの発売から12カ月以上経過していることから、売上高が同程度と仮定した場合、売上原価率に対するマイナスの影響は2021年よりも小さくなると考えています。
さらに、パックスロビッドは、2022年の売上高に対する売上原価率に非常に良い影響を与えると予想しています。調整後SI&Aについては、125億ドルから135億ドルを見込んでおり、中間値で9億ドルの増加です。調整後の研究開発費のガイダンスレンジは、中間値で105億ドルから115億ドルと予想しており、これは昨年より約5億ドル増加します。通期の調整後実効税率は、2021 年度をいくぶん上回る約 16%となる見込みです。
これらの前提条件により、為替によるマイナス0.06ドルの影響を除くと、調整後希薄化後EPSは6.35ドルから6.55ドル、または中間値で前年度比47%の事業成長率を達成する見込みです。なお、この情報は貴社のモデルにとって有益なものであると思われます。当社のガイダンスでは、加重平均株式数を約58億株と想定しており、これは2021年に比べ約1億株増加することに留意してください。これは、当社が通常従業員報酬として毎年発行している株式数を考慮したものです。
21年比で1億株の増加は、中間値でEPSを約0.10ドル減少させます。多くのモデルで、’22年の株式数は’21年比で横ばいを想定しているようですが、その点はいかがでしょうか?22年第1四半期以降、無形資産償却費の調整後財務数値の取り扱いを変更することを決定しました。従来は、大型のM&Aに関連する償却費のみを除外し、すべての無形資産償却費を除外していました。
これにより、2022年の調整後希薄化後1株当たり利益に0.06ドル寄与する見込みで、同業他社との比較可能性を向上させるのに役立ちます。2022年のガイダンスでは、再び自社株買いを行わないことを想定しています。ファイザーは2020年、2021年ともに自社株買いを行っていないことに留意してください。また、当社は引き続き、さらに53億ドルの自社株買いの未使用の権限を保有していますが、価値を高める可能性のある事業開発の機会を考慮し、2022年に自社株買いを行うことはないと考えています。
さて、GSKとの消費者向け合弁事業における当社の32%の株式について、一言ご報告します。ご存知の通り、GSKは2022年夏に合弁会社の68%の株式のうち少なくとも80%について会社分割を実施する意向を表明しています。私たちは、当社の株式を非中核資産として、その価値の実現を目指していくことをお話ししました。その方法・時期は未定ですが、いくつかの選択肢が考えられますので、株主にとって最も価値のある方法でこの資産をマネタイズしていきたいと考えています。
当社はこのJVから年間約6億ドルの税引前利益を得ていますが、これは分割取引によって変わるものではなく、当社の32%の出資比率を変更することなく2022年まで継続することをガイダンスでは想定しています。ここで、COVID-19ワクチンの寄与の見通しと当社の提携契約について、いくつかの前提条件と背景を簡単に思い出してください。ファイザーとバイオインテックのCOVID-19ワクチンの共同研究は、売上総利益を50対50で分配する仕組みになっています。ドイツとトルコを除く全世界の提携収入の大部分はファイザーが計上し、当社はバイオNTechから利益配分を受け、中国地域には参加していません。
当社は、2022年末までに合計40億回分の製造が可能であると引き続き予想しています。2022年のCOVIDワクチンの予想売上高が10億ドル増加して約320億ドルになったのは、主に12月中旬以降に締結した契約の影響であり、事前のガイダンスから切り離したものです。オミクロンやその他の亜種によって必要となる可能性のあるものを予測することはできませんが、ワクチンが新しく発売された2021年に直面し、ワクチンの投与を受けた人がほとんどいない状況に比べ、このガイダンスには年間を通じてアップサイドの可能性が少ないことも注意しておきたいと考えています。COVID-19ワクチンの売上原価には、製造・販売コスト、ロイヤリティ、バイオテック社への売上総利益50%相当額が含まれています。
COVID-19ワクチンの貢献による調整後税引前利益率は、2021年の売上高比率20%台後半より若干高くなると予想しています。コミルナティの状況とは異なり、パックスロビドの需要は、特定の政府との協議の結果や将来のコロナウイルスのパンデミックに対する備蓄のための購入の可能性によって、これらの水準から上向くはずです。COVID-19ワクチンとパックスロビドの寄与を両期間から取り除くと、2022年の収益レンジは450億ドルから470億ドルとなり、中間値で約5%の事業収益成長率となると予想していることがおわかりいただけると思います。なお、このガイダンスでは、メリディアンの旧収益貢献額約3億ドルを除外しており、21年の全四半期は、メリディアンの売却に伴う非継続事業の会計処理を除外して再修正しています。
今後、当社はコミルナティの直販およびアライアンス収入、ならびにパックスロビドからの推定利益を除外した業績ガイダンスを発表する予定はありません。しかし、先ほど、業績見通しの参考として、2022年のコミルナティの税引き前利益率に関する私の見解をお伝えしました。パクスロビドについては、低分子医薬品の典型的なマージンであり、コミルナティとは異なり、税引き前利益の希薄化にはつながらないと考えています。さらにご参考までに、数年前、COVID-19が存在する前に、私は2022年にコミルナティとパクスロビドを除く事業で税引き前利益率40%超のレベルに到達する道筋があるとお話ししました。
今後とも、このスライドにあるような展開の機会を生かし、慎重な資本配分を続けてまいります。要約すると、当社の成長ドライバーの継続的な好業績に基づく、極めて好調な四半期および年度となりました。今年度はガイダンスを引き上げ、すべての主要指標においてガイダンスを達成もしくは上回りました。当社のパイプラインは引き続き前進しており、その前進を支えるために過去最高額の投資を行っています。
先週、アリーナの株主は、ファイザーによる同社買収を承認する投票を行いました。独占禁止法の承認などの買収条件を満たした上で、早ければ2022年前半にアリーナ社の買収を完了させることを目標としています。2025年以降も、最高の外部科学にアクセスし、患者さんにブレークスルーをもたらすために、2022年を通して事業開発に関して活発な活動を行うことを引き続き期待しています。それでは、クリスに代わって質疑応答を始めたいと思います。
クリス・スティーボ — シニア・ヴァイス・プレジデント兼インベスター・リレーションズ担当チーフ
フランク、ありがとうございます。皆さん、技術的な問題で申し訳ございませんでした。念のためお伝えしておきますが、準備した発言はウェブサイトに掲載しています。もし、技術的な問題で聞き逃したことがあれば、準備した発言をご覧ください。
また、技術的な問題から、質疑応答の時間を少し長めにとって、皆様のご質問にお答えしたいと思います。シルヴィア、最初の質問をお願いします。
質疑応答
運営者
ありがとうございます。最初の質問は、バンク・オブ・アメリカ証券のジェフ・ミーチャムさんからです。
Geoff Meacham — バンクオブアメリカ・メリルリンチ — アナリスト
やあ、みんな。質問を受けてくださってありがとうございます。2つだけです。1つ目は、パックスロビドのガイダンスについてです。
あなた方が契約済みだけを織り込んでいるのは知っています。しかし、現在検討されている契約や用量について、一般的な感覚をお聞かせください。また、それは供給量の増加に依存するのでしょうか?2つ目の質問、外部BDについてですが、アルバート、その戦略は理解しています。不確実なのは、あなたが持ち込んだ製品のいくつかをスケールアップできるかどうかだと思います。COVIDの長期的な貢献度が想定よりも低い場合、よりインパクトのある大型案件を手がける意欲はどうでしょうか?あなたには明らかに能力があります。
ありがとうございます。
アルバート・ブーラ — 会長兼最高経営責任者
ありがとうございます。アンジェラさん、パックスロビッドを少し持っていきますか?
アンジェラ・ホワン — エグゼクティブ・チーム兼ファイザー・バイオファーマシューティカルズグループ社長
もちろんです。それで、現在、世界の100以上の国や政府と積極的に協議しています。ですから、話し合いはとてもうまくいっていると言えるでしょう。契約の状況ですが、おっしゃるとおり、すでに結んでいる契約も含まれています。
もちろん、この数字は毎日変わりますし、契約や販売契約は文字通り毎日結ばれています。ですから、この数字は要注意だと思いますし、今後も動きがあることを期待しています。私たちの製品への関心は非常に高いと思います。そして確かに、臨床プログラムが発展し、出現し続けるにつれて。
ご存知のように、現在はハイリスク試験のみです。標準的なリスクと予防的な試験もあります。また、完全な臨床プログラムは、契約や注文を促進するもう一つのポイントになると思います。ですから、本当にうまくいっていると思いますし、この分野ではさらに多くのことを成し遂げられると思います。
アルバート・ブーラ — 会長兼最高経営責任者
ありがとうございました。Aamir、BDについてコメントをお願いします。
Aamir Malik — エグゼクティブ・バイスプレジデント、チーフ・ビジネス・イノベーション・オフィサー。
もちろんです。Geoff、ご質問ありがとうございました。トップラインに関しては、信じられないほど柔軟に対応するつもりです。私たちは、真のブレークスルーとなる可能性のある化合物に最も関心があると何度も言ってきました。
これは、臨床開発の後期段階でも、医療技術革新の初期段階でもかまいません。私たちは、適切な選択をし、真の価値を付加するための科学的能力を有するTA、腫瘍、I&I、希少疾患、ワクチン、内科、病院などに偏るつもりです。また、案件のタイプについても柔軟に対応するつもりです。買収はもちろんですが、戦略的パートナーシップやアライアンスも視野に入れています。
実際、私たちの最高の成功は、資本を必要としない協力関係からもたらされたものです。もし、戦略的で価値を創造し、先ほど述べたような基準を満たすような大きな機会があれば、そのために活用できるバランスシートがあるのは明らかです。ですから、そのような案件を検討することは可能です。しかし、私たちは、シナジー効果のある取引そのものよりも、先ほど申し上げたような優先順位について話し、それに焦点を当てるつもりです。
アルバート・ブーラ — 会長兼最高経営責任者
アミール、ありがとうございます。そしてGeoff、2つのポイントともよく聞かれると思うので補足しておきます。パックスロビドについては、明らかに、今ある数字よりはるかに大きくなる可能性があります。しかし、これは過去にもやっていませんし、今すぐにガイダンスとして可能性を示すためにやるつもりもありません。
契約済み、あるいはすでに合意しているがまだ契約していない、しかし価格と数量は合意している、といった具合に、多かれ少なかれ確実なものに基づいてガイダンスを提示しています。ですから、ワクチンでスタートしたときのことを思い出していただければと思いますが、当初、私たちは第1四半期に150億ドルというガイダンスを出していたと思います。最終的には360億ドルを売り上げました。今回、パックスロビッドの最初の生産でさらに強力なスタートを切りました。
すでに1億2,000万回の治療実績があり、現在行っている話し合いが実現すれば、さらに上乗せすることが可能です。事業展開についても、サイズに関する質問が多いので強調しておきたいと思います。私たちは規模にこだわることはありません。偏っているのはディールです。
しかし、プレミアムを正当化するためには、大幅なコストシナジーを実現する必要があります。これは……他の、たとえば会社の歴史のある時期には非常に有益な取引になるかもしれませんが、今ではないのです。今、当社は製造マシンを持っていますが、最高のパフォーマンスを発揮しています。研究開発マシンも持っていますが、最高のパフォーマンスを発揮していますし、商業マシンは、実行力と提供力の点で業界のリーダーであり続けているのです。ですから、私が一番やりたくないことは、相手企業の株主に対してプレミアムを正当化するために、製造拠点を閉鎖し、研究拠点を統合し、現場部隊を統合して、コストシナジーを正当化できるような取引をすることなのです。
今は、会社の勢いをそぐような時期ではありません。今こそ、製造装置、研究装置、商業装置に、自社で有機的に生産するものに加えて、より多くの基板を投入する時なのです。そのために、このような分野での事業展開を目指しているのです。では、次に行きましょう。
運営担当者
次の質問は、ウェルズ・ファーゴのモヒット・バンサルさんです。
Mohit Bansal — ウェルズ・ファーゴ証券 — アナリスト
素晴らしい。ありがとうございます。私の質問を受けてくださってありがとうございます。パックスロビドについて一つ。
パックスロビドについて、物流やアクセスに関する問題が報道されていますね。今のところ供給が逼迫していることは理解しています。特に、在宅検査が標準となり、診断から5日以内にこの薬を服用する必要がある世界では、供給が問題でなくなったときに、どのように物流を改善しようとしているのか、お考えを聞かせてください。ありがとうございました。
アルベルト・ブーラ — 会長兼最高経営責任者
供給に関する物流の問題があるとは言えません。しかし、アンジェラさん、それをお願いします。
アンジェラ・ホワン — エグゼクティブ・チーム兼ファイザー・バイオファーマシューティカルズグループ社長
EUAが承認されて以来、米国政府から26万5,000人分の投与量が割り当てられています。
この26万5,000人分のうち、85%が注文されています。そして、各州からさまざまな注文パターンが出ています。ある州は割り当て分の100%を注文しています。ある州は割り当て分の100%を注文し、他の州は80%、70%といった具合に、さまざまな注文パターンがあります。
ですから、割り当て分まで注文していない州は、本当に一握りだけです。しかし、ほとんどの場合、週ごとの注文はどんどん増えており、非常に強力な発注が行われていると言えるでしょう。ですから、ドローダウンと使用率は非常にうまくいっていると思います。また、州によって割り当てが異なり、その状況も異なります。
それから、Albertが言ったように、ロジスティクスの問題はないと思います。当初、困難だったのは、パックスロビドを実際に配布する場所が州ごとに異なるシステムであったため、投与量がどこにあるのかが明確でなかったことだと思います。しかし、現在では、州レベルでも、ファイザーのウェブサイト上でも、さまざまなツールがオンライン上に公開されています。州政府のツールをファイザーのウェブサイトにも掲載し、HCPと患者さんの両方が、パクスロビドがどこで入手可能か、どこで注文や処方ができるかを確認できるようにしました。
その点では、すべて解決されたと思います。将来的には、診断から良好な結果が得られ、迅速に処方され、患者さんが薬剤を迅速に入手できるようになるまでのエンド・ツー・エンドをシームレスにすることが、私たちの目標です。検査や診断の観点だけでなく、遠隔医療の観点や薬局の観点からも、診断から治療までの患者さんの道のりをできるだけ早く、効率的にするために、多くのパートナーと連携しているところです。ですから、これらすべてが整っており、今後、発売や利用が増えるにつれて、さらに詳しい情報が得られるでしょう。
Albert Bourla — 会長兼最高経営責任者(CEO
また、アンジェラさんがおっしゃったことに少し補足をします。85%というのは……アメリカ政府に提供している数量からすでに注文されているもので、これは非常に高い数字です。例えば、ワクチンの最初の月の同じ数字は、当時のことをよく覚えているのであれば、それよりも劇的に低かったのです。
そして、それは本当に州によって変動します。ですから、今現在、数量が出揃ったら、すぐに注文している州もあります。また、流通が軌道に乗るまで時間がかかる州もあります。一般に、ワクチンの最初の1ヵ月は、以前よりもずっと効率的です。
また、非常に重要なのは、毎週、一定の補充が行われていることです。今はまだ時期尚早なので、スクリプトのデータはありませんが、各州が蓄えている数量がなくなり、すぐに注文が入るということです。ですから、最初の1カ月は、アメリカ政府との連携による投与量の配分という点では、かなり満足のいくものだったと言えるでしょう。また、Angelaが説明したように、ツールも劇的に改善されました。
しかし、より大きな改善は、2ヶ月目にはより多くの量を利用できるようになることです。なぜなら、今問題になっているのは、この薬を見つけようとする人が、州内の数カ所にしかいないことです。ですから、今月はそれが大きく変わるでしょう。そして、基本的に、3ヵ月目には、かなりの数量が納入されることになると思います。
なるほど。次の質問に行きましょう。
オペレーター
次の質問は、BMO Capital MarketsのEvan Seigermanです。
エヴァン・セイガーマン — BMOキャピタル・マーケッツ — アナリスト
こんにちは、皆さん。私の質問を受けてくださって、本当にありがとうございます。私はあなたがアリーナの取引のためのSECのレビュープロセスに関する最新情報を提供することができればと思っていました。私の記憶が間違っていなければ、最近、あなたとArenaがHSR法の申請をし直し、FTCがさらに30日間審査できるようにするという手続き上の動きがあったはずです。
それから、BD取引による収益が130億ドルに達すると予測する根拠について、ぜひ教えてください。それは、具体的なターゲットとターゲットの組み合わせを念頭に置いているということでしょう。具体的な目標やその組み合わせについて教えていただければ幸いです。ありがとうございました。
アルバート・ブーラ — 会長兼最高経営責任者
そうですね。ありがとうございました。最後の1つについて、念のためですが、これは私たちの想定ではありません。私たちの想定は130億ドルよりもはるかに高いものです。
今お伝えしたのは、これまでに契約した案件の総意です。FTCの審査については、当社の法務顧問であるダグ・ランクラーに審査をお願いしたいのですが、いかがでしょうか。
Doug Lankler — ゼネラルカウンセル — アナリスト
はい。ご指摘のとおり、私たちは再申請を要請しましたが、これは珍しいことではありません。もちろん、この買収には通常のクロージング条件、独占禁止法上のクリアランス、株主の承認が必要ですが、ご存知のように、私たちはこの承認を得ています。私たちは、この取引が今年の上半期に完了するという、私たちが提案した感覚から大きく外れることはないと考えています。
今年の上半期に完了すると考えていることに変わりはありません。
アルバート・ブーラ — 会長兼最高経営責任者
ありがとうございます。そして、Aamir、これはコンセンサスの数字であって、我々の数字ではないことを説明しましたが。2030年の売上高が130億ドルということですが、このコンセンサスは、私たちが契約した案件のキャッシュに対するものですが、他に何かコメントはありますか?
Aamir Malik — エグゼクティブ・バイスプレジデント、チーフ・ビジネス・イノベーション・オフィサー。
そうですね。唯一付け加えるとすれば、アルバートが概要を説明した2019年以降のすべての基板と案件の進行について、我々は非常に良い感触を得ているということです。このグループでは、かなりの数の承認とEUA、申請、そしてかなりの数の第3相の開始が確認されています。ですから、その基板は順調に進行していると考えています。
そして130億ドルというのはコンセンサスナンバーです。私たちの期待値はこれよりもはるかに高いものです。また、多くの取引があります。トリリウム、バイオヘブン、そして最近行ったmRNAの取引についても、まだコンセンサス予想に織り込まれていないものがあると聞いています。
アルバート・ブーラ — 会長兼最高経営責任者
ありがとうございました。次の質問をお願いします。
オペレーター
次の質問は、Evercore ISI のウマー・ラファトです。
Umer Raffat — Evercore ISI — アナリスト
こんにちは、皆さん。私の質問を受けてくださって、本当にありがとうございます。今日はワクチンについて2つほど質問させてください。まず、インフルエンザ・ワクチンについてですが、9月からmodRNAの臨床試験を実施されていますね。
そして、インフルエンザ用の自己増幅型mRNAの新しい試験を開始されたようですね。インフルエンザで2つ目のmRNAプログラムを進めるという決定は、現在進行中の第1世代インフルエンザのフェーズ1から何か新しいデータが出たことが引き金になったのでしょうか?次に、オミクロン特異的ブースターについてですが、おそらく、通常のCOVIDワクチンとの免疫原性の違いや欠如に関するいくつかの新しいデータに照らして、質問させてください。オミクロン特異的ブースターの優越性を通常のものと比較して示すことができると、どの程度確信されていますか?また、規制上の基準はどのようなものでしょうか?ありがとうございました。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
ありがとうございます。どうもありがとうございました。その質問はミカエルが受けられると思います。インフルエンザ・ワクチンについてですが、念のため申し上げますと、計画では常にインフルエンザのsamRNAを開始し、2つのプログラムを並行して実行することになっていました。
SAを実施せざるを得ないようなデータを見たわけではありません。それは常に計画されていたことです。私たちは、SAで新しい形のmRNA技術を進めています。次世代のRNA技術として最も有望なものの1つです。
しかし、ミカエル、そのことについて、また、オミクロン・スペシフィックについて、私たちの優位性に対する確信について、何かコメントはありますか?
Mikael Dolsten — ワールドワイド研究開発・メディカル担当プレジデント
ありがとうございます。まず第一に、mod mRNAのデータから、さまざまなレジメンや多価のコンストラクトに関する試験データを蓄積しているところです。私たちは、インフルエンザワクチンの開発を熱望しているという見解に変わりはありません。現在、最も積極的なスケジュールは、mod mRNAに集中しています。
私たちの計画は、現在の7価の標準治療に対して差別化できるものを開発することです。他社も同じようなことを言っていますが、現時点では、mod mRNAをベースにしたmRNAで差別化できる可能性があると考えています。Albertが言及したように、私たちは実際に自己増幅型のINDを申請しています。プロトコルはすでにClinicalTrials.govにアップされていると思いますが、投与は今後2、3カ月以内に行われる予定です。
このプラットフォームは、混合ワクチンに特に適しており、mRNAの負担が大幅に軽減され、複数の異なる病原体の混合ワクチンを長期にわたって製造することが可能です。インフルエンザにおけるmodRNAの進展については、今後も随時お伝えしていきます。そして、これが実現可能な道であることを示唆するデータを見て、私たちは差別化されたワクチンを目指してアプローチを改良しているところです。
アルベール・ブーラ — 会長兼最高経営責任者
オミクロンはどうでしょうか?優位性についての自信は?
Mikael Dolsten — ワールドワイド研究開発・メディカル担当社長
そうですね。規制当局としては、オミクロンのブーストが成功すれば、野生型ワクチンによる同様のブーストに対して、オミクロンの中和抗体がより高くなり、他の既承認株に対しても許容できる力価が示され、幅広い保護が得られると期待していますが、おそらくオミクロンをより高くすることになると思います。私は、科学的な検証を行うべきであると考えています。データが出るまで何週間もかかると思います。
先ほども申し上げたように、この試験には3種類の投与方法があり、オミクロンと野生型との比較です。これは、過去に3回接種した上に、過去に2回、1回または2回のオミクロンを接種したものです。これは非常に興味深いデータセットになるでしょうし、その後、オミクロンかナイーブか。ですから、本当に興味深い試験だと思いますし、多くのデータを抽出し、その優越性を得ることができるかどうかを報告したいと思います。
しかし、いずれにせよ、私たちの現在のワクチンは、3回の投与で活性があり、関連する中和抗体を上昇させるということを、強調しておきたいと思います。そして、私たちが見ることのできるT細胞応答は、実際のエビデンスにおいて、入院や死亡に対する現在のワクチンの効果的な防御に寄与するものである可能性が高いです。しかし、私たちの科学は、時間をかけてmRNAワクチンをさらに改善する方法について、いくつかの次元で進行していますが、それらはすべてかなり良いものです。
ですから、ファイザーは、バイオNTechとともに、複数のアプローチを通じて、この分野のリーダーであり続けることを期待すべきです。
アルバート・ブーラ — 会長兼最高経営責任者
ミカエルさん、ありがとうございました。次の質問をお願いします。
オペレーター
次の質問は、カンターのルイーズ・チェンさんからです。
Louise Chen — Cantor Fitzgerald — アナリスト
私の質問を聞いてくれてありがとうございます。最初の質問ですが、COVIDを除く基礎的なビジネスに対する主なプッシュとプルは何でしょうか?また、現在のような不安定な状況にもかかわらず、2025年までの売上高ガイダンスを達成できると確信する根拠は何でしょうか?それから、TL1A抗体とその開発状況、データの報告についてお聞きしたいのですが。データ報告時期について、何か変更があったのでしょうか?ありがとうございました。
アルベルト・ブーラ — 会長兼最高経営責任者
ありがとうございました。6%という数字に自信を持てるのは、19年に設定したCAGR6%という目標を達成し続けているからです。そして、現在までのところ、6%を達成しています。特に今年度は、基礎的なビジネスでは5%です。
しかし、多少の変動はあります。しかし常に、今年はChantixの売上が前年比で減少する年であることは分かっていましたので、この契約はかなり大きな影響を及ぼしました。アンジェラさんには、インプットとその進捗状況について、またミカエルさんには抗体の問題について、もう少し詳しくお聞きしたいと思います。アンジェラさん?
アンジェラ・ホワン — ファイザー・バイオファーマシューティカルズグループのエグゼクティブチーム兼グループプレジデント
ルイーズさん、ありがとうございます。6%の自信は、本当に2つのことが要因になっていると思います。まず、現在から2025年までの間に行われる上市、そしてそれが私たちの成長を引き続き牽引していくでしょう。しかし、もうひとつ重要なことは、当社のインライン・ポートフォリオでは、どの製品にもまだ成長の機会があるということです。
さまざまな方法で成長することができますよね?まだ診断が不十分な患者さんがいます。ですから、新たな診断により、EliquisとVyndaqelは引き続き多大な成長を遂げることができます。多くの製品で、まだクラスの成長が見込めます。CDK4/6阻害剤、XTANDI、BRAF/MEKTOVIを考えてみてください。
これらはすべて、クラスの観点から見ると、まだ十分に活用されていない治療法だと思います。だから、そこに成長があるのです。そして最後に、すべての製品について、強力な臨床プロファイルと強力なライフサイクル・サポートがあるため、市場シェアの点で成長する機会があります。ですから、まだまだ大きな成長が見込めると思います。
中核となるインライン・ブランドの成長は、まだ十分ではありません。それに加えて、新発売のブランド、これが私たちの成長の原動力となるのです。
アルバート・ブーラ — 会長兼最高経営責任者
ミカエル?
Mikael Dolsten — ワールドワイド研究開発・メディカル担当社長
アンジェラさん、ありがとうございます。TL1Aについては、前回の決算説明会で、内視鏡的改善率34%、バイオマーカー48%という、標準治療をはるかに上回る強力なデータを示しました。この試験は、非常に早く登録が完了しました。もう完全に登録されています。
完全な臨床試験の結果は第4四半期に発表される予定です。前回の試験での有望なデータに基づいて、中間解析の機会を検討中で、保留中のデータにより、主要な試験に向けてプログラムの開発を加速できる可能性があります。ですから、全体としては、非常に順調で、非常に速いペースで進んでいます。
Albert Bourla — 会長兼最高経営責任者
ありがとうございました。次の質問をお願いします。
オペレーター
次の質問は、コーウェンのスティーブ・スカラ氏からです。
スティーブ・スカラ — コーウェン・アンド・カンパニー — アナリスト
ありがとうございました。はっきりさせておきたいのですが、ファイザーがパックスロビドについて保守的でありたいということは理解しています。しかし、ファイザーは2022年の可能性について表面を削っただけで、その表面を削ったものが2022年のパクスロビドガイダンスの内容であるように思えます。ですから、その発言に反対であれば言ってください。
次に、もう一度はっきりさせておきたいのですが、事業開発なしに25年から30年にかけてファイザー全体が成長することはないとお考えですか?最後に、ダングリプロンについてですが、スライド39に非常に良いデータがあります。この試験の中止率はどの程度だったのでしょうか?また、投与量をさらに増やすことは可能でしょうか?また、ファイザー社は12週以降も体重減少を期待しているのでしょうか?ありがとうございました。
Albert Bourla — 会長兼最高経営責任者(CEO
それでは、最初の2つの質問を私が行い、研究の方はミカエルが行います。私たちは保守的なガイダンスを出しているわけではありません。私たちには原則があり、それに従っています。
その原則とは、すでに締結された契約、あるいは締結が間近に迫っている契約に対してのみ、ガイダンスを与えるというもので、主要な条件について合意しているからです。パックスロビドについては、このように聞いています。明らかに、これは私たちが今製造の準備をしている1億2千万本の治療薬のごく一部にすぎません。また、現在、さまざまな政府と話し合っていることのごく一部でもあります。しかし、例えば、各国政府と行っているすべての話し合いを受けて、どれだけのものが通過できるかをリスク調整し、ガイダンスを出すというようなやり方はしていません。
これは私たちがやっていることではありません。私たちが行うのは、ワクチンについても同じですが、特定の期限までに署名されたもの、あるいはすでに合意されたものだけです。フランクは先週と言ったと思いますが、この期限です。ですから、明らかに多くの可能性があるのですが、私たちは自分たちの保守性を少し数字に込めているわけではありません。
私たちは、自分たちが何を言い、なぜそれを言うのかを常に明確にできるよう、原則に従っているのです。では、そういうことですね。ミカエルさん、試験用量と12週遅れについてはどうですか?
Mikael Dolsten — ワールドワイド研究開発・メディカル担当プレジデント
ダヌグリプロンについては、私たちのデータに満足し、感動していただけたようでうれしいです。HbA1cによる血糖値の低下と体重の減少は、短い治療期間では最高の結果だと思います。忍容性と中止率は、投与量の漸増を1週間から2週間に延長したため、前回の試験より改善されました。また、全体的な安全性と有害事象は、注射剤で見られるような同等の漸増アプローチと非常によく一致していると思います。
この中程度の漸増速度で忍容性と投与中止を改善できることがわかったので、次の試験では、さらにゆっくりと、おそらく1カ月くらいまで投与量を漸増させる予定です。このプロファイルには非常に満足しています。次の試験では、投与レジメンを確定し、強力なプロフィールをもってピボタル試験の可能性を探ることができると思います。
Albert Bourla — 会長兼最高経営責任者(CEO
それでは。次の質問をお願いします。
オペレーター
次の質問は、ウォルフ・リサーチのティム・アンダーソンからです。
Tim Anderson — Wolfe Research — アナリスト
ありがとうございます。いくつか質問があります。RSVワクチンのデータは、以前は22年初頭と言われていました。今、あなたは22年前半と言っていますね。
それは、多少の遅れがあったということでしょうか?というのも、私にとっては早期とは1月中旬、2月、そのようなものだと思っていたからです。このような製品の承認申請について、臨床試験が成功したと仮定した場合、現実的な時間枠はどのくらいでしょうか?そして最後の質問ですが、イブランスの売上は軟調です。患者補助プログラムによるものとのことですが、その理由は何でしょうか?
他のCDK4/6製剤ではそのような影響は見られません。また、ファイザーでも他社でも、そういったプログラムが他のブランドに影響を与えるという話は一般的に聞いたことがありません。そこで、アクセスを維持するために価格を下げなければならないような、イブランスへの圧力が他にあるのではないかと思うのですが、いかがでしょうか。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
はい。インフルエンザに関する質問は何でしたか、ティム?
Tim Anderson — Wolfe Research — アナリスト
mRNAインフルエンザワクチンの承認申請までの現実的な時間について。
アルバート・ボーラ — 会長兼最高経営責任者(CEO
はい、ありがとうございます。では、ミカエルさん、行きませんか?RSVはどうですか?両方について話すことができます。今は成人と母体の両方がありますし、それからmRNAの方も。
そしてアンジェラさん、あなたはイブランスについて話してください。
Mikael Dolsten — ワールドワイド研究開発およびメディカル担当プレジデント
はい。RSVについては、母体と成人の登録が非常にうまくいっており、基本的には、完全に登録されていると言ってよいでしょう。ですから、私たちが求めていたイベント数を確保することが完全に目的です。両試験とも、第1四半期、第2四半期、あるいは第2四半期の後半のどこかで、読み切られるものと考えています。
イベントが蓄積されるのを見守るしかありませんが、非常に順調に進んでいます。RSVは結論が出始めており、そのデータを楽しみにしています。mRNAインフルエンザは、現在、いくつかの異なるタイプの投与レジメンから免疫原性を蓄積しているところです。mod mRNAを用いた最適な投与レジメンを結論づけることができれば、今年中に第2相、第3相試験を開始できる可能性があります。
しかし、もちろん、適切な第2/3相用量レジメンを特定する前に、推測するのは少し早いです。もし今年、そのような試験に着手するのであれば、この分野とこの成人集団で非常に大規模な試験を実施した経験から、非常に早く結論を出すことができると考えています。そのため、来年中には結論が出る可能性があります。しかし、一歩ずつ進めていくしかありません。
今のところ、私たちは勇気づけられ、そこから前進していくつもりです。
Albert Bourla — 会長兼最高経営責任者
ミカエルさん、ありがとうございます。それから、イブランスのアンジェラさんはいかがでしょうか?
アンジェラ・ホワン — ファイザー・バイオファーマシューティカルズグループのエグゼクティブチーム兼グループプレジデント
もちろん、イブランスの数量減少の主な理由は、患者支援プログラムであることを確認できます。2021年第4四半期は、2020年第4四半期と比較して、PAP処方が32%増加しました。これはすべて、COVID導入前と比較して53%増です。
このように、本当に膨大な量の有償処方箋が発生しています。そして、私は……これが本当に第一の理由です。また、年間を通じて、これは四半期ごとに見ていることですが、新患の受け入れが若干スローダウンしています。しかし、このような現象は、当社のポートフォリオの複数の製品で見られます。
しかし、このような現象は、私たちのポートフォリオの複数の製品で見られています。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
アンジェラさん、ありがとうございました。次の質問に移る前に、スティーブ・スカラからの質問のひとつに、25年から30年にかけての成長には事業開発が必要だと考えているかという質問に答えていないことに気づきました。これは明らかに、今のところ確信には至っていません。私たちは、LOEが170億ドル程度と明確に推定されると考えています。
また、LOE以上の成果を上げるためのパイプラインもあります。ですから、私たちの計算では、オーガニックに限り、プラスの成長軌道に乗せたいと考えています。先ほど申し上げた250億ドルというのは、LOEと[聞き取り不能]のバランス、その間に発明される新しいもの、そしてもちろん2030年までのCOVIDの軌道など、すべてに上乗せする必要があるのです。しかし、私たちは今、成長のために事業開発をまったく必要としていません。
必要なのは、例えば2030年までずっとトップラインを6%成長という高いレベルで維持するための事業開発なのです。それでは、次の質問に移ります。
オペレーター
次の質問はシティのアンドリュー・バウムさんからです。
アンドリュー・ボーム — シティ — アナリスト
ありがとうございます。いくつか質問があります。まず、オミクロンの注射が1回ではなく、2回必要になるとのことですが、どのようにお考えですか?最近発表された動物モデルでは、1回のオミクロンmRNAワクチンで、先祖代々のスパイク変異体よりもオミクロンに対する中和抗体のレベルが低くなることが示唆されており、おそらく抗原性の罪に起因すると思われるからです。これは明らかに、2回接種という点での収益だけでなく、コンプライアンスにも影響を与えるものです。
次に、CD47の見通しについて、御社の分子とギリアドの分子との違いについてお聞かせください。ありがとうございました。
Albert Bourla — 会長兼最高経営責任者
そうですね、1つ目は私が手短にお話しして、2つ目はミカエルがお話しできるようにしたいと思います。結果を待つしかありません。しかし、すべてのmRNAワクチンが同じであるとは思いません。
ですから、ある取り組みの前臨床データを、他の取り組みの臨床結果に外挿するべきではないと思うのです。私たちは、1種類と2種類の両方をテストしています。かなり早い時期にハイブリッドワクチンをテストしています。しかし、これまで見てきたところでは、オミクロンに対する免疫原性は非常に強いと確信しています。
しかし、もちろん、これは前臨床試験に基づいています。この仮定を検証するためには、最初の臨床データを見るのを待つ必要があります。それでは、Mikael、Gileadについてはどうでしょうか?ところで、アンドリュー、あなたの期待についてはどうですかと言われました。私たちの期待は、1種類とか2種類とか5種類とかではなく、先ほど申し上げたように、先週コミルナティと契約を締結したものです。
ですから、これからサインするものは、これまで私たちが出したものに加えてのものになります。ミカエル、ギリアドについて。
Mikael Dolsten — ワールドワイド研究開発・メディカル担当プレジデント
そうですね。トリリウム社から私たちの製品に関心が寄せられたのは、そのユニークなデザインが引き金でした。マグロリマブとは対照的に、受容体融合ブロッカーと呼ばれるタンパク質で、現在、保留されています。ギリアド社の抗体は、標的への親和性が低く、特に高発現のがん細胞に集積し、赤血球への集積を抑えて貧血や溶血性貧血を引き起こさないようにすることが目的でした。
そして実際に、概念実証のための研究において、血液がんに対する単剤での活性が確認され、赤血球への影響は基本的に無視できるほど小さくなっています。つまり、これはうまくいっているのです。なぜマグロリマブが臨床保留になっているのかはわかりません。しかし、もちろん、私たちの分子が持っているこの分化は、これまで私たちの分子がうまくいっている理由の一例かもしれません。
私たちは当初、B細胞タイプのリンパ系悪性腫瘍に焦点を当てていますが、特に私たちのプロファイルが優れていれば、マグロリマブが使われてきた骨髄系領域、AMLやMDSにもますます興味を持つようになると考えていますし、そうした研究からの結果も待っているところです。ですから、私たちにとってTrilliumとの契約は、私たちが期待したものをすべて提供するものであり、よりユニークなプロファイルによって、実際にアップサイドをもたらす可能性があるのです。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
ミカエルさん、ありがとうございました。次の質問をお願いします。
オペレーター
次の質問はJPMorganのChris Schottからです。
Chris Schott — JPモルガン・チェース・アンド・カンパニー — アナリスト
こんにちは、素晴らしい。質問をありがとうございました。まず、ガイダンスについてお聞かせください。今年のコア事業とCOVID関連の収益について、あまり詳細を説明されていないようですが、この点については多くの疑問があります。
しかし、売上高の下限を450億ドルとして、40%のマージンを適用し、税金を調整すると、下限で1株あたり2.60ドルという数字になるのではないかと思っています。この計算で何か問題がありますか?それとも、今年のコアガイダンスの下限を考えるのであれば、私の計算は正しいのでしょうか?2つ目の質問はPaxlovidについてですが、ここで典型的な低分子化合物の粗利率について言及されていますね。この点について、もう少し詳しく説明してください。この製品の売上総利益率は、80%台半ばと考えるのが妥当でしょうか?それとももっと高いのでしょうか、あるいはもっと低いのでしょうか?今年度中に進むいくつかの契約や、パックスロビッドの数字が動くかもしれないことを考えると、収益性をよりよく理解したいのです。
それから、最後にもう1つ。BDのビジネスとアプローチについて、まだよく理解できていません。COVIDの上市前の2、3年前と比べ、現在のファイザーの事業開発に対するアプローチは大きく異なると考えるべきなのでしょうか。それとも、2019年を例にとって考えてみると、あなたが見ていたことに焦点を当てた継続になるのでしょうか?ありがとうございました。
Albert Bourla — 会長兼最高経営責任者
3つ目の質問は私が素早く行い、最初の2つの質問はフランクにお願いします。私は……継続と言いたいところですが、ペースはずっと加速しています。2019年以降、言っていることは変わっていないと思います。
Aamirが言ったように、私たちは科学に踏み込んでいます。正しいターゲットの選択で失敗が少ないと思われる分野に入っていきます。私たちはより成功しやすくなるので、少なくとも業界の成功率に見合うようになります。それを超えるのが目標です。
資産の選択にあたっては、付加価値をつけられるところに行きたいと考えています。そして、いくつかのバイオテクノロジー企業の優先的なパートナーとなることで、価値を付加することができる重要な分野があります。また、Aamirが言ったように、私たちが行った最高の取引の中には、最も資本集約的な取引ではないものもありましたね。だから、そういうことも含めて、私たちは学んでいるのです。しかし、この分野での活動をもっと強化するつもりです。
というのも、もちろん、今こそ科学は、付加価値や価値創造につながる十分なターゲットを見つけられる段階にあると思うからです。これがBDの側面です。さて、フランク、マージンやガイダンスなど、財務に関する質問がたくさんあります。
フランク・ダメリオ — 最高財務責任者(CFO
クリス、コミルナティとパックスロビドを除くビジネスについて、あなたが行ったウォークスルーの結果について教えてください。売上高については、中間値を使用したいと思います。税引前利益率は40%でしたね。
そして、その税効果です。税効果を考慮したとは聞いていません。つまり、計算をして、ウォークスルーをして、税効果を計算し、それを発行済株式数で割れば、だいたいの数字がわかると思うのです。パックスロビドの売上総利益率については、このように回答させていただきます。
1つは、製品別のマージン情報を提供していないためですね。いろいろな理由があって、やっていないことです。しかし、考え方としては、1つは、税引前利益率は、当社の他の経口固形製剤と同様のマージンプロファイルであるということです。また、売上総利益率を見ると、今年はパックスロビドを発売するため、SI&A投資が行われることを思い出してください。また、パックスロビドを発売するため、研究開発への追加投資もあります。
これらはすべて、他の経口固形製剤と同様に、この事業の税引前利益率に反映されることは明らかです。これはすべてガイダンスに織り込み済みです。この影響は、昨年度の売上高に占める売上原価の割合が37.7%であったことから、その影響を確認することができると思います。今年のガイダンスを見ると、32.2%から34.2%、中間値は33.2%で、中間値で4.5%減少していますが、そのほとんどは今年のパックスロビッドの売上によるものです。
これは、今年のパクスロビッドの売上に大きく影響されています。
アルバート・ブーラ — 会長兼最高経営責任者
ありがとうございます。次の質問をお願いします。
オペレーター
次の質問は、ゴールドマン・サックスのクリス・シブタニさんからです。
クリス・シブタニ — ゴールドマン・サックス — アナリスト
どうもありがとうございました。質問が2つあります。1つは、繰り返しになりますが、25年までの中間成長期待を支えるものについて、私が明確に理解しているかどうかを確認するためです。2019年に発表された当初は、25年までのCAGR6%を達成するために、事業開発からの貢献を想定していなかったと思います。
今もそうなのでしょうか?それが最初の質問となります。それから2つ目の質問は、パックスロビドに関連するものです。パックスロビドについては、標準リスク試験を拡大しました。アンジェラさんが各国政府と行っているような決定や議論に影響を与えるためには、どのような結果が必要なのか、お話しいただけますか?特に、主要評価項目である症状の緩和については、統計的有意差を逃しましたが、これを達成する必要があるのでしょうか?それとも、副次的評価項目である標準リスク試験での重症入院リスクの減少を達成できるかどうかが、議論の焦点になるのでしょうか?ありがとうございました。
Albert Bourla — 会長兼最高経営責任者
はい。そして、時間の都合上、両方受けられるかもしれません。6%というガイダンスは、BDを除いたものであることを確認できます。つまり、19年から25年まで、当時からCAGR6%ということです。
標準リスクの主要評価項目については、すべてとは言いませんが、ほとんどの国の政府が、入院を減らすことができるかどうかに、購入や議論の焦点を合わせていると思います。ところで、ほとんどの国、例えばFDAは、ワクチン接種と未接種をすでに承認していますが、これには、標準リスク集団に含まれる人々も含まれます。つまり、標準リスク集団に含まれる人々も含まれることになります。しかし、誰もが、入院を防ぐためにすべての人に接種するという前提で動いているのだと思います。
それが主な — 誰もが注目している主なことです。さて、社内契約ですが、これは非常に異なっています。そして、それは非常に大きな風景だと言えるでしょう。今はまだ、そのような話はしていません。
しかし、もし陽性となれば、ハイリスク集団の感染予防にも利用できます。家庭や老人ホーム、あるいはビジネスなど、人が一緒に暮らす環境で、誰かが感染してしまうのです。しかし、これは、もしポジティブな結果であれば、私たちが今行っている議論の上位に来るものです。次の質問へどうぞ。
オペレーター
次の質問は、みずほ証券のヴァミル・ディヴァンさんからです。
ヴァミル・ディヴァン — みずほ証券 — アナリスト
こんにちは、素晴らしい。質問をお受けしてありがとうございます。パックスロビドと事業開発について、同じテーマでお話したいと思います。まず、パクスロビドについてですが、私たちが同じページで始めているかどうか、念のため確認させてください。
現在のガイダンスには何回分の投与が含まれているのでしょうか?リリースでは、米国に2,000万回、英国に275万回とありましたが、明らかに他の契約も締結されています。そのため、今現在、どのようなものが含まれているのか、数字や範囲を教えていただけないでしょうか。それから、事業開発についてですが、スライド13の中で興味深いことが1つあります。
アルバートさんは、バランスとキャッシュフローの強さによって、2030年に少なくとも250億ドルのリスク調整後収益を追加できる新しいBDの機会を追求することができるとおっしゃっています。この250億ドルというのは、具体的な数字なのでしょうか?この250億ドルというのは、具体的な数字だと思うのですが、どうでしょうか。ですから、よく練られたものだと思います。
その理由は何なのでしょうか?もちろん、今後数年間の業績次第では、この数字はもっと小さくなる可能性もありますし、もっと大きくなる可能性もあります。なぜそのような表現にしたのか、その理由を教えてください。ありがとうございました。
アルバート・ブーラ — 会長兼最高経営責任者
250億ドルを選んだ理由 — 250億ドルについて話すということですね?
Vamil Divan — みずほ証券 — アナリスト
ええ、少なくとも250億ドルの調整後売上高と言っています。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
はい、わかりました。了解しました。フランク、パックスロビドと服用はどうするんだ?
フランク・ダメリオ — チーフ・ファイナンシャル・オフィサー
もちろんです。ヴァミル、パックスロビドのガイダンスについてですが、先ほどアンジェラも言っていましたが、私たちは今とてもアクティブで、さまざまな政府と100以上の交渉を行っています。私たちは、誤解を招くような仮定や、その仮定が契約交渉に不利になるような情報は出したくありません。しかし、今、あなたは、発表され公開された、線量情報が含まれるいくつかの契約について述べました。
アメリカは2,000万人、イギリスは275万人ということでしたね。私たちが公表したものをすべて合わせると、およそ3,000万回の治療となります。ですから、この3,000万件の治療は、220億ドルの売上として提示したガイダンスの中に明確に含まれています。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
ありがとうございます。そして、アミール、なぜ250億ドルを選択したのか?
Aamir Malik — エグゼクティブ・バイスプレジデント、チーフ・ビジネス・イノベーション・オフィサーです。
ヴァミール、2つほど考えを聞かせてください。ひとつは、バランスシートの強さとキャッシュフローのおかげで、かなりの資本を投下できることです。そして、配当の増加以上に、事業開発に投入されたキャッシュフローは魅力的なリターンをもたらすと考えています。
これが1つの要素です。もうひとつは、率直に言って、今がこの業界における科学的進歩の絶好の機会であると考えています。学術界、ベンチャー企業、バイオテクノロジー企業、大企業、中小企業を問わず、社内で行っていることを補完してくれる外部基盤には事欠きません。そして、私たちは、追求したい科学について、思慮深く、規律正しく行動するつもりです。
そして、この2つのことと、私たちが持つ能力を組み合わせることで、今後、事業開発を通じて当社のビジネスに大きな成長をもたらすことができると考えています。
アルバート・ブーラ — 会長兼最高経営責任者
そうですね。また、ヴァミール、私たちは、目標を立てると、目の前の目標を達成することができると信じていることを理解しておくことも非常に重要です。実際、私たちは上場企業ですから、目標を公開する必要があると考えていますし、公開することに問題はありません。そこで、また、基板と機会の分析に入りました。
なぜなら、いつも通り、私たちは目標を掲げて、それを達成することが好きだからです。しかし、私たちは現在の、つまり私たちが行った分析によれば、この目標は、たとえば今持っている火力をすべて使わなくても達成できる、非常に妥当な目標だと考えています。だから、配当や他の資本活用をしながらも、それを実現することができるのです。そして、私たちは自信を持ってこれを公表し、人々がこれと比較して測定を開始できるようにします。
ありがとうございました。次の質問は?
オペレーター
次の質問は、ベレンバーグのケリー・ホルフォードさんからです。
Kerry Holford — Berenberg — アナリスト
ありがとうございます。ではまず、経口GLP-1についてです。第2b相試験で、最大用量の1日2回、200mgまで使用する場合の1日あたりの錠剤数を確認できますでしょうか。最高用量での錠剤負担はどのくらいですか?また、肥満については、本日はお話がありませんでした。
第2相試験のデータは社内にあるのですか?もう1つの経口GLP-1分子を臨床に出したとおっしゃいましたが、これはどういうことですか?また、その薬剤が最初のダヌグリプロンとどのように違うのか、興味があるのですが。そして最後に、ガイダンスについてです。売上高ガイダンスの40億ドルの範囲についてですが、ワクチンと抗ウイルス剤に関する推定値が提示されていることから、残りのフレックスの大部分はベースビジネスに関連していると考えてよいのでしょうか?また、その場合、その事業における主要な可動部分を理解するのに役立ちますか?そのフレックスの原動力となりそうなのはどの薬剤でしょうか?ありがとうございました。
アルバート・ブーラ — 会長兼最高経営責任者(CEO
ケリーさん、ありがとうございます。時間の都合上、最後の1つを非常に手短に説明させてください。いいえ、フレックスはすべてに広がっています。例えば、310億ドルのうち…330億ドルのうち、ワクチンで5億ドル、パックスロビドで10億ドル、5億ドル…ではなく、5億ドルと仮定すべきです。
もう10億ドルです。それから事業については、いつものように10億ドル、上下に振っています。つまり、中間値として10億ドルを上乗せしていますが、これはこのレベルのビジネスに対してこれまでずっと行ってきたことと同じです。それから、ミカエル、口頭での質問ですが、どうしますか?
ミカエル・ドルステン — ワールドワイド研究開発・メディカル担当社長
そうですね。ダヌグリプロンはBID薬であり、錠剤の負担は比較的少ないと思います。また、臨床開発中のGLP-1製剤の追加についてもご質問をいただきました。あれは1日1回投与の薬です。
経口GLP-1製剤の最適な滴定はどの程度になるのか、私たちが先駆的に定義してきたと思いますが、それに関するデータがありません。ダヌグリプロンと同じ試験で、1日1回投与にすることも考えています。しかし、今のところ、私たちがお伝えしたこの試験に基づいて、ダヌグリプロンは、ピボタル試験の可能性を進めるために必要なものをすべて持っていると信じています。もちろん、期待される結果が得られるまでは、第2b相試験終了後、速やかに第3相試験に移行するための最良の選択肢を与えてくれるものです。
Albert Bourla — 会長兼最高経営責任者
ミカエルさん、ありがとうございました。そして最後の質問をお願いします。
オペレーター
最後の質問は、バークレイズのカーター・グールドさんからです。
Carter Gould — バークレイズ — アナリスト
素晴らしい。おはようございます。質問をお受けしてありがとうございます。もう終わりなので、1つだけにしておきます。
回答が得られないかもしれませんが、パックスロビドのOUS価格について、GDPと数量ベースの割引の間で価格戦略のようなものを推進している基本的な側面があると理解しています。しかし、実際のところ、地域間で価格設定はどの程度一致しているのでしょうか。どのようなレベルでもいいので、教えていただければと思います。また、スタンダードリスクデータやプロフィーのデータが年内に出てくる可能性がありますが、上期と比較して下期の価格設定は比較的一定になると予想されますか。何かご教示いただければ幸いです。ありがとうございます。
Albert Bourla — 会長兼最高経営責任者
パックスロビドの価格設定は、ティアプライシングです。つまり、高所得国向けの階層があり、それは、たとえばメルク社の製品について公表されているものとほぼ同じであり、私たち自身も公表されているものを見ています。唯一の例外はアメリカで、注文が多かったので特別な価格になっていますが、他はほぼ同じです。それから、もちろん、中所得国には第2層があります。
そして、低所得国にはコストで提供することにしています。低所得国に対しては、私たちがコストで提供するだけでなく、もちろん、非常に多くのジェネリック企業が低所得国向けに製造を開始するプロセスを開始しました。さて、もし価格が一定に保たれるのであれば、明らかに、ここでコメントするようなことではありません。私たちは、価格が将来どのように変化するか、あるいは変化しないかについて、コメントするつもりはありません。
ありがとうございました。それでは、最後に簡単にコメントをさせていただきます。もちろん、ペースとインパクト、そして財務の両面で強力な結果を生み出しており、2022年もそれを継続することを楽しみにしています。私たちが行っている人の変化について少しお話したいと思います。
それについて言えば、私たちは、患者さんのために画期的な結果を出してきた実績を持つ、先見性と目的意識の高いリーダーを引き寄せ続けています。その一例として、先週、ウィリアム・パオ博士が今年3月21日付でファイザーに入社し、執行副社長兼最高開発責任者に就任することを発表しました。Dr.
パオ博士は、腫瘍学者および科学者として25年以上の経験を有しています。彼はロシュから入社し、直近では医薬品研究および早期開発の責任者を務めていました。彼は、がん、神経科学、眼科、希少疾病に関連する疾患を治療するための新しい分子実体のポートフォリオの発見と早期開発を監督していましたので、この話は尽きません。もちろん、がんは彼のポートフォリオの中で非常に大きな位置を占めています。
パオ博士は、ファイザーの伝説的なリーダーであるロッド・マッケンジーの後任ですが、彼は最近、ファイザーに35年間勤務した後、引退する意向を表明しています。私は、ComirnatyとPaxlovidをこれほど早く世に送り出した卓越したリーダーシップを含め、ファイザーに対するロッドの素晴らしい貢献に感謝したいと思います。もちろん、また、誰もが心に留めていることに触れる必要があります。
私の信頼する同僚であり友人であるフランク・ダメリオが、CFOとして10年半の間ファイザーに多大な影響を与えた後、ファイザーを退職する意向を表明したことを、この場をお借りしてお伝えしたいと思います。フランクは、私がこれまで幸運にも一緒に仕事をした中で、最も賢く、尊敬され、最も効果的なリーダーの一人であり、彼がファイザーと当社のすべての関係者に及ぼしたプラスの影響は計り知れません。フランクは、私たちが後任者を探す間も役員として留まり、移行期間中はコンサルティングの役割も果たすことに同意していますので、はっきりさせておきますが、まだどこにも行かないということではありません。とはいえ、この場を借りて、ファイザーと私個人にとって重要な存在であった彼に、公式に感謝の意を表したいと思います。
そしてフランク、世界中の8万人の同僚を代表して、あなたの健康と、新しい章を始めるに当たってのあらゆる幸福を祈ります。人生の旅路がどこに行こうとも、それはきっと正しい方向であると信じています。では、これで電話を終わります。ご出席いただきありがとうございました。
素晴らしい一日をお過ごしください。
以上です。他の翻訳希望があればご連絡いただければ検討いたします。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>


