モデルナ (MRNA)2022年第3四半期決算説明会の日本語訳です。
ワクチン頼みのモデルナの決算ですがアフターコロナになってきているので流石に厳しいですね。コロナワクチン以外の製品がないと厳しいので今買っていくには難しいです。中国のワクチン購入が決まれば再度株価は暴騰すると思いますがしばらくはなさそうです。
技術力はあるので今後の開発品次第では化けると思うのでパイプラインに注目して追っていきたいと思ってます。
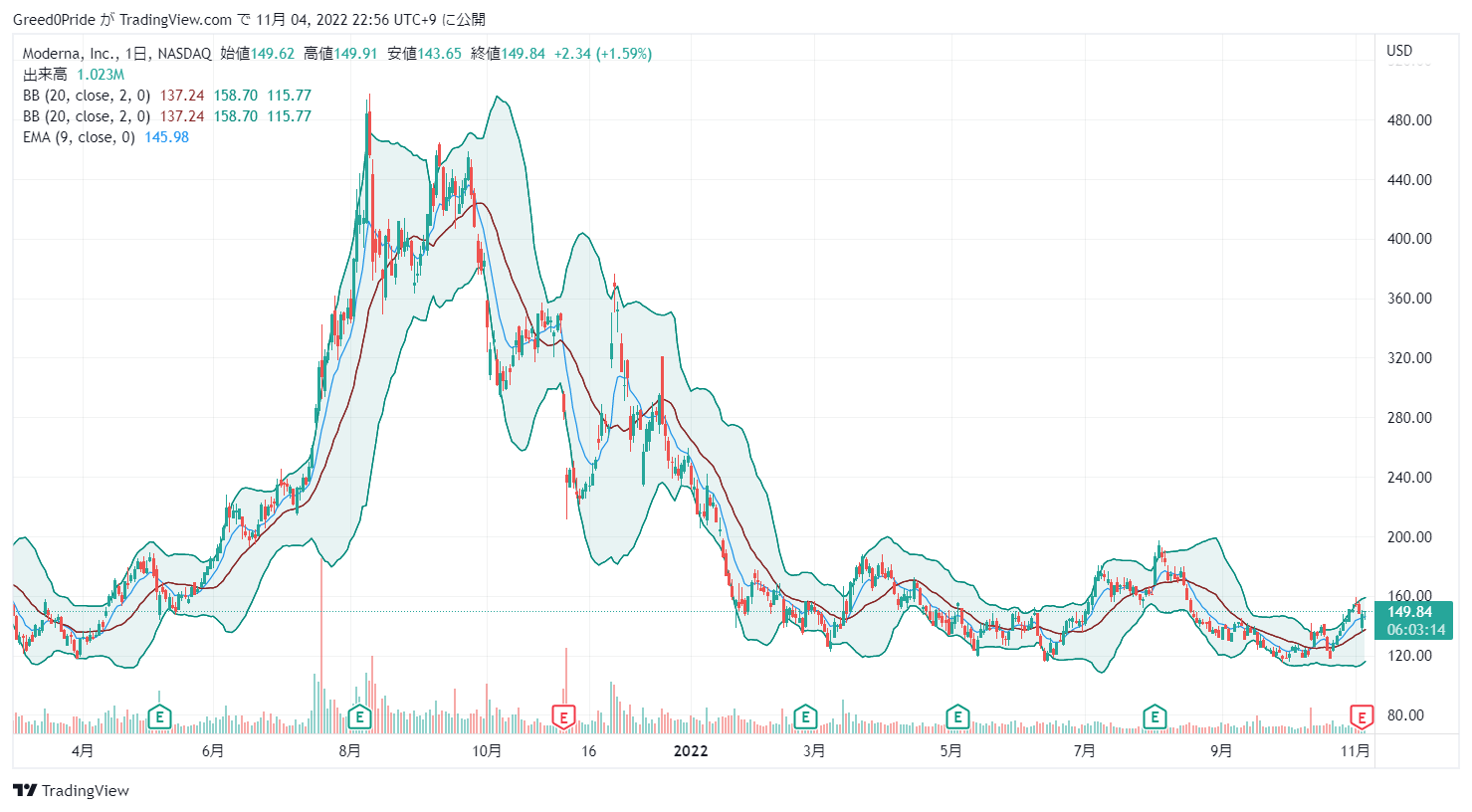
モデルナ (MRNA)株価
前回の2022年第2四半期決算説明会はこちらです。
モデルナ (MRNA)2022年第3四半期決算説明会
Call participants:
Lavina Talukdar — Head of Investor Relations
Stéphane Bancel — Chief Executive Officer
Stephen Hoge — President
Arpa Garay — Chief Commercial Officer
Jamie Mock — Chief Financial Officer
Salveen Richter — Goldman Sachs — Analyst
Matthew Harrison — Morgan Stanley — Analyst
Edward Tenthoff — Piper Sandler — Analyst
Michael Yee — Jefferies — Analyst
Gena Wang — Barclays — Analyst
Tara Bancroft — Cowen and Company — Analyst
Jessica Fye — JPMorgan Chase and Company — Analyst
Geoffrey Meacham — Bank of America Merrill Lynch — Analyst
Eliana Merle — UBS — Analyst
Joseph Stringer — Needham and Company — Analyst
Lili Nsongo — SVB Securities — Analyst
More MRNA analysis
2022年11月03日 午前8時00分
オペレーター
おはようございます。モデナの2022年第3四半期決算説明会にようこそ。[オペレーターの指示】この通話は録音されていますので、ご了承ください。この時点で、モデナのIR担当のラヴィナ・タラクダー(Lavina Talukdar)に通話を引き継ぎたいと思います。
どうぞ続けてください。
Lavina Talukdar — 投資家向け広報の責任者
ありがとうございます、ケビン。皆さん、おはようございます。本日は、Modernaの2022年第3四半期決算とビジネスアップデートについて、お電話にお付き合いいただきありがとうございます。今朝発表したプレスリリースと、これからご覧いただくスライドは、当社ウェブサイトの投資家情報セクションからアクセスできます。本日の電話会議には、最高経営責任者のステファン・バンセル、社長のスティーブン・ホーグ、最高商業責任者のアルパ・ガレイ、最高財務責任者のジェイミー・モックが出席しています。
ご挨拶の後、午前9時15分までご質問をお受けします。この電話会議では、1995年米国民事証券訴訟改革法のセーフハーバー規定に基づく将来見通しに関する記述も含まれていますことをご承知おきください。当社の実際の業績や結果が、これらの将来見通しに関する記述で明示または黙示されたものと大きく異なる原因となりうる重要なリスク要因については、添付のプレゼンテーションのスライド2および当社のSEC提出書類をご覧ください。
ステファン・バンセル — 最高経営責任者
ラヴィーナ、ありがとうございます。皆さん、おはようございます、こんにちは。2022年第3四半期のカンファレンス・コールへようこそ。本日は、ステファンが臨床プログラムをレビューする前に、まず私が四半期の簡単なビジネスレビューから始めます。
その後、アルパがコマーシャル・ダイナミクスについて説明し、ジェイミーが財務を説明します。その後、質問をお受けする前に、いったん終了とさせていただきます。当四半期の売上は34億ドルでした。当期純利益は10億ドル、現金投資額は170億ドルでした。
2022年には、充填・仕上げ加工メーカーからの納入が遅れるため、先行購入契約に基づく納入額を180億ドルから190億ドルの範囲で見込んでおり、2023年には20億ドルから30億ドルの収益の繰り延べが発生する見込みです。第3四半期は、1273.214と1273.222の2製品を同時に上市し、さらに製品を10回分バイアルから5回分バイアルに移行するという複雑な状況に対処しなければなりませんでした。第3四半期は、バイアル生産量において、実際に当社の納品量が多く、過去3四半期の平均値である約20%増となりました。2023年については、アルパがもう少し詳しくご説明します。
第3四半期は、700万株超の自社株買いを行いました。2022年2月に発表した30億ドルの自社株買いプログラムは完了しました。2021年の最初の自社株買いプログラムの開始から第3四半期末までの間に、2300万株以上の自社株買いを行いました。2022年8月に発表した30億ドルの追加取得を目的とした最初の自社株買いプログラムは継続中です。
それでは、前回の更新以降のパイプラインのハイライトと進歩についてご説明します。私は、パイプラインを製品上市に近づけ、同時にパイプラインの幅を広げるために、モデナチームが重要な進展を遂げたことを非常に嬉しく思っています。COVIDブースタープログラムも引き続き進めており、オミクロンBA.1をターゲットとするCOVID 1273.214プログラムとBA.4/5をターゲットとする1273.222プログラムの両方について世界中で認可を取得しました。また、ご存知のように、現在、2つの呼吸器系ワクチンが第3相試験段階にあり、順調に進行しています。
インフルエンザワクチンについては、9月のR&Dで、最初の第3相免疫原性試験の登録が完了したことを発表しました。2023年の第1四半期にデータが出る予定です。なお、季節性インフルエンザワクチンについては、加速承認経路を追求する予定です。また、インフルエンザワクチンの第3相有効性試験を開始し、この試験には迅速に登録が行われています。
アレルギー用ワクチンの第3相試験については、今冬のデータ読み出しに向けて順調に進んでいます。メルク社は、当社の個人用がんワクチン mRNA-4157 の開発・商業化オプションを行使し、第 4 四半期に 2 億 5,000 万ドル以上を支払ったと発表したことを嬉しく思っています。当社とメルク社は、今後このプログラムについて費用と利益を折半することになります。PCV の第 2 相試験のデータは、引き続き本年第 4 四半期に得られる見込みです。
希少疾患に関しては、R&D Dayにおいて、PAとGSD1aの両方から有望な臨床効果の初期兆候が見られたこと、またOTCの新しい開発候補品を発表したことをお知らせします。スライド6には、2022年11月のモデナのスナップショットが掲載されており、ワクチンや治療薬など、現在48のプログラムが開発中で、パイプラインの幅広さを示しています。会社は成長を続けており、現在、Modernaのチームメンバーは3,700人を超えています。先週は、8年連続で科学分野のトップ・エンプロイヤーに選ばれたことを大変嬉しく思っています。
現在、世界各地に15の販売子会社を持ち、170億ドルという強固なバランスシートをもって、継続的な成長に向けた資金を確保しています。それでは、パイプラインのレビューについて、スティーブンに話を譲りたいと思います。スティーブン?
スティーブン・ホーグ — 社長
ステファン、ありがとうございます。皆さん、おはようございます。今朝は、私たちの臨床の進捗状況についてお話します。私たちは、市場のさまざまな需要に対応するため、現在の秋冬シーズン向けに2種類のワクチンブースターを発売し、これらのワクチンについて世界中で承認または認可を取得しました。
オミクロンBA.1を標的とする1273.214は、臨床試験においてBA.1およびBA.4/5サブラインに対して1273よりも有意に高い力価を誘導したことを以前お伝えしましたが、このたび、1273.214のmRNAが、BA.1サブラインに対して有意に高い力価を誘導したことを確認しました。そして、mRNA-1273.214は、英国、スイス、カナダ、オーストラリア、欧州連合、日本、その他の国々で承認されています。オミクロンBA.4/5亜型をターゲットとするmRNA-1273.222については、第2/3相試験が進行中で、今期末にはデータが得られる見込みです。MRNA-1273.222は、米国をはじめ、英国、スイス、オーストラリア、カナダ、欧州連合、日本、その他の国々で承認されています。
それでは、スライド9に移ります。呼吸器系ワクチンのパイプラインをレビューします。次のスライドでは、第3相試験について詳しくご説明します。ここでは、呼吸器系ワクチンの初期段階の試験の進捗を強調したいと思います。
季節性インフルエンザを対象としたMRNA-1020、10.30は、現在、第1/2相試験を実施中で、完全に登録が完了しています。小児RSVを対象とするmRNA1345は、現在、第1相試験の登録が完了しています。次に、呼吸器系の混合ワクチンのパイプラインについてですが、ここでは重要な進展がありました。COVIDとインフルエンザの混合ワクチンであるmRNA-1073は、第1/2相試験を実施中で、現在、完全に登録されています。コビド、インフルエンザ、RSVの混合ワクチンであるmRNA-1230も、フェーズ1/2の試験で登録を開始したことを大変嬉しく思います。
新しい開発候補としてmRNA-1045を発表しましたが、これはRSVとインフルエンザの混合ワクチンを対象としたもので、フェーズ1/2の試験が開始されました。最後に、混合ワクチンのパイプラインとして、hMPVとPIV3を対象とした小児用ワクチンもあり、こちらは完全に登録されたフェーズ1/2の試験が進行中です。最後に、風土病のヒトコロナウイルスワクチン、そして小児用のRSVとHMPVの混合ワクチンが前臨床開発中です。次に、スライド10にある第3相のインフルエンザとRSVのプログラムについて説明します。
インフルエンザについては、南半球での第3相免疫原性試験は、6,000人の参加者が完全に登録されており、データの読み出しは2023年の第1四半期に予定されています。すでに述べたように、規制当局は、この試験の結果を待って、当社の季節性インフルエンザワクチン候補の早期承認経路を支持する意向を示しています。また、北半球での第3相有効性試験の登録も開始し、現在10,000人以上の参加者を登録しています。この第3相有効性確認試験のタイミングは、この試験におけるインフルエンザ患者数の増加によって決定され、早ければ今年の冬に実施される可能性があります。
RSVに目を向けると。高齢者を対象とした当社の主要な第3相有効性試験には、現在35,000人以上の参加者が登録されています。先に述べたように、この試験の主要評価項目は、安全性とワクチンの有効性です。第3相有効性試験の結果は、この試験におけるRSV症例の発生状況によって決定されます。
現在、非常に好調なRSVシーズンの真っ只中にあるため、この冬のシーズンには結果が得られると引き続き期待しています。次に、潜伏感染症および公衆衛生ワクチンのポートフォリオについて説明します。CMVワクチンは第3相試験を実施中です。伝染性単核球症を予防するEBVワクチンは第1相試験を実施中で、がんや多発性硬化症など長期的な後遺症を予防するEBVワクチンは前臨床試験中です。
また、HIVワクチンも2つのフェーズ1試験が進行中であり、HSVワクチンとVZVワクチンも前臨床試験が進行中です。最後に、ジカ熱に対する公衆衛生ワクチンは第2相試験が進行中で、ニパワクチンは第1相試験が進行中です。それでは、スライド12にある治療薬パイプラインを見てみましょう。まず、アストラゼネカ社から、ポートフォリオレビューの結果、IL-12プログラムの権利を当社に返還するとの通知があったことを記しておきたいと思います。
彼らは第1相試験を終了させ、その後、私たち自身でこのプログラムの次のステップを評価することになります。次に、チェックポイント・ワクチンが第1相試験で最初の患者への投与を開始したことに興奮しています。そして最後に、パートナーであるバーテックス社は、当社のmRNA嚢胞性線維症プログラムのINDを今年末までに提出する予定です。私たちは、最新のR&Dデーで、個別化がんワクチン、PA、GSD1aプログラムの最新情報を共有しましたので、次のスライドでより詳しくお話したいと思います。
さて、R&D Dayでは、2つの希少疾患プログラムのデータを共有したことを思い出してください。1つ目は、プロピオン酸血症プログラムで、複数回投与試験です。9月の時点で、6年間の投与経験があり、投与回数も100回をはるかに超えています。概ね良好な忍容性を示しており、心強い限りです。
また、プロピオン酸血症患者における代謝異常の重症度を考慮すると、代謝異常の発生頻度が数値的に減少していることは、非常に心強いことです。GSD1aプログラムでは、最初のコホートにおける最初の2人の患者さんからの初期のデータを共有しました。この試験は、低血糖に陥ることなく長期間にわたって絶食または無食を続けることができないGSD1aの患者さんを対象に、コントロールされた安全な環境で絶食チャレンジを行う単回昇順投与試験です。最初のコホートの患者さんは2人とも、mRNA-3745の忍容性が高く、絶食時間の延長とグルコースを含む主要バイオマーカーの正常化を示しましたが、これは非常に有望な活性のシグナルだと考えています。
最後に、個別化がん治療薬の第2相試験の結果が年内に出る予定であることを、皆さんにお知らせしたいと思います。PCV+KEYTRUDAとKEYTRUDA単独を比較する無作為化試験には、再発リスクの高い切除されたメラノーマ患者約150人が登録されました。主要評価項目は、無再発生存率です。先ほどStephaneが述べたように、パートナーのメルク社は、mRNA-4157を共同で開発・商業化するオプションを行使しており、今期中にそのデータを共有することを楽しみにしています。
それでは、Arpaにバトンタッチします。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
スティーブンさん、ありがとうございます。まず、スライド16の売上高のレビューから始めます。第3四半期の米国向け売上は10億ドルで、主にオミクロンBA.4/5をターゲットとした二価ブースター、mRNA-1273.222の納入によるものです。mRNA-1273.214の欧州向け売上も10億ドル、その他の地域は11億ドルでした。
第1~3四半期までの売上は、米国が34億ドル、欧州が45億ドル、それ以外の地域が57億ドルでした。当年度第3四半期および9ヵ月間において、これら主要地域間での売上高の地理的な分散が見ら れました。2023年の市場や長期的なコビドブースターの可能性について疑問があると思いますので、私たちがどのように考えているかを説明したいと思います。私たちが流行市場に移行する際、商業的な見通しにおいて考慮した重要な要因があります。
それは、コビドブースターの継続的な医療ニーズと、毎年のブースター市場の潜在的な大きさです。次のスライドでは、季節性インフルエンザの市場について、私たちの考えを説明します。また、2023年の米国での市販市場への移行の基礎となるいくつかの要因についても詳しく説明します。次に、COVIDのセクションで、現在締結している契約の概要と、2023年に予定されている追加契約の見通しについて説明します。
最後に、9月に開催されたR&D Dayで発表した、2023年に上市予定の呼吸器系ワクチン・フランチャイズの概要と、上市時期についてお知らせします。COVIDブースターの医療上の必要性から始めると、スライド18のチャートは、季節性インフルエンザとCOVIDに関連する入院と死亡を関連する期間にわたって比較したものです。インフルエンザについては、COVIDに関連する介入によって典型的なインフルエンザシーズンが混乱する前に、米国における過去10シーズンのインフルエンザを振り返りました。そしてCOVIDについては、SARS-CoV-2およびその亜種に対してワクチン接種または感染による免疫が広まる期間をカバーする、2021年10月から2022年9月の入院と死亡を調べました。
この期間は、流行期にCOVIDに対する集団の免疫がどの程度になるかを示す近似値であると考えています。このグラフにあるように、過去12ヶ月間のCOVIDによる入院は、分析に含まれる10年間の中で最も医療負担が大きかった年を表す2017、2018年のインフルエンザシーズンよりも3倍高い数値となっています。そして、COVIDによる死亡はさらに高く、同じ重症のインフルエンザシーズンの7倍の割合で入っています。このように、より流行期に近いと思われる時期にCOVIDの医療負荷が高いことがわかり、流行期におけるブースターの必要性が強調されました。
また、次のスライドでご紹介するCOVIDの潜在的な年間流行市場の規模を把握するのに役立ちます。COVIDブースター市場の規模を把握するために、まずインフルエンザ市場の数量から見ていきます。インフルエンザの年間市場規模は、全世界でおよそ5億〜6億回分です。市場規模は、スライド左側の感度表に示すように、投与回数と世界価格に大きく依存します。
ここに示した価格は、グローバル価格に関する結果の範囲を示すための純粋な例示に過ぎません。最終的には、コビドブースターのグローバル価格は、販売構成と市場間の価格差を反映したものになります。当社のエンデミック価格は、このワクチンが世界中の医療システムにもたらす価値に焦点を当てたものとなります。2023年に流行市場に移行するにあたり、この年の当社の数量に影響を与える主な要因としては、医療ニーズ、進行中のウイルスの進化、公衆衛生当局からの勧告、消費者のワクチン接種への動機付けなどが挙げられます。
そのため、コビド世界流行市場の数量は、時間とともに少なくとも6億回に近似すると考えていますが、2023年の数量に影響を与える変数を確実に予測するのは時期尚早であると考えています。スライド20「米国における商業市場への移行」については、民間支払機関、医療保険制度、薬局チェーン、個人薬局、医院など、顧客基盤がより細分化されることが予想されます。また、受注の予測可能性の低下、インフルエンザワクチンと同様の配送の季節性、Modernaが負担する流通コストへの移行、さらに、米国では、単回投与への移行、技術革新と製品の差別化の継続などの大きな要因も想定しています。スライド21に移り、これまでに締結した2023年の契約についてまとめています。
イギリス、カナダ、スイス、台湾、クウェートで、総額25億ドルの先行購入契約を締結しました。さらに、2022年からは20億ドルから30億ドルの繰り延べを見込んでいます。これらの繰延は、スライドに記載した国々からのものです。これらの先行購入契約と延期を合わせると、2023年の売上高は45億ドルから55億ドルとなります。
最後に、非常に重要なことですが、2023年の契約が追加で締結される見込みの国がいくつかあります。米国、EU、日本、オーストラリア、アジア、中南米、コバックスで23件の受注を確保するために取り組んでいます。そして、今期後半から来年にかけて契約シーズンが始まるので、これらの受注を見通すことができるようになると考えています。スライド22のCOVIDの見通しを要約すると、COVIDはインフルエンザに比べて医療負担が大きいため、COVIDの風土病ワクチン市場は長期的にはインフルエンザ市場と同等かそれ以上の規模になる可能性があると予想しています。
米国市場は商業市場へと移行しつつあり、当社はその進化するニーズに応えることができる立場にあると確信しています。最後に、当社は2023年に45億ドルから55億ドルの確定契約の基盤を確立しており、これに米国、EU、日本などの主要市場から今後数カ月で重要な受注を追加することを見込んでいます。さて、最後に、9月のR&D Dayで強調した呼吸器系ワクチン・フランチャイズの形成について、ご説明します。早ければ来年には、インフルエンザとRSVに進出する可能性があります。
インフルエンザとRSVは、COVIDと合わせて考えると、先進国市場ではアルツハイマー病、脳卒中、糖尿病よりも年間死亡者数が多い疾患です。Stephenが強調したように、症例集積とワクチンの有効性次第では、今年の冬にインフルエンザとRSVの第3相試験のデータが出る可能性があります。私たちは、これらの呼吸器系ワクチンの上市に向けて積極的に準備を進めており、現在構築中のCOVIDのコマーシャル・インフラを活用していく予定です。それでは、ジェイミーにバトンタッチしたいと思います。
ジェイミー・モック — 最高財務責任者
アルパさん、ありがとうございます。本日、皆さんとご一緒できることを嬉しく思います。モデナに入社して2カ月が経ち、私は会社の将来と、新世代の医薬品を患者さんに届けるという当社の役割に、さらに大きな期待を抱いています。まだお会いしたことのない皆さんとは、これから何ヶ月、何年と一緒に仕事ができることを楽しみにしています。
本日は、まず第3四半期の業績と資本配分の優先順位についてご説明し、最後に2022年の残り少ない業績に関する主要なドライバーについての見解を述べさせていただきたいと思います。次に、スライド 25 をご覧ください。当四半期の製品売上高は、前年同期比35%減少し、31億ドルとなりました。この減少は、COVID-19ブースターワクチンの市場認可のタイミングと、それに関連するCMOパートナーとの製造の立ち上げによる販売量の減少に起因しています。
なお、米国では8月31日に、EUでは9月2日に、日本では9月12日にそれぞれ販売許可を取得しています。2022年第4四半期は、ブースターワクチンの供給契約に対する納入を継続するため、製品売上は第3四半期よりも高くなると予想しています。売上原価は、製品売上高の35%(前年は15%)でした。これには、過剰で陳腐化したCOVID-19製品に関連する在庫評価損3億3,300万ドル、未使用の製造能力に関する費用2億900万ドル、確定購入契約に関する損失および関連するキャンセル料1億200万ドルが含まれます。
これらの費用は、オミクロンをターゲットとするCOVID-19二価ブースターへの製品需要のシフトおよび余剰生産能力に関連する費用に起因するものです。研究開発費は、前年度比 57%増の 8 億 2,000 万ドルとなりました。研究開発費の増加は、RSV、インフルエンザ、CMV、COVIDブースターの第3相試験など、当社のパイプラインが増加・成熟していることに引き続き起因しています。販売費および一般管理費は、前年同期比65%増の2億7,800万ドルとなりました。
支出の増加は、商業的および会社全体の構築の加速を支援するために、人材および外部サービスへの投資を継続したことによるものです。実効税率は前年の6%に対し、14%となりました。なお、2020年末に23億ドルの繰越欠損金があり、2021年の報告税率に非経常的なベネフィットが発生しました。税引き後純利益は 69%減の 10 億ドルとなりました。
2022 年第 3 四半期の希薄化後 EPS は 67%減の 2.53 ドルとなりました。自社株買い活動の結果、2022年第3四半期末の希薄化後加重平均株式数は、前年の4億3400万株から2200万株減少し、4億1200万株となりました。次に、スライド 26 の累計業績について説明します。2022 年 1~9 月期の製品売上高は 136 億ドルで、前年同期比 26%増となりました。
この増加は、主に顧客ミックスが良好であったこと、及び2021年上半期と比較して2022年上半期の顧客需要に対応するための製造能力が高まったことに起因しています。売上原価は、製品売上高の 26%(前年同期は 16%)でした。これは、第2四半期の決算説明会で述べたとおり、コバックスからの大幅な需要減、オミクロンをターゲットとしたCOVID-19二価ブースターへの需要シフト、余剰生産能力に伴うコスト増によるものです。税引後当期純利益は、前年同期比6%減の69億ドルとなりました。
純利益の減少は、主に、売上原価の増加、その他の営業費用の増加、税率の上昇によるものです。希薄化後1株当り当期純利益は、3%減少し、16.46ドルとなりました。スライド 27 の現金・預金に目を向けます。第2四半期末の181億ドルに対し、第3四半期末は170億ドルの現金及び投資残高となりました。
この減少は、第3四半期に実施した自社株買い10億ドル及び連邦税の支払い8億ドルを反映してい ます。また、当四半期末の将来の製品供給に関する預金残高は38億ドルとなりました。次に、スライド28をご覧ください。当社の資本配分の優先順位に変更はありません。
これまでも、そしてこれからも、複数の分野にわたる基盤事業への再投資を最優先します。研究開発費は、9月までの累計で21億ドルとなり、前年同期比で55%の増加となりました。mRNAプラットフォームには引き続き大きな期待を寄せており、現在進行中の複数の試験が第3相に移行し、48の開発プログラムを持っています。製造拠点の拡充に伴い、資本支出は前年同期比88%増の3億800万ドルとなりました。
また、コマーシャルやデジタル機能、会社全体の構築にも継続して投資しています。第二の投資優先課題は、Modernaの技術や能力をさらに拡大するために、魅力的な外部投資や提携の機会を模索することです。私たちは、当社のプラットフォームを実現・補完する魅力的な機会を検討し、外部投資の可能性を評価する上で、規律あるアプローチを取っています。当社は、追加の外部提携の機会について複数の活発な議論を進めています。
そして、社内外の投資機会を評価した後、次に現金の追加的な使途を評価します。2022年第3四半期には、10億ドルで700万株を買い戻しました。9月30日までの累計では、2,000万株、29億ドルの買戻しを行いました。10月には、2022年2月に承認された30億ドルのオーソライズを完了し、8月の追加オーソライズ30億ドルの活用を開始しました。
次に、スライド29にある2022年の最新の財務フレームワークについて説明します。短期的なサプライチェーンの制約により、20億ドルから30億ドルを2023年に繰り延べ、2022年に180億ドルから190億ドルの事前購入契約に基づく納入を見込んでいます。この合計額には、契約時の為替レートに対するマイナスの影響が含まれており、現在の為替レートが年末まで続くと仮定すると、2022年通年で売上高の約1.5%になると見積もっています。当社の総売上原価には、製造原価、他社からのロイヤルティ、物流・倉庫費などが含まれています。
2022 年通期の売上原価は、前述の通り、累計で発生した費用、第4四半期の販売台数の範囲、及び製品更新に伴う追加費用 の可能性により、26-28%の範囲となる見込みです。研究開発費及び販売費・一般管理費については、当社の成熟した開発ポートフォリオとグローバルなスケールアップに より、通期で約 40 億ドルの費用を引き続き見込んでいます。現行の税法にもとづくと、国際的な事業構成に起因する海外由来の無形固定資産利益や株式報酬控除によるメリットにより、2022年の実効税率は引き続き10%台前半から半ばになるものと見込んでいます。最後に、資本支出についてですが、プロジェクトの完了時期を考慮し、従来の6億ドルから8億ド ルを若干下回る5億ドル程度となる見込みです。
以上で決算に関する私の発言を終え、ステファンに電話を戻します。
Stéphane Bancel — CEO(最高経営責任者
ジェイミー、アルパ、スティーブン、最新情報をありがとうございます。質疑応答の前に、今年を締めくくり、2023年に向けての主要な優先事項を確認したいと思います。今年も引き続き、オミクロンブースターのアップデートを行い、2022年の販売を促進することに注力します。すでにヨーロッパ、日本、アメリカでの2023年の販売契約について、世界中の遠くから取り組んでいます。
アルパと私たちのチームは、2023年に米国市場で非公開にできるよう、米国チームとのセットアップやスケールアップも行っています。私たちは、パイプラインの実行を続けています。年内に予定されているPCVの第2相データを、手に入れたら発表できることを楽しみにしています。インフルエンザやRSV、CMVの第3相試験の登録を続けるために、チームは素晴らしい仕事をしてくれましたし、希少疾患プログラムの進展に期待しています。
来年に向けて、アルパとチーム、そして製造を含む組織全体が、商業用COVID市場を含む年内の複数のワクチン上市に備えるとともに、当社の治療プログラムが第3相で非常に迅速に進展する可能性も秘めています。最後に、来週11月10日に開催される当社初のESGデーに、多くの皆様がご参加いただけることを願っています。バーチャルイベントは、当社のウェブキャストからご覧いただけます。これをもって、ご質問をお受けしたいと思います。
運営者ですか?
質疑応答
オペレーター
[最初の質問はゴールドマン・サックスのサルヴィーン・リクターからです。お待たせしました。サルヴィーン・リヒター — ゴールドマン・サックス — アナリスト
おはようございます。私の質問に答えてくれてありがとうございます。COVIDワクチンの価格についてですが、ファイザーは民間市場での価格を110から130にするよう案内しています。これは、これまでの議論と一致していますか?また、民間市場は来年いつ頃出てくるとお考えでしょうか。それから、2つ目の質問です。
先ほど、来年のコスト負担について、流通コストやインフルエンザ、RSV、臨床試験に関する商業インフラの構築についてお話がありました。今後のOPEXの状況について、方向性を教えてください。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
それでは、価格に関する質問をお受けします。まず、競合他社の価格設定についてコメントできる立場にはありません。しかし、パンデミックからエンデミックに移行する際の価格設定について考えるとき、私たちの真の焦点は、医療システムに提供する価値に基づいてワクチンの価格を設定し、世界中の公衆衛生当局が設定する費用対効果のガイドラインを反映させることです。米国では、ACIPがそれにあたります。
過去に発表された価格設定のガイダンスの中には、グロス(総額)レベルのものもあり、さまざまなチャネルで多少のディスカウントが予想されることは重要な点だと考えています。さらに、米国では、商業ベースに移行する際、ACIPが推奨するすべてのワクチンについて、消費者の自己負担がゼロであることも忘れてはなりません。ですから、消費者アクセスの観点からは、価格設定が摂取の障壁になることはないと考えています。
ジェイミー・モック — 最高財務責任者
サルヴィーンさん、コストの部分についてお伺いします。そうですね、私たちのコストは風土病のように変化していくでしょう。まず、プレフィルドシリンジや単回投与バイアルへの移行が進みますので、前年比では変わると思います。また、二価ワクチンへの投資も継続しなければなりませんし、特に米国では、今後、流通コストをモデナが負担することになります。
ですから、コストプロファイルは変化し、それが何を意味するのかについては、後日、発表して更新します。
Salveen Richter — ゴールドマン・サックス — アナリスト
ありがとうございます。
オペレーター
[次の質問は、モルガン・スタンレーのマシュー・ハリソンさんからです。お待たせしました。Matthew Harrison — Morgan Stanley — アナリスト
素晴らしい おはようございます。質問を受けてくださってありがとうございます。PCVについてお聞きしたいのですが。
これは概念実証の第2相試験ですが、p値が0.05より大きければ、この試験の成功と見なすことができます。この試験の成功について、どのように考えているか、教えていただけますか?また、非盲検試験ということですが、社内で利用できるデータはどのくらいあるのでしょうか?
Stephen Hoge — 社長
Matthew、ご質問ありがとうございます。おっしゃるとおり、これは第2相試験ですが、実際にはかなり大規模なものです。150人の患者さんがいて、2対1に無作為化されているので、100人の患者さんが併用療法を受け、50人が標準治療(この場合はKEYTRUDA)を受けています。これはかなりのサンプル数で、有効性を見ることができます。
この試験は第2相試験です。統計的な閾値を事前に指定したわけではありませんが、ハザード比を調べており、p値を得ることができます。現時点では、特定のp値やハザード比についてコメントするつもりはありません。そうするのは時期尚早です。
しかし、明らかに、私たちは標準治療と比較して、その標準治療よりも有意に有益であることを実証するために、標準治療との比較を行っています。ただ、重要なのは、この試験は150人という参加者数ではそのための検出力がなかったということです。そのため、ハザード比とp値を指標とすることになります。そして、その結果の強さに応じて、実際、おっしゃるとおり、p値が0.05未満で、非常に強い結果が出た場合、その後の開発の進め方を決定することになります。
もちろん、ハザード比が高ければ高いほど、そしてp値が低ければ低いほど、私たちはそのプログラムを進めるために非常に迅速に行動するつもりです。
オペレーター
ありがとうございました。次の質問は、Piper SandlerのEdward Tenthoffからです。どうぞよろしくお願いします。
エドワード・テンスオフ — パイパー・サンドラー — アナリスト
素晴らしい。 ありがとうございます。そして、すべての進展におめでとうございます。そして、すべての進展におめでとうございます。COVID市場と今後の見通しについて、詳しく教えていただきありがとうございます。質問は、私の好きなテーマである希少疾病に戻ります。
最初のプログラムによる概念実証を手にして、COVIDによる概念実証の際にワクチンで行ったように、パイプラインを拡大する意向はあるのでしょうか?
スティーブン・ホーグ(Stephen Hoge)社長
エド、ご質問ありがとうございます。簡潔に言うと、「絶対」です。がんワクチン、感染症ワクチン、希少疾病ワクチンなど、どのような治療法であっても、技術的な概念実証を達成し、患者さんに対して行いたいことを実現できたと判断した場合には、その技術を応用できる病気や意味を急速に拡大することを検討しています。希少疾病の場合、先ほどもお話したように、2種類の薬剤を使用した2つの異なる疾病のデータから、私たちは非常に勇気づけられました。
しかし、それ以上に重要なのは、有効性に関して、バイオマーカーやダイナミックリードアウトの観点からも、患者さんにとって有益となり得る、本当に心強い結果が出始めていることです。そこで、この2つの結果を受けて、私たちはパイプラインの拡充を急いでいます。すでに公表され、臨床試験を進めているプログラムが多数あり、M&Aを含め、すでに臨床試験を開始しているものもあります。R&Dデーでお話ししたように、私たちはこのパイプラインを大幅に拡大することを検討しています。
その一例として、ちょうど1カ月前にOTCプログラムを発表しました。しかし、このパイプラインはさらに大幅に拡充されるものと期待してください。私たちの目標は、リスク軽減された臨床データを背景に希少疾患への投資を拡大し、今後数年間でパイプラインを2倍以上にすることです。
Edward Tenthoff — Piper Sandler — アナリスト
素晴らしい。ありがとうございます。
オペレーター
次の質問は、ジェフリーズのマイケル・イーからです。どうぞよろしくお願いします。
Michael Yee — Jefferies — アナリスト
こんにちは、おはようございます。質問をありがとうございます。Stephenに質問があります。
RSVでは、2人のプレイヤーが読み取れる結果が出ました。1つは80%で、プラスマイナスだと思います。1つは66%プラスマイナスで、エンドポイントによって異なります。そこで、競争力という点でハードルをどう見ているか、また、RSVワクチンの差別化の機会があるかどうかをお聞きしたいのですが、まもなく結果が出るかもしれません。
それについて少しお聞かせください。それから、PCVのフォローアップです。繰り返しになりますが、メルク社の参加は決まっています。データが出る直前のタイミングというのは、情報が不十分だったのでしょうか、それともデータ直前のオプトインの意味合いについて少しお話いただけますか?
スティーブン・ホゲ — プレジデント
マイケル、ご質問ありがとうございます。まずRSVについてですが、私たちのプラットフォームは以前COVID、特に呼吸器系ワクチンでその可能性を実証していますので、他のワクチンで見られた結果には非常に勇気づけられました。この結果は、私たちにとって良い兆しだと思います。
重症化については、ご指摘の通り、80%の範囲で確立されたバーがあります。私たちは、3つの症状、つまり “重症化 “を見ています。研究間の比較は困難です。全く同じ時期に実施されたわけではありませんし、ご存知のように、常に全く同じ定義で実施されているわけでもありません。しかし、私たちは、重症化した疾患に対する有効性が、他の研究で見られたものと同等であることを期待し、また、それ以上であることを望んでいます。
COVIDについては、当社のプラットフォーム技術が他の技術と比較して、そのような潜在的な利益を確認することができたことは確かです。RSV-AとRSV-Bの両方に対する中和RSVの力価の向上は、他社の結果と同等であったと考えています。ですから、私たちはこの結果にとても勇気づけられました。この冬には、RSVの有効性に関する結果が得られると思います。
私たちの目標は、他と同等かそれ以上であることです。PCVについては。PCVに関しては、Matthewも質問していましたが、Merckが参加することになりました。ですから、以前開示したように、オープンラベルの試験です。
私たちは、KEYTRUDAと併用したがんワクチンを投与された人と投与されなかった人について、この試験を通じて事象を追跡してきました。そして、この試験で無作為化された最後の患者さんのフォローアップが1年を過ぎたので、少なくとも1年間のフォローアップができ、さらに、2つの異なるコホート(併用療法を受けた患者さんと標準治療のKEYTRUDAを受けた患者さん)のフォローアップが2年以上できるようになりました。このデータは、私たちとメルク社が知っているものです。しかし、重要なのは、このデータは現在進行中の未解析であり、一次解析ではないことです。
オープンラベルでありながら、今この時点で行うべき正しいことは、クロージングプロセスを開始し、すべてのスキャンを入手し、臨床試験に関連するすべてのデータを見直し、見落としがないことを確認することです。そして、データベースを完成させ、研究の主要な分析、つまり、2群間のハザード比とその統計的有意性を評価するのです。これが今、私たちが行っているプロセスです。そして、このデータがポジティブかネガティブか、ポジティブの強さ、Matthewの質問のように次のデータ開発にどれだけ早く進めるかを決定する前に、これらのデータセットに対して正しいデリジェンスをすべて実施することが重要なのです。
そして、その作業は現在進行形で行われています。メルク社がオプトインを決定したのは、カレンダーと契約に基づいてであり、明らかにオープンラベルの情報にアクセスできたことによりますが、本当に重要な分析、一次分析は、規制当局や他の人々と同様に、次に何をすべきかという我々の決定の基礎となるもので、今まさに実施しようとしているもので、まだ完了していませんが、今四半期中にはその結果が出ると思います。
Michael Yee — Jefferies — アナリスト
ありがとうございます。とても参考になりました。ありがとうございました。
オペレーター
[次の質問はバークレイズのジーナ・ワンさんからです。どうぞよろしくお願いいたします。Gena Wang — Barclays — アナリスト
ありがとうございます。スティーブ メルクについてのコメントもお願いします。メルクが無再発生存率の非盲検データを見たかどうかを確認したいのです。それから、P1モデルのコントロールが過去のデータに沿ったものであること、7日前半であることも確認したいです。また、PCV第2相のデータはどのように共有されるのでしょうか。もう一つの質問は、スライド19、グローバルでのコビッドの市場機会についてです。
米国での大幅な価格上昇が予想されますが、20ドルから40ドルの価格帯を提示されていることから、主要市場における米国外の価格変動はどの程度を見込んでおられますか。
スティーブン・ホーグ — プレジデント
ゲーナ ありがとうございます。繰り返しになりますが、この試験は連続したデータセットではありません。オープンラベルの試験です。ですから、メルク社との契約により、彼らは、オプトインするかどうかを決定しなければならない時点で、このプログラムについて我々が何を知っているかを知る権利がありました。
そこでもちろん、私たちはその時点の研究データにアクセスできるようにしました。そして、皆さんもご存じのように、彼らはそのプログラムに参加することを選択しました。彼らは明らかに、非常に多くの経験を持っています。対照群に関しては、KEYNOTE-054試験があり、これは彼らの先行登録試験です。
コントロール群に何を期待するかという経験があるのです。そして、このプログラムに参加し、現在行っている一次解析に進む価値があるという彼らの決断から、好きなように推論することができると思います。対照群、つまり標準治療としてKEYTRUDAを投与された50人の患者を、登録試験やメルク社などの企業が持つ長年の患者経験と比較することで、もし実際に差が見られたとしても — ハザード比の差が見られたとしても、対照群との差ではないことを確信することができます。現時点では、この試験での有効性に関する主要な分析が完了した時点で、今四半期に発表する予定のデータは、PCVに関するトップラインデータのみです。
その後、会議やその他の適切な場で、より詳細なデータセットを共有する予定です。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
次に、価格に関する質問をお受けします。ご質問は主に米国外価格と当社の期待値に関するものでした。ここには2つの要素が絡んでいます。1つ目は、米国外の市場が、中央調達型のパンデミック設定から、流行型の設定に移行するタイミングとその速さです。
私たちは、さまざまな地域や国が、より風土病対策的なアプローチや商業的なアプローチにどのように戻っていくかを見ています。そのような状況になれば、やはり、世界中のさまざまな医療システムで提供される価値に応じてワクチンの価格を設定することになるでしょう。また、各国の規制や公衆衛生当局のガイダンスに基づき、費用対効果のガイドラインに関する確立されたシステムに従っています。全体的な世界平均価格は、地域ミックスによって大きく左右されると予想しています。
そのため、最終的な価格を予測することは困難です。しかし、需要の変化や価格の変化を見極めながら、今後も情報を発信していきます。
運営担当者
ありがとうございました。次の質問はコーウェンのタラ・バンクロフトからです。どうぞよろしくお願いします。
タラ・バンクロフト — コーウェンアンドカンパニー — アナリスト
どうも、みなさん。質問をお受けいただきありがとうございます。2023年に締結したAPAの45億ドルから55億ドルが底値と見ていいのでしょうか?また、今後契約を予定している地域から、最低限どの程度の売上を追加できるとお考えでしょうか。また、これに関連して、プレスリリースで言及された主要市場での売上はどの程度含まれますか。例えば、最新の米国での契約によるオプションは含まれますか?
アルパ・ガライ — チーフ・コマーシャル・オフィサー
ご質問ありがとうございます。45億ドルから55億ドルというのは、すでにAPAを締結しているため、2023年に見込んでいるフロア売上と、2022年から23年への繰り延べ分ということになります。また、米国、EU、日本、オーストラリアなどの主要市場や、中南米、アジア太平洋、中東、コバックスなどの地域でも、追加的な売上を見込んでいます。また、ラテンアメリカ、EU、日本、オーストラリア、アジア太平洋、中東、コバックスなどの地域販売も見込んでいます。
オペレーター
ありがとうございました。[次の質問はJPモルガンのジェシカ・ファイからです。どうぞよろしくお願いいたします。
ジェシカ・ファイ — JPモルガン・チェース・アンド・カンパニー — アナリスト
おはようございます。おはようございます。私の質問を聞いてくださってありがとうございます。納期遅れの理由に挙げられている短期的な供給制約は、今のところ解消されているのでしょうか?この秋の二価ブースターの取り込みは、予想と比較してどうでしょうか?また、中国が欧米のmRNAワクチンを発注する可能性があるとのことですが、来年以降、ある程度合理的なスケジュールで実現できると、どの程度楽観視していますか?
ステファン・バンセル — 最高経営責任者
それでは、ステファンからです。最初に供給に関する質問をさせていただき、次にコマーシャルPCUに関するArpaの質問に移りたいと思います。ご承知のように、第3四半期は、製造の観点から非常に複雑な状況にありました。
6月末に米国で5つの製品を発売し、その製品は週末には薬局で販売されました。そして、1273で販売した1バイアル10回分の用量からのシフトです。そのため、基本的に必要なバイアル数が2倍、または同じ用量になりました。このように、Fill/Finishメーカーとの間には、かなり多くの問題点がありました。
現在も多くの店舗で販売されており、多くの問題を解決しているところです。また、2023年の秋には、より良い状態になるよう、年末に向けてしっかりとした修正を行うよう取り組んでいます。アルパ?
Arpa Garay — チーフ・コマーシャル・オフィサー
ワクチンの摂取に関する最初の質問です。ワクチン接種率については、世界中でばらつきが見られますが、これまでのところ、最も良いデータは米国市場からのものです。2022年のワクチン接種率を2021年と比較すると、特にCOVIDブースターの場合、実は同じようなパターンを追跡しており、11月、12月、その他の秋冬シーズンがどうなるかを見るにはまだ少し早いようです。
11月、12月、そして残りの秋冬シーズンがどうなるかを見るのは少し早いですが、初期のレートは絶対値としてはかなり低いものの、昨年と比較して我々が予想した通りの傾向をたどっています。世界では、公衆衛生当局の主導により、説明会参加率が非常に高い市場もあります。また、他の市場では、夏に4回目の接種を受けたばかりの人たちが、5回目の接種を受けるまで数カ月待つように規制当局から勧告されるなど、今年発生した動きをまだ見ているところです。ですから、世界中で追跡調査を続ければ、もっと多くのことが分かると思います。しかし、摂取の初期兆候は心強いものです。
最後に、中国についてお聞きします。中国でのビジネスチャンスについては、引き続き検討しています。今のところ新しい報告はありませんが、私たちにとって商業的に重要な市場であることは間違いありません。
オペレーター
ありがとうございました。[次の質問はバンク・オブ・アメリカのジェフ・ミーチャム・ジェフからです。どうぞよろしくお願いします。
Geoffrey Meacham — バンクオブアメリカ・メリルリンチ — アナリスト
おはようございます。ああ、質問をありがとう。2つほど質問があります。最後のコメントのフォローアップをしたいと思います。
ブースターの導入は地域によってまちまちだとおっしゃいましたね。これは、バリューブースターや追加フォローアップ、研究に関して、モデナがさらなる投資を期待するものなのでしょうか?それが最初の質問です。2つ目は、ステファンの質問になりますが、バランスシートはかなり強固なままです。買い戻しは行っているようですが、買収や本格的な資本配分のようなものは見当たりません。
M&Aは現金の使い道として、優先順位のどのあたりに位置づけられるのでしょうか?また、COVIDの収益基盤が22年よりも23年の方が縮小し、今後さらに縮小していく中で、その状況は変わっていくのでしょうか?
アルパ・ガライ — チーフ・コマーシャル・オフィサー
ワクチン接種率に投資しているかという最初の質問ですが、本日お伝えしたように、COVIDブースターワクチン接種に対する医療ニーズは引き続き明確であり、特にインフルエンザによる入院や死亡と比較した場合、その必要性は明らかです。ですから、私たちが実際に行っているのは、政府や公衆衛生機関と提携し、国レベルで現在進行中の医療ニーズと、その集団におけるCOVIDブースターワクチン接種の価値という観点から、私たちが持っているデータを共有することなのです。そして、このような公衆衛生当局とのパートナーシップにより、ワクチン接種に関する緊急性を高め、行動を起こすことができるのです。これが私たちのアプローチです。
私たちは、公衆衛生当局が、住民のワクチン接種を促進するための最良の立場にあると信じています。
ステファン・バンセル — 最高経営責任者
アルパさん、ありがとうございます。バランスシートの面では、ジェイミーが発言したように、私たちの最大の戦略は変わっていません。ご存知のように、技術ライセンスやM&Aを検討していますし、すでに契約も結んでいます。以前から申し上げているように、私たちは依然として核酸にフォーカスしています。
低分子化合物や高分子化合物、細胞治療薬などを購入することは、戦略上、あまり良いことだとは思っていません。だから、同じ核酸を本当に欲しいと思っています。ジェイミーも彼のチームも知っているように、大きなチームは非常にアクティブです。私たちが多くのことをやっているところに、彼らは多くの仕事をやっています。
以前から申し上げているように、技術面、生物学的側面、価値を理解する上で、リスクを理解するという点で、私たちは規律正しくあり続けたいと考えています。私たちは価値を創造するためにここにいるのであって、プレスリリースを管理するためにいるのではありません。しかし、チームは非常に活発です。定期的にディリジェンスを行っていますが、すべての案件が多くの価値を創造できるものではありません。
今後、数カ月、数四半期にわたって提携先を増やしていっても不思議ではありません。
Geoffrey Meacham — Bank of America Merrill Lynch — アナリスト
ありがとうございました。
オペレーター
[次の質問はUBSのEliana Merleからです。お電話をお待ちしております。Eliana Merle — UBS — アナリスト
質問をお受けいただき、ありがとうございます。RSVについてもう1つだけ。COVIDワクチンを超えて、RSVの文脈でワクチン様式としてのmRNAについて考えるという点で、RSVの文脈でmRNAの可能性と他のより伝統的なワクチン様式と比較した潜在的優位性についてどうお考えでしょうか?また、今後発表される予定の資料から、RSVの可能性だけでなく、他の方法と比較した場合のワクチンにおけるmRNAの可能性について、私たちが学べることは何でしょうか?
Stephen Hoge — 社長
そうですね。ご質問をありがとうございます。まず、私たちは以前COVIDのプラットフォームで実証していますし、実際、最近の論文ではインフルエンザでも、一般的に本当に幅広く、バランスの取れた免疫反応が見られることが分かっています。T細胞や細胞媒介性免疫が非常に高くなる傾向があり、抗体中和価も常に高いとは言えないまでも、高い値を示すと思います。
高齢者と呼吸器感染症については、この2つが非常に重要です。このプラットフォームの特徴である、強力な細胞媒介性免疫の生成能力、T細胞の増強は、重症化予防に重要ですが、季節性防御のための非常に高い力価を達成することで、やはり高い中和力、つまり感染量の障壁となる力価を得ることができ、これは高齢者にとって本当に重要なことです。この組み合わせこそが、プラットフォームの観点から見た当社の優位性であり、高齢者を対象とした、この分野の主要なウイルスキラーを網羅する呼吸器系ワクチンのポートフォリオを開発することに、当社が非常に興奮している理由なのです。RSVはまさにその典型です。
ご存知のように、現在、この分野には大きなアンメット・ニーズがあります。第3相試験の登録が完了し、非常にうれしく思っています。開発初期に確認された力価や細胞媒介性免疫に非常に満足していますし、そのうちのいくつかは私たちが公開で発表しました。ですから、その有効性を読み取るのが楽しみです。
他のアプローチとしては、組換えタンパク質、ウイルスベクター、アジュバントアプローチが、この2年間、つまり1年か1年半の間に、さまざまな企業で本当に素晴らしい進歩を示していることを祝福したいと思います。RSVは非常に大きなアンメット・ニーズを抱えています。そこにインパクトを与えるには、さまざまなアプローチが必要です。しかし、高齢者向けにはさまざまな解決策があるはずです。
私たちは、私たちのプラットフォームが優位性を持っていると信じています。しかし、他のワクチンの成功や、非常に有望な有効性の結果を考えると、成功する優れた選択肢が数多く存在することに留意することが重要です。
Eliana Merle — UBS — アナリスト
素晴らしい。ありがとうございます。
オペレーター
[次の質問は、ニーダムのジョセフ・ストリンガーからです。お待たせしました。ジョセフ・ストリンガー — ニードハム・アンド・カンパニー — アナリスト
おはようございます。質問をお受けいただき、ありがとうございます。2022年の契約からの繰り延べ、20億ドルから30億ドルについて、明確にしたいのですが。これらは契約済みAPAに固定されており、23年に繰り延べられるだけなのでしょうか?それとも何かオプションがあるのでしょうか?2つ目の質問は、より広い範囲でのパイプラインについてです。
パイプラインは48プログラム、35の臨床試験と拡大していますね。パイプラインの相対的な構成、呼吸器ワクチン、免疫腫瘍学、希少疾患について、現在の状況と、時間の経過とともにパイプラインプログラムの相対的な構成がどのように変化していくとお考えでしょうか?
ジェイミー・モック — 最高財務責任者
それでは、最初のものを手短に説明します。これは2023年までの先行購入契約で、2022年から右肩上がりになっています。
Stephen Hoge — 社長
なるほど。パイプラインについては、ご指摘の通り、48のプログラムがあります。現在、複数のフェーズ3が進行中で、かなり間際の読み出しになることも期待しています。現在、後期パイプラインの大半は呼吸器系ワクチンの商業化です。4つのプログラムがあり、インフルエンザとRSVのデータはすぐに出てくると思います。
そして、呼吸器系では混合ワクチンに急速に移行する予定です。現在、成人用混合ワクチンが3種類あり、臨床試験が行われています。小児用呼吸器混合ワクチンは2種類あり、現在進行中です。一価ワクチンの観点からもそうですが、最も重要なのは、私たちが本当に守りたいさまざまな集団、特に高齢者や幼い人たちに対して、重要なウイルスに対する組み合わせから、最高の呼吸器ポートフォリオを構築することができるようになることでしょう。
ですから、呼吸器系は当面の間、私たちにとって成長分野となるでしょう。しかし、後期開発段階においては、多様化が進むでしょう。すでにCMVの第3相プログラムがあり、現在稼働中で、登録も始まっています。また、潜在性ウイルスワクチンについても、さらに後期プログラムが追加されることを期待してください。
エプスタイン・バー・ウイルスについては、皆さんもご存知の通り、かなり熱心に取り組んでおり、このプログラムも進めていく予定です。このように、潜在的ウイルスのポートフォリオの多様化が始まりますが、その一部はCMVで既に起こっています。また、個別化がんワクチン、治療用ワクチンプログラムからの成果も期待されます。このプログラムは、がんの再発を予防するものですが、すでにがんになっている人に介入するものなので、まさに治療薬と言えます。
そのため、治療的な側面も持っています。そして、この四半期に予定されている1カ月ほどの治療効果判定は、それが成功すれば、主要な臨床試験へと移行するきっかけとなります。ご存知のように、免疫腫瘍学は明らかに競争の激しい分野です。現在のIO療法を改善する必要性が依然として高い分野であり、さまざまな組織や種類のがんが存在するため、私たちが効果を示せば、プログラムを開発する意義があります。
ですから、このような拡大は非常に早く起こる可能性があり、ワクチン分野以外の治療分野では、オンコロジーへの大きな多様化となるでしょう。そして最後の1つは、希少疾患についてです。すでにいくつかのプログラムが、薬理学的にも臨床的にも、非常に有望な結果を示し始めています。例えばプロピオン酸血症のプログラムでは、投与量を決定し、そのプログラムの進むべき道について規制当局との整合性が取れたと確信したらすぐに、そのプログラムでも主要な試験に移行することを期待していてください。
それから、先ほどの質問にもお答えしましたが、これは私たちにとって単なる一過性のものではありません。私たちは、あるモダリティを手に入れたと確信した時点で、多くのプログラムを次々と並行して進めていくつもりです。パイプラインの多様化をどう考えるかは、もっと大きな問題で、時間軸の問題なのです。今は、呼吸器系と潜在的なものが多いですね。
しかし、すぐに呼吸器系を拡大し、治療薬、特にがんや希少代謝疾患への参入を拡大することができると考えています。そしてそれは、今後の臨床試験の結果に基づいて、極めて短期間に実現する可能性があります。
ジョセフ・ストリンガー — ニードハム・アンド・カンパニー — アナリスト
素晴らしい。質問に答えてくれてありがとうございます。
オペレーター
[次の質問はSVB証券のマニ・フォルハルさんからです。お待たせしました。Lili Nsongo — SVB Securities — Analyst
リリ・ノソンゴです。予想される数量について質問があります。2023年については、ばらつきがあるため除外するとのことですが、2023年についてはどうでしょうか。しかし、2023年については、APAによる数量または収益のうち、どの程度を見込んでいるのでしょうか?また、現地でのワクチン使用について、より風土病的なモデルへと移行していく中で、将来的にAPAが発生することを想定していますか?
アルパ・ガライ — チーフ・コマーシャル・オフィサー
はい、ご質問ありがとうございます。来年の数量予想について説明したように、APAの締結以外でも、総数量に影響を与える可能性のある多くの変数を見ています。長期的には、現在のインフルエンザの数量に匹敵する5億から6億の数量に近づくはずだと考えています。
2023年には、ウイルスの進化や各地域の医療ニーズ、公衆衛生当局の推奨事項、さらには消費者のワクチン接種への意欲によって、さまざまな幅が生じると思われます。ですから、先ほどお話した数量に関する感度の理由は、流行段階への移行が続いているため、まだ多くの変数が存在するからです。しかし、医学的な見地から、時間の経過とともに、少なくともインフルエンザ市場と同程度の数量に近づくはずだと考えています。
オペレーター
ありがとうございました。それでは、これ以上のご質問はありません。それでは、最後にStéphane Bancelからご挨拶をさせていただきます。
ステファン・バンセル — 最高経営責任者
皆さん、本日は電話会議にご参加いただき、また丁寧なご質問をいただき、ありがとうございました。また、来週の第1回ESGデーもよろしくお願いします。良い一日をお過ごしください。それでは。
以上です。他の翻訳希望やご感想をいただけると嬉しいです。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>


