モデルナ(MRNA)2022年第2四半期決算説明会の日本語訳です。
売り上げ・EPS共市場予想を超えており良かったですね、8月に30億ドル相当の自社株買いも行うようなので好感されてます。
技術力は非常にあるので良い企業とは思ってますがワクチン以外の製品の上市が欲しいところです。
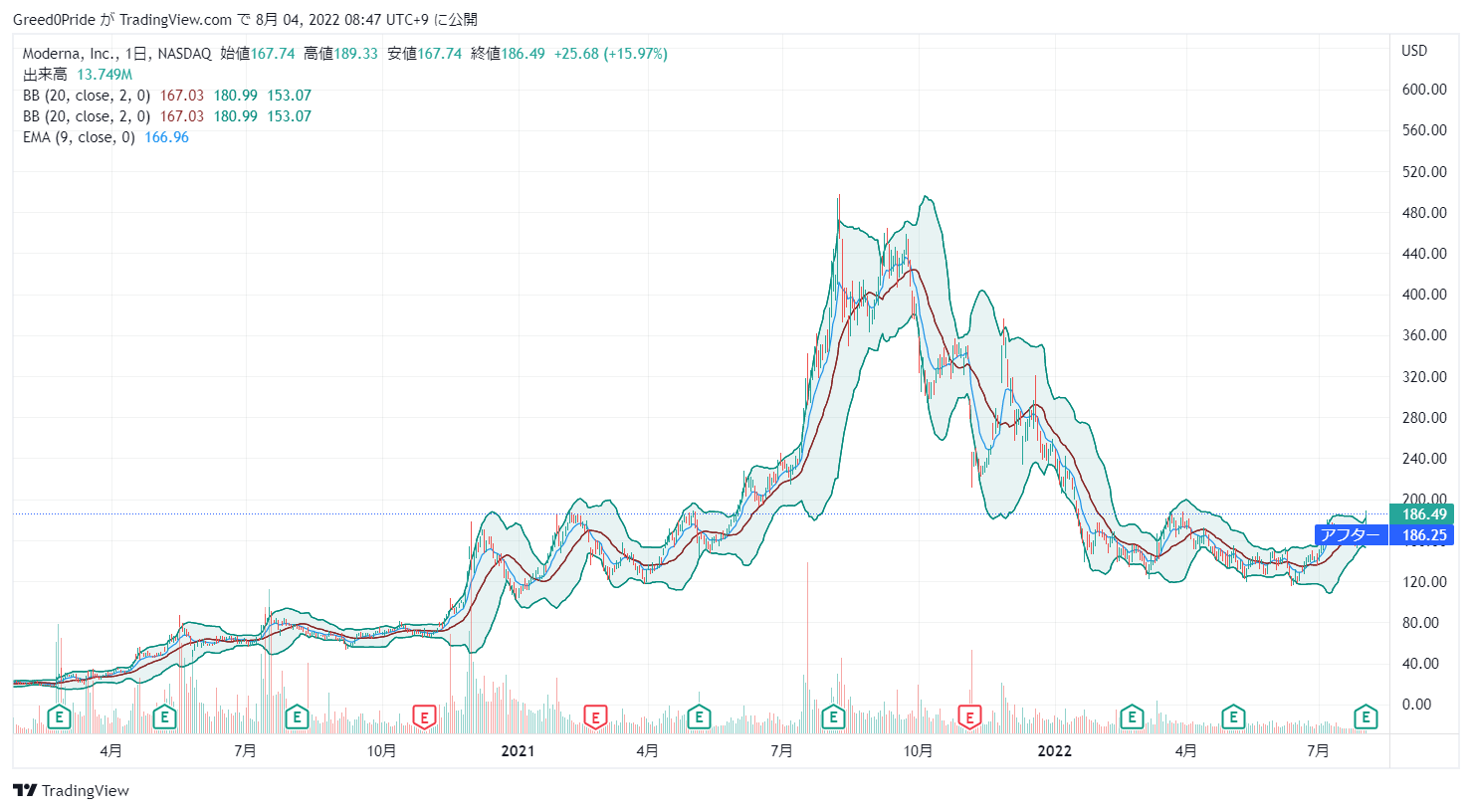
モデルナ(MRNA)株価
モデルナ(MRNA)2022年第2四半期決算説明会
Call participants:
Lavina Talukdar — Head of Investor Relations
Stéphane Bancel — Chief Executive Officer
Paul Burton — Chief Medical Officer
Stephen Hoge — President
Arpa Garay — Chief Commercial Officer
David Meline — Chief Financial Officer
Unknown speaker
Elizabeth Webster — Goldman Sachs — Analyst
Michael Yee — Jefferies — Analyst
Tara Bancroft — Cowen and Company — Analyst
Geoff Meacham — Bank of America Merrill Lynch — Analyst
Ellie Merle — UBS — Analyst
More MRNA analysis
2022年08月03日 午前8時00分
オペレーター
おはようございます。本日のオペレーターを務めさせていただきますケヴィンと申します。Modernaの2022年第2四半期決算説明会にようこそ。[オペレーターの指示】です。]
この通話は録音されていることをご了承ください。この時点で、電話をモデナのIR担当のラヴィナ・タラクダー(Lavina Talukdar)に引き継ぎたいと思います。どうぞ続けてください。
Lavina Talukdar — 投資家向け広報活動の責任者
ありがとうございます、ケビン。皆さん、おはようございます。本日は、Modernaの2022年第2四半期決算とビジネスアップデートについて、お電話にお付き合いいただきありがとうございます。今朝発表したプレスリリースと、これからご覧いただくスライドは、当社のウェブサイトの投資家向けセクションからアクセスできます。本日の電話会議には、最高経営責任者のステファン・バンセル、最高財務責任者のデビッド・メリン、社長のスティーブン・ホーグ、最高医学責任者のポール・バートン、最高商業責任者のアルパ・ガライが出席します。
この電話会議では、1995年米国民事証券訴訟改革法のセーフハーバー規定に基づく将来の見通しに関する記述が含まれていることにご留意ください。当社の実際の業績や結果が、これらの将来見通しに関する記述で明示または暗示されているものと重要な差異を生じる可能性がある重要なリスク要因については、添付のプレゼンテーションのスライド2および当社のSEC提出書類を参照してください。 それでは、ステファンに電話をかわります。
ステファン・バンセル — 最高経営責任者
ラヴィーナさん、ありがとうございます。皆さん、おはようございます、あるいはこんにちは。2022年第2四半期のカンファレンス・コールへようこそ。本日は、スパイクバックスの新しいリアルワールドエビデンスデータをポールが説明する前に、簡単なビジネスレビューから始めたいと思います。
そして、スティーブンが臨床プログラムをレビューします。私はコマーシャル・ダイナミクスについて説明し、デビッドが財務状況を説明する予定です。そして、私が最後に戻り、今後の方向性について考えを述べたいと思います。当四半期、当社は引き続き好調な財務実績をあげました。
売上高は47億ドル、当期利益は22億ドルとなりました。第2四半期の売上高には満足しています。純利益の減少は、主にCOVAX契約に起因する当四半期の売上原価の増加、デビッドが財務の中でそう呼んでいること、4つのフェーズ3プログラムを含む将来のための研究開発投資の大幅な増加、そして2021年第2四半期よりも高い税率が原因となっています。自社株買いプログラムを通じて、第2四半期に900万株の株式数を減らしました。
2021年の最初の自社株買いプログラムの開始から昨日までで、約1800万株の自社株買いを行いました。2022年の納品予定分として約210億円の先行購入契約を引き続き締結しています。また、本日、当社の商業的な勢いとバランスシートに基づき、取締役会が30億ドルの追加的な自社株買いプログラムを承認したことを発表しました。次に、前回のレビュー以降の事業およびパイプラインの最新状況を確認させてください。
私は、パイプラインを製品上市に近づけ、パイプラインの幅を広げるために、Modernaチームが重要な進展を遂げたことを嬉しく思っています。商業面では、最近、米国政府と、オミクロンに対する二価のブースターワクチンについて、当初6,600万回分の新たな契約を締結しました。この契約には、さらに2億3,400万回分を購入するオプションも含まれており、合計で3億回分の売上が見込まれます。
契約締結・発表後、米国政府はすでに400万回分の追加オプションを行使しています。そのため、現在の総量は、実際には米国政府と2022年秋に契約した7,000万ドーズとなっています。
さらに、カナダと英国は、2022年に追加納入するために、現在の契約についてオプションを行使していました。規制面では、米国で小児および若年層への投与が認められたことを大変うれしく思います。
また、カナダ保健省およびオーストラリアでは、小児用医薬品として承認されました。カナダ保健省とオーストラリアも、生後6カ月から5歳までの子どもたちへのワクチン使用を許可しています。当社の研究・臨床チームは、当社のパイプラインの勢いを維持しました。
現在、COVID二価ブースター、インフルエンザ、RSV、CMVの4つの第3相臨床試験が進行中です。重要なのは、mRNA-1020/30を用いた第1相試験で、従来のインフルエンザ抗原と新規抗原を標的とした2種類のワクチンが、現在完全に登録されていることです。また、インフルエンザワクチンとコビドワクチンの混合ワクチンの第1/2相試験も登録が完了しています。安全性と免疫原性の成長プログラムに関するこの読み出しに期待しています。
また、がん領域におけるチェックポイント・ワクチンのINDがオープンになっており、GSDA1希少疾患プログラムでは最初の患者さんに投与しました。最後に、2つのプログラムについて、今年中に概念実証試験のデータを共有できることを大変うれしく思います。希少疾患プログラムであるプロピオン酸血症(PA)のフェーズ1/2と、個別化がんワクチンとキイトルーダの併用療法(キイトルーダ単剤療法)のフェーズ2データです。スライド6は、2022年8月のModernaの通常のスナップショットで、ワクチンだけでなく治療薬も含む46のプログラム開発によるパイプラインの幅広さを示しています。
当社は強固な基盤を持っています。3,400人のチームと11の商業子会社があり、約180億ドルのキャッシュを持つ強力なバランスシートが当社の成長を支えています。それでは、ポールに話を譲りたいと思います。
ポール・バートン — チーフ・メディカル・オフィサー
ステファン、ありがとうございます。COVID-19のパンデミックが続き、SARSのCOV-2ウイルスが著しい進化を遂げる中、多くの人にとって最も関心のあるテーマはブースト、いつブーストをかけるか、何をかけるか、でしょう。次のスライドでは、Moderna mRNA-1273ワクチンがブースターとして臨床的にどのように機能しているか、またmRNAワクチンでプライミング・ブーストした人の抗体レベルが実環境でどのように機能しているかをお見せしたいと思います。次のスライドは、スペインの全国登録者300万人以上におけるCOVID-19の感染率を示しています。
これらのデータから得られる最初のポイントは、ブースティングが非常に効果的であり、感染リスクを減少させるということです。2つ目は、mRNA-1273(Modernaワクチン)がBNT-162b2よりも有効であり、その効果量は時間とともに増加することです。2つ目の例では、米国のVAシステムから、ここで緑で示したmRNA-1273と赤で示したBNT-162b2のどちらかでブーストした45万人以上のデータをお見せしています。
ここでも、感染や入院の予防という点で、mRNA-1273は代替mRNAワクチンよりも有効であると結論付けています。最後に、NHSイングランドのデータベースに登録された300万人以上のデータですが、ここでも、COVID-19の感染と入院が、BNT-162b2よりもmRNA-1273ブーストの方が、感染のオミクロン期間中に臨床的に意味があり、統計的に有意に減少していることが示されています。ここで、私たちが最近、モデナコミュニティで実施した革新的で分散型の実用的な実地試験のデータについて説明したいと思います。この試験はdisCOVEriesと呼ばれ、約850人の参加者を登録し、一次ワクチン接種後の抗体レベルの実臨床評価と、モデナ・モデルナ・モデルナ(MMM群)またはファイザー・ファイザー・ファイザー(PPP群)によるブースティングを行いました。
重要なのは、研究対象者の平均年齢が44歳であることです。参加者の約6割が女性です。そして、民族的にも非常に多様です。参加者は試験に登録され、同意の上、[Inaudible]から家庭用自己投与型マイクロニードル採血キットを受け取りました。
ここに見られるように、懸念されるSARS-CoV-2の様々な分散において、最初のブースター接種後8週間から32週間まで、赤のモデナ製ワクチンを接種した人は青のファイザー製ワクチンよりも高い抗体価が認められ、Y軸の対数スケールで示した耐久性のある抗体価が得られました。この比較の多くは、統計的に有意な差が認められました。それは、懸念されるomicron BA.1変異体に対する抗体レベルにおいても同様で、ファイザーワクチン接種者に比べ、モデナプライムブースト接種者では約12週間の持続期間の優位性が認められます。これらのデータは、実臨床におけるブースティングの設定において、モデナワクチンの高いパフォーマンスを示しており、これは懸念される様々な変異体に対する高い耐久抗体レベルによって説明される可能性があります。
それでは、スティーブン・ホーグ博士に、COVID-19ブースターワクチン4種の構成やその他のパイプラインの最新情報についてのコメントをお願いしたいと思います。スティーブン?
スティーブン・ホーグ — 社長
ポール、ありがとうございます。皆さん、おはようございます。私は、次の秋のシーズンに向けて、オミクロンを含むCOVIDブースターに関する最近のアップデートを手早く確認し、アルパに渡す前に、当社の残りのパイプラインを確認します。2022年の秋冬シーズンには、異なる市場の需要に対応するため、2つの二価の候補を進めています。
MRNA-1273.214は、当社のオミクロンBA.1を含有する二価医薬品です。214は、現在承認されているブースターと比較して、BA.4、BA.5に対する中和価を有意に上昇させるという臨床データを第2/3相試験で既に発表しています。 214は、EU、オーストラリア、英国、カナダ、スイスで承認申請を行い、その後、各国の規制当局と協議の上、承認されました。mRNA-1273.222は、BA.4/BA.5亜種をベースにしたオミクロン含有ワクチンと当社オリジナルのmRNA-1273を組み合わせた2価ワクチン候補です。
FDAは、214および211の二価ワクチンブースターを用いた第2/3相試験のデータなど、懸念される亜種に対する当社の二価ワクチンプラットフォームの強さが実証されたことに基づいて、222の承認申請を行うよう求めています。また、FDAは、パンデミックの進展に伴い、これらのデータが有用であるとして、222の臨床試験を開始するようメーカーに助言しています。この試験は8月に開始する予定です。次に、スライド16の呼吸器系ワクチンのパイプラインについて説明します。
オミクロン配合のコビドブースターを確認したところです。また、6月に南半球でインフルエンザワクチンmRNA-1010の免疫原性試験を開始したことを発表し、今秋にはmRNA-1010の有効性試験の開始を準備しています。HA抗原とNA抗原にまたがる8つのmRNAを持つ次世代インフルエンザワクチン、mRNA-1020 1030も、その第1/2相試験の登録が完了しました。RSVプログラムは、高齢者を対象とした第3相試験と小児科を対象とした第1相試験を含め、現在進行中です。 重要なのは、今期、COVIDプラスインフルエンザワクチンの第1/2相試験の登録が開始され、完了したことです。
このデータが得られ次第、ご紹介できることを楽しみにしています。 COVID+インフルエンザ+RSVの混合ワクチンも、今年中に臨床に入る予定です。当社の風土病用ヒトコロナウイルスワクチンは、小児用RSV+hMPV混合ワクチンとともに前臨床段階にあります。また、小児用HMPV+PIV3ワクチンのフェーズ1bは、現在、完全に登録が完了しています。次に、潜在性ワクチンと公衆衛生ワクチンのポートフォリオについて説明します。
CMVワクチンは第3相試験が進行中です。伝染性単核球症予防のためのEBVワクチンは、現在、第1相試験を実施中です。また、ウイルスによる長期的な後遺症を予防するEBVワクチンも前臨床段階にあります。HIVワクチンの第1相試験とジカ熱ワクチンの第2相試験は、すべて進行中です。
HSVとVZVのワクチンも前臨床段階にあります。そして最後に、NIHと共同で実施しているニパワクチンの第1相試験で、最初の被験者を投与しました。最後に、スライド18にある治療薬パイプラインについて説明します。ステファンは、PCVとPAプログラムの概念実証試験から今年後半にデータが得られる見込みであることをすでに述べました。
このスライドで強調したいのは、その他の重要な最新情報です。まず、GSD1a試験で最初の患者を投与し、チェックポイントがんワクチンのINDを開始することができたことは喜ばしいことです。次に、アストラゼネカ社から、ポートフォリオレビューの結果、VEGFプログラムを返却するとの通知があり、現在、この資産の次のステップを評価しています。最後に、自己免疫疾患を対象としたIL-2プログラムの初期臨床データのレビューと、進化する競争環境に基づいて、当社はこのプログラムのさらなる開発を中止し、パイプラインから削除することを決定しました。 それでは、Arpaにバトンタッチします。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
ありがとうございます、スティーブン。皆さん、おはようございます。モデナの執行委員会の新メンバーとして、私はCOVIDでのインパクト、そしてCOVIDでの商機、さらには当社のmRNA技術を活用した長期的なワクチンや治療薬に期待しています。 次にスライド20に目を移しますと、第2四半期および2022年上半期の地域別売上高構成比が示されています。当四半期の北米の売上高は16億ドルでした。
この売上は、米国政府からの最初の受注を達成するために米国に納入した1273本のブースターに牽引されたもので、その大部分は今年の第2四半期末までに納入されています。また、当四半期には、5歳以下の小児患者を対象としたプライマリーシリーズの承認が得られたため、このグループにも投与しました。EMEA向けの売上は15億ドル、アジア太平洋地域向けの売上は11億ドルでした。 第1四半期、第2四半期の売上は、北米が27億ドル、EMEAが39億ドル、アジア・パシフィック地域が30億ドルでした。
なお、3ヵ月間、6ヵ月間ともに、これらの主要地域において売上高の地域的分散が見られました。この多様性は、当社がいかに迅速にグローバルな営業組織を構築し、実行したかを反映したものです。次に、スライド21をご覧ください。私たちは、世界中でグローバルな規模拡大を続けていますが、ブースター市場(3回目または4回目のブースター投与と定義)におけるスパイクバックスの市場シェアが、引き続きかなりのシェアを示していることも嬉しく思っています。
ステファンが既に述べたように、スライド22に2022年秋の新しい米国政府との契約を示しています。具体的には、当初は当社の二価のCOVIDブースターを6,600万回分、2022年に納入する契約となっていました。今週初め、米国政府から、2価の「コビド
今週、米国政府から、小児用として400万回分のオプションが行使されたとの連絡がありました。これにより、契約総額は約18億ドルとなりました。米国政府からの受注には、さらに2億3,000万回分の購入オプションが含まれており、すべてのオプションを行使した場合、合計で3億回分の投与が可能となります。
先ほどスティーブンから聞いたように、FDAのガイダンスに従って、米国の秋のブースター製品は、1273とオミクロンBA.4/5の部分変量からなるmRNa-1273.222となります。ここで、パンデミックの進展とそれによる商業的見通しへの影響について、少し時間をかけて説明したいと思います。パンデミックの初期には、ウイルスの進化、その時々の人々の免疫力、季節的な傾向など、いくつかの要因によって、流行地が変わるだろうと予想しており、この図解は以前にもお伝えしました。
このような要因は、これまでも、そしてこれからも、商業的な展望に影響を与え続けるでしょう。 異なる時期に複数の変異型が出現し、それが優勢になるにつれて、私たちはこれらの変異型に対応するブースターを開発することができるようになりました。現在、異なる市場ニーズに基づき、2022年秋に向けて2つの二価ブースター候補を進めています。mRNA-1273.214とmRNa-1273.222という2つの2価のブースター候補を進めています。どちらも現在認可されているブースター1273を25マイクログラムと、BA.1またはBA.4/5のいずれかのオミクロン亜変種を25マイクログラム含んでいます。
これらのブースターは今年9月に納入が開始されますが、製造の増強と世界各国の規制当局の認可取得に伴い、第4四半期に比重が高くなる予定です。最後に、2023年に向けて、コビドブースターの米国における商業市場への移行に備え、米国政府がワクチンの唯一の購入者であったパンデミックの時よりも市場が細分化されることになります。
商業組織は、このシフトを見越して、すでに商業支払者やチャネル(チャネル販売業者や主要な薬局など)と連携しています。国際的には、公衆衛生当局が引き続きワクチンの主要な購入者となることが予想されますが、民間の商業市場が存在する可能性のある市場も特定しつつあります。全体として、当社は米国と世界の両方で商業インフラの構築に投資してきたため、この移行に対して十分な準備が整っています。
それでは、デビッドに話を譲りたいと思います。
David Meline — 最高財務責任者
OKです。アルパさん、ありがとうございます。本日は、2022年第2四半期決算の実績分析と、今後の財務パフォーマンスの主要なドライバーについての見解をお伝えします。全体として、私たちは引き続き順調に進んでおり、業務・商業パフォーマンスには非常に満足しています。
スライド 25 では、第 2 四半期の業績概要からご説明します。2022年第2四半期の製品売上高合計は45億ドルで、前期に比べ3億3,400万ドル(8%)増加しました。2022年の製品売上高総額の増加は、主にカスタマーミックスの変化による当社COVID-19ワクチンの平均販売価格の上昇に起因するものです。2022年第2四半期の総売上高は47億ドルで、当社のCOVID-19ワクチンの売上増加により、前年同期と比較して3億9,500万ドル増加しました。
売上原価は14億ドルで、2021年同期の製品売上高の18%に対し、2022年第2四半期は製品売上高の30%でした。これには、過剰で陳腐化したCOVID-19製品に関連する在庫評価損4億9900万ドル、確定購入契約損失1億8400万ドル、未使用の外部製造能力に対する費用1億3100万ドルが含まれています。これらの費用は、前回の電話会議で先行購入契約に影響を及ぼす可能性のある変数として示された、コバックス社への納入予定量の大幅な削減、および、他の顧客、特に欧州連合への納入の延期(当社の二価ワクチン更新の今後の発売予定に照らして)によってもたらされています。2022 年第 2 四半期の研究開発費は 710 百万ドルで、前年同期に比べ 289 百万ドル(69%)増加しました。
研究開発費の増加は、特にCOVID-19およびRSVプログラムでの臨床試験費用と、拡大・成熟する開発ポートフォリオのための人件費に引き続き起因しています。2022年第2四半期の販売費および一般管理費は211百万ドルで、前年同期に比べ90百万ドル(74%)増加しました。支出の増加は、当社のCOVID-19ワクチンの世界的な商業化に加え、加速する会社設立を支援するための人材と外部サービスへの継続的な投資によるものです。2022年第2四半期の実効税率は11%(2021年同期は9%)でした。
2020年末に23億ドルの繰越欠損金があり、昨年の報告税率に非経常的な利益をもたらしている事実を思い出してください。2022年第2四半期の税引き後純利益は、2021年同期に比べ5億8300万ドル(21%)減少し、22億ドルとなりました。この減少は、主に当四半期の売上原価及びその他の営業費用の増加によるものです。2022 年第 2 四半期の希薄化後 1 株当たり利益は、2021 年同期に比べ 1.22 ドル(19%)減少し、5.24 ドルとなりました。
次に、スライド 26 の前年同期比の累計決算に目を向けます。2022年上半期の製品売上高は105億ドルで、前年同期に比べ45億ドル(76%)の増加となりました。2022年の総売上高の増加は、主に当社の製造能力の増強によるもので、若干ではありますが、カスタマーミックスが良好で、平均販売価格が上昇したことによるものです。2022 年上半期の総売上高は、2021 年同期の 63 億ドルに対し、108 億ドルとなりました。
総収入の増加は主に、当社のCOVID-19ワクチンの米国外での売上増加によるものです。2022年上半期の売上原価は24億ドルで、製品売上高の23%でした。これは、報告ベースで前年同期の製品売上高の16%、2020年に費用化された上市前の在庫費用を調整すると19%です。製品売上高に対する売上原価の増加は、主に過剰在庫および陳腐化在庫の評価損費用の増加–および将来の購入約束と未使用の外部製造能力に関連する費用–、さらに、2021年第1四半期に実現した発売前在庫給付がなかったことが、その程度を低下させたことによるものです。
2022 年 1-6 月期の研究開発費は 13 億ドルで、前年同期比 4 億 4200 万ドル(54%)の増加となりました。研究開発費の増加は、引き続き、COVID-19二価ブースター開発を含む開発ポートフォリオの拡大・成熟のための臨床試験費用、人件費、外部サービスによるものです。2022年上半期の販売費および一般管理費は479百万ドルで、前年同期に比べ281百万ドル(142%)増加しました。支出の増加は、当社のCOVID-19ワクチンの世界的な商業化、およびデジタルへの多額の投資を含む加速する会社設立のサポートに起因しています。
さらに、2022 年第 1 四半期には、新たに設立されたモデルナ財団のための初期前払寄付金 5,000 万ドルがありました。上半期の実効税率は13%(2021年同期は7%)でした。この増加は主に、2021年に当社の繰延税金資産の大部分に対する評価引当金の解除に関連して計上された利益によるものです。2022 年上半期の税引後当期純利益は、2021 年同期に比べ 19 億ドル(46%)増加し 59 億ドルとなりました。
純利益の増加は、製品の売上高の伸びによるものです。2022 年 1-6 月期の希薄化後 EPS は、2021 年同期に比べ 4.55 ドル(49%)増加し、13.85 ドルとなりました。次に、スライド 27 の現金および現金預金に目を向けます。2022年第2四半期末の現金および投資残高は、本年第1四半期末の193億ドルに対し、181億ドルとなりました。
この減少は、第2四半期に13億ドルの自社株買いを行ったことを反映しています。将来の製品供給に関する現金・預金の期末残高は、前四半期末の53億ドルに対し、41億ドルとなりました。前四半期比で減少しているのは、顧客からの預かり資産に対する製品の納入によるものです。次に、スライド28をご覧ください。
当社の資本配分の優先順位に変更はありません。これまでも、そしてこれからも、様々な分野での基盤事業への再投資を最優先します。前述のとおり、2022年上半期の研究開発費は13億ドルで、前年同期比54%増となりました。通期の研究開発費予想である25億~30億ドルについては、引き続き計画通りに推移しています。
当社の第二の投資優先課題は、Modernaの技術と能力の範囲をさらに拡大するために、魅力的な外部投資と協力の機会を求めることです。当社は、当社のプラットフォームを実現し補完する魅力的な機会を検討しており、外部投資の可能性を評価する際には規律あるアプローチをとっています。当社は、当社のプラットフォームを有効かつ補完する魅力的な機会を検討し、外部投資の可能性を評価するための規律あるアプローチを取っています。内部および外部の投資機会を評価した後、現金の追加的な使途を検討します。
2022年第2四半期に、900万株を13億ドルで買い戻しました。昨年の自己株式取得活動の開始以来、8月2日までに、1,800万株、希薄化後の発行済み株式の約4%、総額30億ドルを購入しました。なお、当社は今年2月に30億米ドルの自社株買いプログラムを発表し、現在約10億米ドルの自社株買い枠が残っています。本日のプレスリリースでは、取締役会が30億ドルの自社株買いプログラムを期限を定めずに追加で承認したことを発表しました。
次に、29 ページに記載されている 2022 年度の最新の財務フレームワークについて説明します。当社は引き続き、2022年に約210億ドルの先行投資契約を締結しています。これには、先日発表した米国政府との新たな契約による売上見込みと、前回の電話会議でその可能性を示唆した、需要不足によりコバックス社が割り当てられなかった用量の調整分が含まれています。
なお、この合計額には契約時の為替レートに対するマイナスの影響が含まれており、現在のレートが年末まで継続すると仮定した場合、2022年通期で売上高の約1.5%と試算しています。2022 年下半期の売上については、COVID-19 ワクチンの承認見込み時期および新製品の製造立ち上げに伴い、第 3 四半期よりも第 4 四半期の売上が多くなると予想しています。当社の総売上原価には、製造原価、他社からのロイヤルティ、物流・倉庫費などが含まれています。2022年通期の売上原価は、前述のCOVAX社への投与量削減と他の顧客への投与延期に関連する費用により、20%台半ばとなる見込みです。
製品改良にともなう追加費用が発生した場合、売上原価は20%台後半に増加する可能性があります。研究開発費及び販売費・一般管理費については、開発ポートフォリオの成熟化とグローバルなスケールアップに伴い、通期で約40億ドルの費用を引き続き見込んでいます。現在の税法にもとづくと、国際的な事業構成による海外由来の無形固定資産利益や株式報酬削減の効果により、2022 年の実効税率は 10%台前半から半ばとなる見込みです。最後に、設備投資額については、グローバルに製造及び一般事業会社のインフラを整備するため、 引き続き6億米ドルから8億米ドルの範囲で計画しています。
以上、業績に関する私の発言を終え、ステファンに電話を戻します。
ステファン・バンセル — 最高経営責任者
デビッド、アルパ、スティーブン、ポール、ありがとうございました。2022年、私たちは5つの重要な優先事項を実行することに着手しました。まず、210億ドルの先進的な専門分野での契約に対して、ワクチンを提供することを実行することです。今年の半分が過ぎ、2022年秋の契約済み案件と強力な製造チームにより、私たちは目標通りに進んでいます。後期臨床試験では、インフルエンザ、RSV、CMVの第3相試験で勢いがあり、このように積極的なタイムラインを実現しているチームに感謝しています。
当社の技術を応用した2つの治療法の概念実証試験のデータは、PAとPCVの試験データとともに、下半期に共有する予定です。ワクチンと治療薬の新たな開発候補についても、引き続き進展がありました。いくつかはすでに発表されており、さらに下半期には発表される予定です。そして最後に、パートナーであるバーテックス社との吸入型LNPの最近の発表により、予備軍疾患をターゲットとするmRNAのプラットフォームが拡大されました。 私たちは成長するにつれ、患者さんやステークホルダーのために正しいことを正しい方法で行うことを約束します。
創業者チームが率いる企業として、私たちは5年、10年、20年の単位で考えています。この報告書では、患者さん、従業員、環境、地域社会、そしてもちろんガバナンスといった、当社の企業責任のフレームワークの主要な柱を紹介しています。私は、この柱を中心に私たちが行っていることを誇りに思っていますし、私たち自身に設定した野心的な目標をとても誇りに思っています。私は、こうした野心的な目標を達成するための第一歩は、目標を設定し、その目標を達成するための目的志向の文化やガバナンスの枠組みを作り、育成することだと考えています。
その一例として、2030年までに全世界で炭素排出量をゼロにするという目標を掲げ、Modernaを地球と組織のために長期的に持続可能な成長を促進するグローバルリーダーの一角に位置づけています。11月10日に開催されるESG Dayでは、当社のESGの歩みをより詳しくご紹介する予定です。その前に、9月8日の年次総会で皆様をお迎えすることを楽しみにしています。mRNAサイエンスの約束を果たし、患者さんのために新世代の革新的な医療を実現するというModernaの使命は、常に私たちの北極星でした。
インフレとそれに伴う金利や資本コストの上昇など、金融市場における課題にもかかわらず、モデナは非常に恵まれた立場にあります。私たちは独自のmRNA Aプラットフォームを有しており、革新的な医薬品をかつてないスピードで生み出すことができます。また、使命感にあふれた3,400人の従業員からなる強力なチームを有しています。バランスシートには180億ドルの現金があり、強力な商業的勢いがあります。
私たちは、成長を減速させるつもりはありません。私たちは頭を低くして、仕事をこなしています。今、減速している場合ではありません。患者さんは革新的な医療を待っているのです。ご清聴ありがとうございました。では、質問をお受けします。
オペレーター?
質疑応答
操作方法
[オペレーターからの指示]. 最初の質問はマシュー[聞き取れない]からです。あなたのラインは開いています。スピーカー不明
素晴らしい おはようございます。私の質問に答えてくれてありがとうございます。ステファン、買収や提携の機会についてどのように考えているのか、もう少し具体的に教えていただけないでしょうか。
投資家の間でよく話題になるテーマだと思いますが、多くの人が考える範囲はさまざまで、かなり大規模なものと、プラットフォームに対して技術面でより補完的なものとがあると思います。そこで、優先順位についてどのように考えているか、教えていただければと思います。ありがとうございました。
Stéphane Bancel — CEO(最高経営責任者
Matthew、ご質問ありがとうございます。ご存知のように、私たちは1年以上前から資本配分の戦略をとっており、キャッシュフローがプラスになる状況です。優先順位は1番目です。
1.事業への投資、2.会社設立のための外部投資、そして3.自社株買いです。 この数四半期でご覧いただいたように、社内研究開発への投資という点では、この戦略に完全に合致していると思います。Davidが申し上げたように、今年の第2四半期の研究開発投資は、昨年の第2四半期に比べて69%増加しました。また、本日発表した3回目の自社株買い計画も、非常に積極的なものでした。ご覧のように、昨年は外部との共同研究においていくつかの案件を実施しました。
現段階では買収は行っていません。これは、ご指摘の通り、革新的な医薬品を生み出すというミッションを実現するために、会社の可能性をどのように広げていくか、ということだと考えています。そして、外部との提携では、興味深い資産を見つけることと、自分たちが価値を創造できると思う価格で見つけること、この2つのフィルターが常に重要だと考えています。今日、Davidが確認したように、私たちのチームは非常に忙しく、さまざまなものを見ています。しかし、ご存知のように、投資家が投資先企業を探すのと同じで、何かを決定する前に多くのものを見る必要があるのです。
素晴らしいアセットが見つかれば、遠慮はしない。しかし、そのような資産もたくさんあります。会社の戦略に合わない資産もたくさんある。これからも探し続けます。
大規模な買収のために大規模な買収をするのは、私たちの戦略ではありません。私たちがやりたいのは、世界一の核酸メーカーになることです。これまで述べてきたように、核酸の領域にとどまる限り、mRNAの外に出ることは非常に喜ばしいことです。買収も喜んで行います。
良い資産が見つかれば、喜んでパートナーシップを結ぼうと思います。買収は、それ自体についてではありません。これが、私たちが外部投資について考えていることです。
発言者不明
ありがとうございました。
運営者
次の質問まで、少々お待ちください。次の質問はゴールドマン・サックスのエリザベス・ウェブスターからです。どうぞよろしくお願いします。
Elizabeth Webster — Goldman Sachs — Analyst
どうも、皆さん。サルビーン社のエリザベスです。四半期決算おめでとうございます。1273.222の承認までの道のりを教えていただけますか?また、どのような経路をたどるのか、正確に教えてください。
また、今月から開始される試験のデータはいつ頃見ることができますか?次に、APA210億ドルの上積み要因についてお聞きしたいのですが、どこから上積みされるのでしょうか。また、新たな受注を獲得する可能性はありますか?ありがとうございました。
スティーブン・ホゲー — プレジデント
質問をありがとうございました。最初の質問は私が受け持ち、2番目はArpaにパスするとします。まず222番についてですが、これはBA.4, BA.5変異体をベースにした二価ワクチンで、このワクチンの承認について、特に米国ではFDAのガイダンスと焦点になっていることが質問の主な内容だと思います。前臨床試験と製造データの両方、そして基礎となる二価のプラットフォームデータをまとめるために、私たちは引き続き努力しています。
この2つの第2/3相試験と前臨床データ、製造データの合計が申請資料となり、これは公表されたFDAガイダンスと一致しています。FDAはまた、あなたが言及したように、将来の展開をサポートするための追加試験を実施するよう、私たちに要請しました。そして、ワクチンの配備について、そのような決定を下すための情報を提供できるようなサンプルを得たいのです。この研究は8月に登録される予定ですが、ブーストされたサンプルを入手し、収集し、関連するアッセイでテストするのに約1ヵ月かかるため、データが得られるのは数ヵ月後になります。
現時点では、承認前にデータが必要になるとは考えていませんし、FDAもそのようなことは示唆していません。実際、私たちは211と214の先行臨床データ、前臨床データ、製造データに基づいて認可を行う予定です。しかし、そのサンプルは手元にあるはずです。222のデータを秋以降に共有できるようになる具体的な時期については、FDAの最近のガイダンスに基づく承認に必要ないことを再度強調する以外、今日は特に何もありません。
これは本当に、今後の展開の決定をサポートするためのものであり、FDAのガイダンスの後半になります。
Arpa Garay — チーフ・コマーシャル・オフィサー
次に、210億ドルのガイダンスに関する2つ目の質問をお受けします。アドバンスドパーチェスアグリーメントの観点からは、市場の需要の大部分はこの210億ドルに含まれていると考えています。とはいえ、多くの国々が公衆衛生上のニーズや推奨されるブースター人口を評価し、これらの人口への拡大の可能性を検討しているため、当社は二価ワクチンの追加発注の可能性について世界各国と協議を続けています。ですから、210億ドルという数字には満足していますが、214あるいは222の二価ワクチンに対する追加需要があるかどうか、いつあるかについては、引き続き各国と協議を続けていきます。
Elizabeth Webster — Goldman Sachs — アナリスト
了解しました。ありがとうございました。
オペレーター
次の質問まで、少々お待ちください。次の質問はジェフリーズのマイケル・イーからです。どうぞよろしくお願いします。
Michael Yee — Jefferies — アナリスト
おはようございます。質問と最新情報をありがとうございます。BA.4/5 222の認可取得に関するコメントについて、簡単に質問させてください。Stephen、あなたはその経路について言及していましたね。
しかし、私は実際に少し前向きに考えたいと思いました。将来、インフルエンザのような前臨床データだけで、変種や開発ワクチンが迅速に認可されることを想定していますか?また、FDAはそのような方向に進んでいると思いますか?これが最初の質問です。2つ目の質問ですが、皮肉なことに、あなたはサル痘ワクチンについてコメントしましたね。そして今、WHOは世界的な健康上の緊急事態についてコメントしました。
この件に関する最新情報はありませんでしたが、何か進展があったのでしょうか?ありがとうございました。
スティーブン・ホゲー — プレジデント
マイケル、ご質問ありがとうございます。両方受けてみます。まずアプローチについてですが、おっしゃるとおり、COVIDワクチンとブースターについては、毎年、株の更新を行い、株を確定するインフルエンザのモデルが将来的に意味をなすと信じています。
その意味で、222の承認は、もしFDAや他の市場で実現すれば、本当にその最初の事例となります。 私たちは、この枠組みを実現するための補足的なBLAを申請し、その枠組みから引き離す必要があります。しかし、私たちは、米国だけでなく、世界中の規制当局と積極的に協力し、その道筋を確立するよう努力しています。なぜなら、結局のところ、プラットフォームをフルに活用して毎年対応するためには、将来的に承認前に臨床試験を実施しないことが理にかなっているからです。また、インフルエンザ・モデルとプラットフォームの世界的なパフォーマンス(現在、数十億人規模)は、毎回臨床試験を必要としない、より一般的なアプローチに成熟する可能性を示し始めていると考えています。
これが私たちの期待であり希望です。秋から冬にかけて規制当局と協議し、これらの申請を完了させ、2023年に向けて準備を進めていきます。この秋の222件の経験は、新しい標準になるための最初の事例となるかもしれませんね。 サルモネラ菌については、研究プログラムを開始しました。私たちは、その動向を注意深く見守っています。
最近の公衆衛生に関する発表や、ワクチン供給に関する懸念の高まりを受け、私たちは — 現在の流行に介入すると同時に、この公衆衛生上の脅威における供給に関する長期的な問題に対処するために、私たちのプラットフォームを使ってサル痘ワクチンを供給するにはどうすればよいかを検討し始めています。そのような議論についての最新情報はありません。今後、話し合いを進めていく予定です。その中には、適切であれば、規制当局との協議も含まれるでしょう。
そして、臨床開発に移行するかどうか、その道筋が明確になれば、もちろん、最新情報を提供します。しかし、現段階では、前臨床試験のプログラムであることに変わりはありませんが、最近の動向を考えると、非常に注意深く追跡しているプログラムのひとつです。
Michael Yee — ジェフリーズ — アナリスト
了解です。ありがとうございました。
オペレーター
次の質問まで、少々お待ちください。次の質問はバークレイズのGena Wangです。お待たせしました
スピーカーが不明です
ハイ、ゲーナの代わりのシェルドンです。質問を受けてくださってありがとうございます。質問が2つあります。
1つは、2022年のAPAについてです。COVAXの契約はまだ何回分割り当てられていないのか、また210億ドルのガイダンスの中でどのように説明されたのか、コメントいただけますか。また、2023年のAPAについても教えてください。また、来年の需要についてどのように考えるべきでしょうか。続いて、インフルエンザワクチン(mRNA-1010)の第3相免疫原性試験について質問します。予想されるデータのタイムラインはどのように考えていますか?北半球でも登録が必要なのでしょうか?ありがとうございます。
スティーブン・ホゲー — プレジデント
最後の質問を先にさせてください。それとも…
アルパ・ガレイ — チーフ・コマーシャル・オフィサー
もちろんです、順番にお聞きします。繰り返しになりますが、210億ドルの前倒し購入契約には、コバックス投与量の追加割り当ては含まれていません。そのため、コバックス諸国からの需要の減少をすでに反映しており、今年いっぱいは、これらの国々からの追加注文や需要はほとんどないと予想しています。
2023年の受注に関しては、すでに発表した5カ国、イギリス、カナダ、オーストラリア、クウェート、台湾と契約を締結しています。また、カナダ、スイス、台湾ともオプション契約を締結しています。そして、2023年の追加受注に向けて、世界各国と積極的に対話をしています。これらの先行受注がどのようなものであるかについては、今年の終わりか来年の初めに、追加のガイダンスを提供することができる予定です。
スティーブン・ホーグ — プレジデント
素晴らしい。それから、現在進行中のインフルエンザの第3相試験についてですが、これは南半球の免疫原性と安全性の試験です。先ほど申し上げたように、この試験は現在進行中です。現在、どのような状況にあるのか、その特徴はまだわかっていません。
現時点では、この試験を北半球で行う必要はないと考えていますので、南半球での安全性免疫原性試験を終了する予定です。今年の後半には、北半球で第3相有効性試験を実施する予定です。そのため、今年は北半球での比較試験を実施する予定ですが、現在進行中の第3相試験、つまり、早期承認の裏付けとなる安全性免疫原性試験は実施しない予定です。
発言者不明
南半球の免疫原性データのうち、2022年の後半にデータが出そうなのですね?
スティーブン・ホゲ — プレジデント
ですから、いつごろのデータが得られるかについては、特にご案内していません。しかし、一般的に、安全性免疫原性試験は、登録後、29日目、つまり、1カ月後に非劣性または優越性のエンドポイントを追跡します(聞き取れず)。ですから、登録が完了すれば、すぐにデータが出ます。しかし、最終的には、安全性データのフォローアップも行い、規制当局がどのようなフォローアップやデータを望むかについて相談したいと思います。
そのような協議がすべて終わるまでは、時期について具体的にご案内することはありません。
発言者不明
ありがとうございました。
司会
次の質問まで、少々お待ちください。次の質問はコーウェンのタイラー・ヴァン・ビューレンからです。どうぞよろしくお願いします。
タラ・バンクロフト — コーウェンアンドカンパニー — アナリスト
こんにちは おはようございます タイラーに代わってタラです。ファイザーが言っていた1月1日からの11%のシェアアップについて、何かコメントを頂ければと思います。
例えば、アデノワクチンのシェアが減少していることから、そのほとんどがアデノワクチンからもたらされているのでしょうか?もちろん、Spikevaxのシェアの変化がどこから来ているのかにも興味があります。
Arpa Garay — チーフ・コマーシャル・オフィサー
もちろん、そのご質問はお受けします。シェアに関しては、本日報告したシェアは、Spikevax Acrossの3回目と4回目のブースターの累積シェアで、ファイザーが共有しているいくつかのデータとは異なっています。このように、私たちのビジネスの源泉の大部分は、市場シェアを維持し、場合によっては市場シェアを拡大することで、現在に至っています。
また、現在および将来の成長の大部分を占めるブースター人口に焦点を当てます。
Tara Bancroft — Cowen and Company — アナリスト
わかりました。ありがとうございます。
オペレーター
次の質問まで少々お待ちください。次の質問はバンク・オブ・アメリカのジェフ・ミーチャムからです。どうぞよろしくお願いします。
Geoff Meacham — Bank of America Merrill Lynch — アナリスト
やあ、みんな。質問をありがとうございます。スライド23で、COVIDの長期的な機会について例示されていますね。23年以降の投資について、ガイダンスを求めるわけではありませんが、数量や患者数などの観点から、流行段階のテールについてどのようにお考えでしょうか。また、資本配分の面でも関連する質問ですが、皆さんは事業への投資をどのようにお考えでしょうか。ステファンは、スライドの中で、モデナの技術をさらに拡大することを目標に掲げています。
しかし、その外側にある機能を追加することをどのように考えていますか — その外側にある、周辺的なものかもしれませんが、中核となるmRNAから少し離れて、どこまで舵を切るつもりなのか、よく分かりませんでした。ありがとうございました。
スティーブン・ホゲ — プレジデント
そうですね。最初の質問についてはArpaと私がタッグを組んで、M&AについてはStephaneのところに来ると思います。まず、この写真にある病気の罹患率についてですが、私たちは、風土病のヒトコロナウィルスは、季節的な病気が発生すると考えていますし、残念ながら、突破口の感染や入院、そして死亡も発生するでしょう。これは、特にリスクの高い人たちの間で、いつまでも続くでしょう。
問題は、その高リスクとは65歳以上なのか、50歳以上なのか、18歳以上で高リスクの要因を持つ人なのか、あるいは広くなのか、ということですが、これは本当にウイルスの進化によります。予想するのは困難です。しかし、時間が経つにつれて、インフルエンザや流行中のヒトコロナウィルスと同じように、毎年、多くの人々に中和防御力を高めて感染症を予防し、その恩恵を受ける季節性の市場になると考えています。アルパ、この市場がどのように発展していくか、コメントをお願いします。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
唯一付け加えるとすれば、私たちは世界中の政府機関と緊密に連携し、対象人口やブースターを推奨する頻度について、彼らの推奨がどのように進化しているかを確認し続けるということです。ですから、私たちは彼らと協力し続け、時が経つにつれて需要がどのように形成されるかを見ていくつもりです。
Stéphane Bancel — CEO(最高経営責任者
ありがとうございます。資本配分についてですが、以前にもお話ししたように、私たちは情報分子、つまり核酸で勝負することに非常に興味を持っています。ご存知のように、私たちはヒトのタンパク質を発現させるためのmRNAだけを見ているわけではありません。遺伝子編集によるmRNAにも注目しています。
ご存知のように、私たちはすでにこの分野でいくつかの提携を結んでおり、近い将来、皆さんに最新情報をお伝えできるのを楽しみにしています。しかし、遺伝子治療の分野では、RNAも潜在的な関心分野であることをお話ししました。ですから、核酸の分野では本当に頼りになると思います。これまでにもお話ししてきたように、低分子や高分子にこだわることは、3年、5年、10年というスパンで見た場合、Modernaのベストバージョンを作るということではありません。
核酸に関しては、できることがたくさんあると思います。また、研究、開発、CMCにまたがるプラットフォームへのプラグアンドプレイが可能なことも気に入っています。ですから、ただ製品のために製品を手に入れ、会社をより複雑にし、核酸との共通点が少ないと思われる技術に手を出すことに比べ、真の利益とシナジーがあるのです。
Geoff Meacham — Bank of America Merrill Lynch — アナリスト
そうですか。素晴らしい。ありがとうございます。
司会
次の質問まで少々お待ちください。最後の質問はUBSのエリー・マールからです。お待たせしました。
Ellie Merle — UBS — アナリスト
やあ、みんな。質問をお受けいただき、ありがとうございました。パイプラインと資本配分を考える上で、優先順位をどう考えているか、自社株買いとさらなる事業展開について教えてください。それから、猿痘について2つ目の質問ですが、前臨床試験で検討していると発表されて以来、公衆衛生の緊急事態や幅広いワクチンのニーズを考慮し、ここからの計画やさらなる開発計画について少しコメントいただけないでしょうか?
ステファン・バンセル — 最高経営責任者(CEO
それでは、資本配分についてお話します。Davidが数四半期前から使っているスライドで説明しているように、私たちの優先順位の第1位は、ビジネスへの投資であり続けています。私たちは、私たちが持つプラットフォームにとても期待しています。
ご存知のように、ワクチンの分野では、ワクチンのモダリティにリスクがあるため、かなり積極的な投資を行っています。現在、すでに4つのワクチンが第3相に移行しているのは、注目に値します。前回の電話会議でもお話しましたが、ワクチンの臨床試験の開始から第3相試験の開始まで、約12ヶ月という時間枠を3回にわたって実現することができました。もちろん、今年の後半には、癌と希少疾患におけるヒトでのプルーフオブコンセプトが控えており、これは興味深いものです。
この2つのうちの1つ、あるいは両方がうまくいって興味深い臨床シグナルが得られれば、おそらくワクチンと同じように、非常に迅速に拡大することができるでしょう。ご存知のように、メッセンジャーRNAの優れた点の1つは、私たちが多くのロボット工学やデジタル化を駆使して会社を構築してきたことで、非常に迅速に拡張することができるということです。希少疾患や癌などの新しいアプリケーションでは、技術がうまくいくかどうかがわかる前に、いくつかのプログラムから始める予定です。しかし、例えば、PAでポジティブな結果が出た場合、希少疾病の分野で今よりも多くのプログラムを迅速に開発することになるのでしょうか?答えは「イエス」です。
また、がん領域でも何かあると思います。ですから、事業への投資は最優先事項です。優先順位No.
2番目は、パートナーシップ、ライセンシング、M&Aを通じてプラットフォームを拡大することです。そして、余剰資金を株主に還元していきます。本日、取締役会が新たに30億ドルの自社株買い計画を発表したのは、社内で有効な使い道が見つからない場合に資本を還元できることを確認したためだと思います。[聞き取れず)猿轡?
スティーブン・ホーグ — 社長
はい、そうです。ですから……概念的には、私たちは明らかにサルモネラ菌に関する懸念を強く認識していますし、最近の発表にも非常に敏感になっています。ですから、私たちが考えているのは、もしそのプログラムを開発するとしたら、どのようにそれを動かすかということです。その目的は、非常に迅速に行動することです。 先ほどStephaneが説明したように、当社のプラットフォームはかなり確立されています。迅速に拡張する能力も実証済みです。
もし私たちがサルモネラ菌の臨床開発プログラムに取り組むとしたら、それは臨床試験で承認可能な一連のエンドポイントに向かって非常に迅速に前進することでしょう。その意味でも、規制当局と協議し、どのような道を選ぶかを決める必要があります。私たちにとって、プログラムを進めて第1相臨床免疫原性を実証することが第一の関心事ではなく、公衆衛生対策に貢献するために行うものです。ですから、そのような対話は、私たちが始め、関わっていくことになります。
また、現在、より大きな公衆衛生の脅威が存在することも認識しています。COVIDは依然として公衆衛生上の大きな脅威であり、多くの規制当局はこの秋のブースター更新作業への対応に全力を注いでいます。ですから、私たちはそのことを尊重します。しかし、私たちはそのような会話に参加するつもりです。
そして、エンドポイントが何であるかを考慮した上で、前進するかどうかが明確になれば、当然それを提供します。しかし、現時点では、これらのエンドポイントを明確にしていないため、これ以上のことを言うのは時期尚早であり、したがって、現段階で前臨床プログラムを臨床開発に移行するかどうかについて、我々自身が決定しているわけではありません。
Ellie Merle — UBS — アナリスト
ありがとうございます。
Stéphane Bancel — 最高経営責任者
皆さん、本日はお電話でご質問いただき、誠にありがとうございます。9月上旬に開催するR&D Dayで、多くの方々とお話できることを楽しみにしています。良い一日をお過ごしください。ありがとうございました。
以上です。他の翻訳希望やご感想をいただけると嬉しいです。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>



[…] 前回の2022年第2四半期決算説明会はこちらです。 […]