ギリアド・サイエンシズ (GILD)2022年第4四半期決算説明会決算説明会の日本語訳です。
好決算と増配で株価も上昇です。製品の開発力もあるので今後も期待したい銘柄ですね。
カップウィズハンドルっぽいチャートなので気になってましたがこのままブレイクアウトを期待したいです。
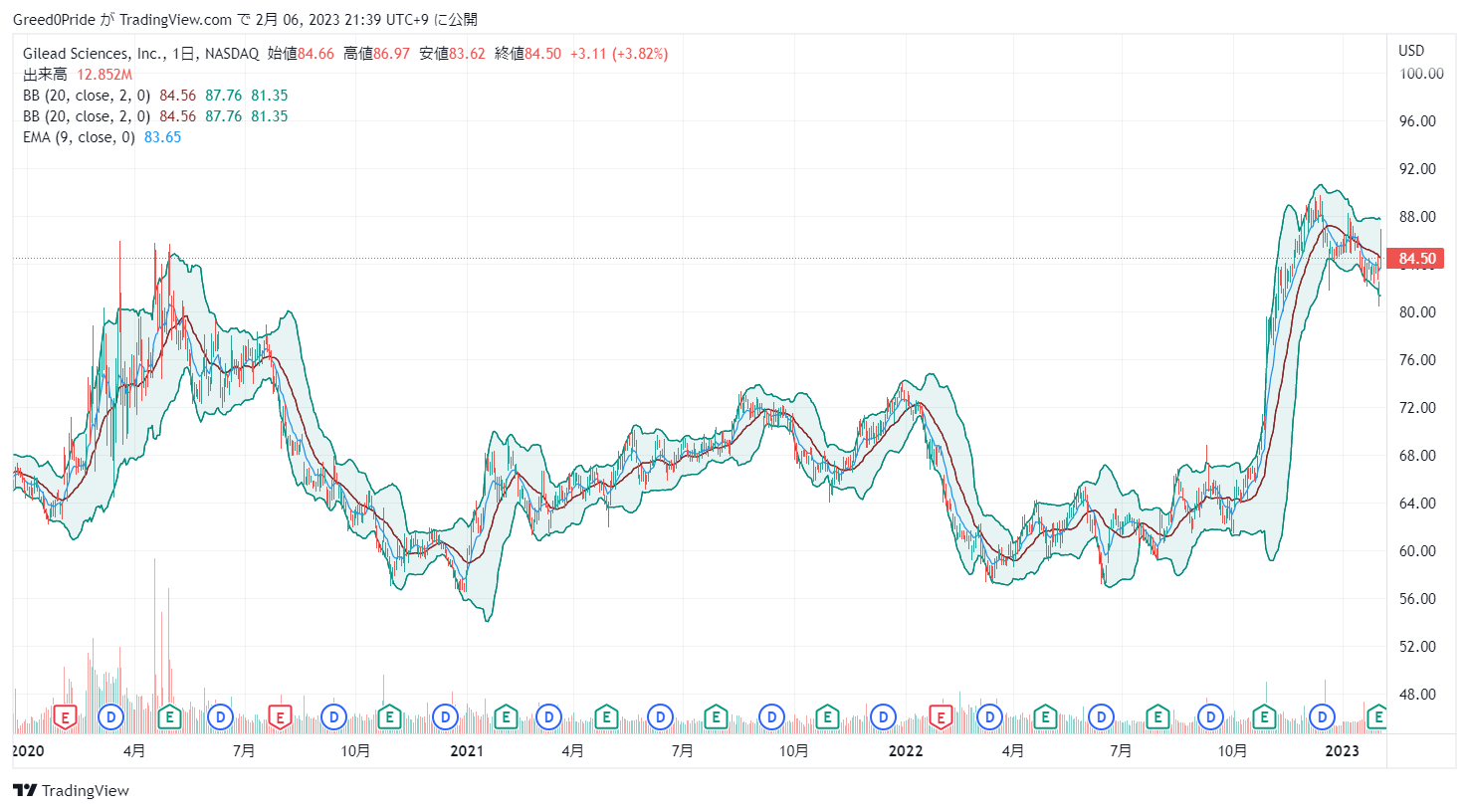
ギリアド・サイエンシズ (GILD)株価
ギリアド・サイエンシズ (GILD)2022年第4四半期決算説明会
Call participants:
Jacquie Ross — Vice President, Investor Relations
Dan O’Day — Chairman and Chief Executive Officer
Johanna Mercier — Chief Commercial Officer
Merdad Parsey — Chief Medical Officer
Andy Dickinson — Chief Financial Officer
Tyler Van Buren — Cowen and Company — Analyst
Geoff Meacham — Bank of America Merrill Lynch — Analyst
Michael Yee — Jefferies — Analyst
Guyn Kim — Piper Sandler — Analyst
Colin Bristow — UBS — Analyst
Chris Schott — JPMorgan Chase and Company — Analyst
Brian Abrahams — RBC Capital Markets — Analyst
Mohit Bansal — Wells Fargo Securities — Analyst
Umer Raffat — Evercore ISI — Analyst
Olivia Brayer — Cantor Fitzgerald — Analyst
Simon Baker — Redburn Partners — Analyst
Christi Shaw — Chief Executive Officer, Kite
Nicole Germino — Truist Securities — Analyst
Evan Seigerman — BMO Capital Markets — Analyst
More GILD analysis
2023年02月02日午後4時30分
オペレーター
こんにちは。本日は、ギリアド・サイエンシズの2022年第4四半期および通期決算の電話会議にご出席いただき、ありがとうございます。本日の電話会議のモデレーターを務めますハンナと申します。プレゼンテーションの部分は全回線をミュートし、最後に質疑応答の機会を設けます。
[それでは、司会のジャッキー・ロスに会議を引き継ぎたいと思います。どうぞよろしくお願いします。ジャッキー・ロス — インベスター・リレーションズ担当バイス・プレジデント
オペレーターの方、どうもありがとうございます。本日、市場が閉じた直後に、2022年第4四半期および通期の業績に関するプレスリリースを発表しました。プレスリリース、スライド、補足データは、当社ウェブサイトの投資家向けセクション(gilead.com)でご覧いただけます。本日の電話会議のスピーカーは、会長兼最高経営責任者のダニエル・オデイ、最高商業責任者のジョアンナ・メルシエ、最高医学責任者のメルダッド・パージー、最高財務責任者のアンドリュー・ディッキンソンです。
その後、カイト社の最高経営責任者であるクリスティ・ショーが加わり、質疑応答が行われます。その中には、ギリアドの事業、財務状況および業績、製品、製品候補、企業戦略、事業および業務に関する計画および期待、財務予測および資本手段、2023年の財務ガイダンスに関する記述が含まれます。これらの記述はすべて、当社がコントロールできない一定の仮定、リスクおよび不確実性を含んでおり、実際の結果がこれらの記述と大きく異なる可能性があります。これらのリスクについては、決算発表時のプレスリリースや最新のSEC開示資料でご確認ください。すべての将来予想に関する記述は、ギリアドが現在入手可能な情報に基づいており、ギリアドはそのような将来予想に関する記述を更新するいかなる義務も負わないものとします。
非 GAAP 財務指標は、当社の基本的なビジネス・パフォーマンスをご理解いただくために使用されます。GAAPから非GAAPへの調整表は、決算プレスリリースの補足データシート、およびギリアドのウェブサイトに掲載されています。それでは、ダンに電話をつなぎます。
ダン・オデイ — 会長兼最高経営責任者(CEO
ジャッキーさん、ありがとうございます。数週間前にサンフランシスコで多くの皆さんとお会いする機会がありましたが、今回、再びお会いして、2022年の第4四半期および通年の好調な業績と、2023年のガイダンスをお伝えできることをうれしく思います。これらの業績は、当社の事業変革の具体的な効果を示しており、特にHIVポートフォリオと急成長中の癌ビジネスが成長軌道に乗ったことを示しています。四半期業績の詳細はチームからご説明しますが、スライド4では、HCVの売上のピークが成長を牽引した2015年に、ベース事業において通期で最も力強い成長を遂げたことをご紹介します。
2022年通年のビクタービーの売上は前年比20%増の104億円となり、初めて100億円を超えました。Biktarvyを除いた2022年のベースビジネスは前年比8%増で、2023年の最初のガイダンスでは、ベースビジネスの成長率は4~6%を示していることをお伝えします。収益ガイダンスの詳細についてはアンディがお話ししますが、この機会に、成長軌道への復帰を果たしたギリアドの各チームを評価したいと思います。世界中の人々と地域社会の健康増進に対する彼らのコミットメントのおかげで、ギリアドは、これまで以上に多くの患者さん、より困難な疾患や状態にリーチを広げる態勢を整えました。
財務的な成果だけでなく、2022年の臨床的な進展も、私たちの歩みを補強しています。年末、サンレンカは米国で、多剤耐性HIV感染症の重い治療経験のある成人患者を対象とした初の承認を取得しました。これは、第3四半期に欧州で承認されたことに続くものです。
サンレンカは、承認された最初の6ヵ月皮下投与薬であり、予防と治療にわたって大きな可能性を持つ、近年のHIV治療薬における最もエキサイティングなイノベーションを象徴するものだと考えています。HIVコミュニティと協力してSunlencaの認知度を高め、当社の長時間作用型薬剤のポートフォリオを前進させることを期待しています。前治療歴のあるHR陽性HER2陰性転移性乳がんに対するTrodelvyのPDUFA日が近づいており、もう一つの承認の可能性があると期待しています。また、今年後半には欧州の規制当局から連絡があるものと思われます。
一方、トロデルヴィの商業的モメンタムは、2022年通年の売上高が79%増となり、高まっています。細胞治療では、リーダーシップを強化し、最近日本で承認された再発または難治性の大細胞型B細胞リンパ腫の二次治療薬であるYescartaの利用範囲を拡大する計画を引き続き実行します。パイプラインの最新情報と重要なマイルストーンについては、Merdadから少しお話があると思います。今のところは、過去4年間で2倍以上に増加した臨床プログラムの大幅な拡大について簡単にご説明します。
長時間作用型HIV治療プログラムにおいてレナカパビルと提携する新しい前臨床候補、新規経口ヌクレオシドCOVID-19の新しい第3相OAK CRE試験、今年開始予定の5つの第3相試験など、さらなるプログラムの追加を続けています。ヨハンナにバトンタッチする前に、1年前に皆さんと共有した臨床目標を簡単に振り返ってみたいと思います。ギリアド社とカイト社のチームは、計画通りの成果をあげると同時に、状況の変化に応じて機敏に行動し、素晴らしい成果をあげてきました。2022年、私たちは規律正しく断固とした実行力をもって素晴らしい1年を過ごし、2023年以降も実行力の実績がさらに強化されることを大いに期待しています。
それでは、第4四半期および通期の業績について、ジョアンナからご説明します。ジョアンナ?
ヨハンナ・メルシエ — チーフ・コマーシャル・オフィサー
ありがとう、ダン。そして皆さん、こんにちは。商業的業績についてお話しする前に、ギリアドのチームがまた素晴らしい四半期を過ごし、非常に成功した年を締めくくることができたことに感謝したいと思います。2022年はギリアドにとって例外的な年であり、当社のウイルス学フランチャイズは今後何年にもわたってリーダーシップを発揮し続けることができる位置にあり、当社の癌戦略の実行と世界中のより多くの患者の生活を改善するための新薬の提供において大きな進展がありました。スライド7より
当四半期は非常に好調で、ビクタービを除く製品売上高は63億ドル、前年同期比9%増、為替の影響とトゥルバダとアトリプラの独占権喪失を除くと12%増となり、当社の各主力フランチャイズで堅調な伸びを示し、全地域で再びHIVとがんがリードする成長を遂げました。前四半期比では、HIV、Trodelvy、細胞治療が牽引し、売上高は5%増加しましたが、HCVで一部相殺されました。通年では、ビクタービーを除く製品売上高は231億ドルで、HIVとがん領域に牽引され、前年比8%増、為替とトルバダ・トリプラLOEの影響を除くと11%増となりました。予想通り、2022年の通年ビクタールビー売上は2021年に比べて大幅に減少しました。
とはいえ、Biktarvyの業績はこれまでの予想以上に持続的であり、COVID-19の治療を受ける入院患者にとって不可欠な役割を果たし続けていることは明らかです。2022年には、第4四半期の10億ドルを含め、ビクタビは39億ドルを達成しました。全体として、通年の製品売上高は270億ドルで、ベースビジネスの成長がBiktarvyの売上減少で相殺され、2021年と比較して横ばいとなりました。スライド8では、第4四半期のHIVの売上高は、需要の増加に加え、良好な価格ダイナミクスにより、前年同期比5%増の48億ドルとなりました。
これは、第4四半期の在庫が通常より少なかったことによるもので、季節的な在庫管理に早くから取り組んできたことを反映しています。第4四半期のHIVの売上は6%増加しましたが、これは主に有利な価格設定と在庫の変動、および需要の増加によるものです。通期では、チャネルミックスによる平均実現価格の上昇に加え、「ビクタービー」の継続的な好調に関連し た需要の増加により、HIV の売上高は前年同期比 5%増の 172 億ドルとなりました。これは、在庫調整と為替変動の影響により一部相殺されました。
全体として、当四半期のHIV治療薬市場は、米国で前年同期比1.5%増、欧州で2%強の伸びとなりました。年間ベースでは、2%から3%という当社の予想通りの市場成長となっています。予防に移行する
米国のPrEP市場は、認知度の高まりを反映して、2022年第4四半期に前年同期比18%増、前四半期比3%増となりました。第4四半期の本コードの売上は5億3700万ドルで、前年同期比13%増、前四半期比7%増となりました。特筆すべきは、ジェネリック医薬品やその他の参入企業にもかかわらず、PrEP用Descovyの需要が引き続き増加しており、40%以上の安定した市場シェアを維持したことに加え、通年で20%以上増加していることです。
このようなトレンドと昨年のPAC IPの和解により、成長するペット市場において、Descovyの地位はさらに強化されました。全体として、このことは、10 年代半ばに真の長時間作用型 6 カ月ごとのレジメンとして PrEP 用レナカパビルを発売する可能性を見据えた強力な基盤となっています。スライド9のTrodelvyに移ります。当四半期の売上高は29億ドルで、前年同期比15%増でした。これは主に需要の増加、およびチャネル在庫の減少により一部相殺された有利な価格設定によるものです。
前四半期比では、需要の増加、ならびに良好な価格設定と在庫調整により、6%の増収となりました。Biktarvy は発売以来、四半期ごとに市場シェアを拡大し続けており、第4四半期も例外ではなく、前年同期比で3%ポイント以上シェアを拡大しました。この継続的な勢いは、昨年発表した5年間の長期データによって強化されたビクタービーの差別化された臨床プロファイルの証しです。特に、米国、欧州、その他の主要市場において、「ビクタービー」は依然として新規治療開始数No.1です。
2022年末には、世界中で約100万人がビクタービでHIVを管理していることになります。これらを総合すると、ビクタビは2022年に初めて100億円を超える通年売上高を達成することになります。
今後、ビクタビは、米国、欧州、その他の主要市場において、HIV治療薬のリーディングカンパニーであり続けることができると確信しています。さて、2023年のHIVの第1四半期を展望すると、いくつかのポイントがあります。まず、価格動向ですが、新年を迎えるにあたり、第1四半期は患者さんの自己負担額や免責額が通常通りリセットされることが予想されます。これらは、例年どおり、第1四半期の平均実現価格にマイナスの影響を及ぼします。
次に、これまで第4四半期に在庫が積み上がり、第1四半期に卸売業者による在庫の取り崩しが顕著であったことを思い出してください。当社は、第4四半期から第1四半期にかけて在庫の動きをより適切に管理するための新しいプロセスを導入しましたが、第1四半期には、前年同期と比較してより緩やかなレベルではありますが、在庫の取り崩しが発生すると予想しています。このことを踏まえ、当四半期のHIV/エイズの売上は、前四半期比で10%台前半の減少を見込んでい ます。これは、2022年第1四半期に報告した18%の前四半期比減少に比べます。
2023年通期については、22年のHIVの業績の一部は、平均実現価格に好影響を与えたチャネルミックスの変化によるものであり、2022年に報告した前年比5%の売上増に一部寄与していることを思い出していただきたいと思います。2023年のチャネルミックスは昨年と比較的類似しているため、2022年のような平均実現価格の変化からHIVの成長が恩恵を受けるとは考えていません。その結果、2023年のHIVの成長率は2022年よりも小幅に低下するものの、引き続き成長すると予想しています。HIV市場の将来について考えるとき、ギリアドは、HIVとともに生きる多くの人々やHIVのリスクを抱える人々に、ケアのための複数の選択肢を提供することができる立場にあります。
そのために、私たちは最近、米国と欧州で、多剤耐性HIV感染症で治療経験の多い成人に対するサンレンカの承認が得られたことに興奮しています。この最初の適応症は、HIVとともに生きる人々の1%から2%を占めるに過ぎず、膨大なアンメット・メディカル・ニーズが存在するのです。これらの人々は、複数の抗レトロウイルス剤レジメンを繰り返しており、これまで、有効な選択肢があったとしても、ごくわずかなものでした。
現在、「サンレンカ」は米国、英国、欧州の各市場で承認されており、さらに多くの国で「サンレンカ」を使用できるよう、規制当局や保険償還機関と可能な限り迅速に協働しているところです。この「サンレンカ」の最初の上市は、ギリアド社にとって重要なマイルストーンであり、HIVの治療と予防の可能性を展望するものであると考えています。サンレンカによって、真のアクティング・レジメンが現実のものとなりました。医療従事者、地域団体、HIV患者やそのリスクを抱える人々の間で、Sunlencaの6カ月ごとの皮下投与に対する認知度と親しみが高まるにつれ、Sunlencaは将来に向けて良いポジションにあると信じています。
スライド10のHCVに目を向けます。第4四半期の売上高は、米国矯正局(DOC)の購入時期や米国での有利な価格動向を反映して、前年同期比12%増の4億3900万ドルでした。前四半期比では、HCVの売上高は16%減でしたが、これは主に2022年の第3四半期に欧州で発生したリベート請求が解決し再発しなかったことと、米国でのその他の価格動向によるものですが、DOCの購入時期で一部相殺されています。今後、新規販売台数は引き続き減少すると見込んでいますが、当社の市場シェアは米国、欧州ともに50%超を維 持していることは心強いことです。
を維持しています。第4四半期のHPVとHDDの売上は、スライド11に記載の通り、2億5,500万ドルとなりました。売上高は前年同期比4%減、前四半期比では主に米国外の洗面台需要の減少や価格変動により3%減となりました。
第4四半期の売上高は10億ドル、通期では39億ドルでした。パンデミックの進展に伴い、COVID-19の治療におけるビクタビーの役割は、入院患者の標準治療の重要な部分として変わっていないことは明らかです。実際、ビクタビは現在でもこのような状況で承認された唯一の抗ウイルス剤です。そして、米国では、COVID-19の治療を受けている入院患者さんの50%以上にビクタビが使用され続けています。
経口ヌクレオシドであるCOVID-19については、まもなくMerdadから説明があると思いますが、引き続き取り組んでいきたいと考えています。オンコロジーに移り、Trodelvy のスライド 13 から始めます。第4四半期の売上高は1億9,500万ドルで、前年同期比65%増、前四半期比8%増となりました。通年では、トロデルヴィの売上は6億8,000万ドルで、前年比79%増となりました。
トロデルビへのアクセスを世界中で拡大し続ける中で、既存市場での需要の高まりに勇気づけられました。トロデルビィは現在、ヨーロッパの主要な市場で保険償還されています。また、米国では、前四半期比で13%需要が増加しました。また、米国では前四半期比13%増となり、拡大した営業体制と認知度の向上により、成長率は前四半期のほぼ2倍となりました。
また、今月末に予定されているFDAの決定により、前治療歴のあるHR陽性HER2陰性転移性乳がんにもTrodelvyの臨床的意義が拡大する可能性があり、私たちは期待しています。このことは、米国において少なくとも6,000人の患者さんが治療可能となることを意味し、当社の米国現地法人は、ちょうど発売記念会議を終えたところで、来る承認に向けて活気にあふれています。前治療歴のあるHR陽性HER2陰性転移性疾患の患者さんにとって、トロデルビが利益をもたらす機会は、TROPiCS-02のデータに基づくトロデルビのNCCNカテゴリー1優先推奨によって裏付けられています。
また、欧州医薬品庁は最近、HR陽性HER2陰性におけるTrodelvyの販売承認申請の妥当性を確認し、本年末の決定を期待しています。次にスライド14ですが、クリスティとカイトチームを代表して、第4四半期の細胞治療薬の売上高は4億1,900万ドルで、前年同期比75%増、前四半期比5%増となりました。通期の細胞治療薬の売上は15億ドルで、前年比68%増でした。第4四半期および通年の成長は、特に米国で大型B細胞リンパ腫におけるイースカルタの継続的な普及に牽引されたものです。
医師によるイースカルタのデータへの親近感の高まりと、カイト社の業界をリードする製造体制が引き続き主要な成長要因となっています。イースカルタの売上高は3億3700万ドルで、2021年第4四半期と比較して85%増、前四半期比では6%増となりました。米国におけるセカンドラインLBCLの力強いモメンタムだけでなく、サードラインLBCLの継続的な取り込みも、米国と欧州市場の両方で確認できたことは喜ばしいことです。
また、サードラインのLBCLも米国および欧州市場で継続的に増加しています。イェスカルタの第4四半期の売上は、マントル細胞リンパ腫と成人急性リンパ芽球性白血病の両方で数量需要が増加し、前四半期比2%増の8200万ドルでした。前年同期比では、テカルタの売上は44%増となりました。CAR-T細胞療法が治癒の可能性を持つ治療クラスとして勢いを増し、テカルタスが世界的に選択される主要な細胞療法としてスタートしたことを嬉しく思います。
カイトの業界をリードする信頼性の高い製造能力と、世界中に広がる認定治療センターのチームの足跡により、より多くの患者さんがアクセスできるようになってきています。そしてつい先週、英国の国立医療技術評価機構(NICE)は、大細胞型B細胞リンパ腫の3次治療薬としてイースカルタをルーティング使用することを推奨しました。これにより、イースカルタは英国で委託が可能な最初のCAR-Tとなりました。現在、米国やその他の市場で利用可能な追加適応症の承認と償還は、来年以降も継続される見込みです。
イースカルタは、米国以外で2番目に大きな細胞治療市場となる可能性を秘めた日本のLBCL二次治療薬として最近承認され、本年後半にギリアド社とカイト社に販売承認が移行することを期待しています。その間、まだ初期ではありますが、パートナーである第一三共と協力して、セカンドライン・プラスで約7,000人の患者さんにYescartaを提供できるよう取り組んでいきます。カイトは、カリフォルニア州エルセカンダの施設を通じて、日本市場向けの供給を開始します。それでは、Merdadからパイプラインの最新情報です。
メルダッド?
Merdad Parsey — チーフ・メディカル・オフィサー
ありがとう、ジョアンナ。トロデルヴィーやオンダネルマブのデータが良好で、レナカパビルも最近承認されたので、2023年以降にプログラムを進めることに、チームは本当に興奮しています。まず、スライド16のブラジからです。
今お話したように、レナカパビルは、他の抗レトロウイルス薬との併用で、多剤耐性HIV患者に対して初めて米国FDAの承認を取得しました。サンレンカで販売されているレナカパビルは、最初で唯一の年2回の皮下投与型HIV治療薬で、これまで代替薬が限られていた多剤耐性HIV患者さんにとって切望されていた選択肢をもたらすものです。欧州委員会からの承認と合わせ、FDAの承認は重要な検証であると同時に、当社が他のマノカテラーベースの治療および予防プログラムを継続的に進めていることを意味しています。
HIV治療については、現在、2つの新しいインテグラーゼ阻害剤、またはプレINDの領域での[聞き取れない]を含む、さまざまな開発段階にあるレナカパビルの10のパートナー薬剤を有しています。今年、2つのHIV中和抗体(bNAb)に対するレナカパビルのフェーズ1bの概念実証試験のデータを共有する予定です。また、PrEPでは、HIV予防のための単剤療法としてのレナカパビルの臨床開発が進行中で、2つの試験が進行中で、さらに2つの試験が2023年後半にFPIを達成する予定です。スライド17に移ります。
COVID-19用新規経口ヌクレオシドGS-5245は、引き続き進捗しています。ギリアド・ビクタビやワクチン接種などの治療により、COVID-19の患者さんの見通しは良くなっていますが、効果的で便利な経口治療の選択肢は依然として大きなニーズとなっています。私たちは、FDAをはじめとする世界の規制当局と協力し、グローバルな申請を可能にする臨床開発プログラムを立ち上げています。リスク要因が1つ以上あるワクチン未接種患者、またはリスク要因が2つ以上あるワクチン接種患者として定義される高リスク患者を対象としたフェーズ2 BIRCHtrialを開始しました。
第3相OAK TREAT試験では、CDCが定義する危険因子を持たない12歳以上の標準リスク患者を対象とします。この試験は、第1四半期に米国で最初の患者を登録する予定です。進捗は、試験実施施設付近でのCOVID-19の普及状況にもよりますが、可能な限りお伝えします。スライド18のオンコロジーに移り、Trodelvyから始めます。
TROPICS-02のデータの勢いが続いており、1月初旬には、前治療歴のあるHR陽性HER2陰性転移性乳がんに対する販売承認申請が欧州医薬品庁で承認されたことを発表しました。Johannaが述べたように、米国では今月末に、欧州では年後半にsBLAの承認が下りる見込みです。トロデルビは、すでに多くの転移性TNBCや進行性膀胱がんの患者さんの標準治療を変えてきました。
今回の承認は、HR陽性HER2陰性転移性乳がんの患者さんにとって、治療法を変える可能性のあるこの治療法を提供するための重要な一歩になると期待しています」と述べています。さらに、最近発表されたデータでは、TrodelvyのPFSおよびOSの効果は、腫瘍のTROP2発現量の範囲内で一貫していることが証明されています。このサンアントニオ乳がんシンポジウムで発表された画期的なポストホック解析は、ベースラインのTROP2発現が治療効果と関連しなかった転移性トリプルネガティブ乳がんにおけるTrodelvyのデータと一貫していました。スライド19に移ります。
当社は、12月にパートナーであるArcus社とARC-7試験の第4回中間解析のデータをASCOのプレナリーセッションで発表しました。ARC-7試験は、150名の患者さんを登録した無作為化第2相概念実証試験で、これまでに発表された抗TIGIT試験の中で最大のデータセットであり、2つのDOM含有群で100名以上の患者さんが登録されています。DOMを含む両群が、評価したすべての有効性指標においてZIM単剤療法と比較して臨床的に意味のある差別化を示し、この集団においてドンビニルマブの追加により抗PD-1療法に対する臨床反応が改善したことが明確に立証されたことを嬉しく思っています。また、DOMを含む治療群における安全性データが一貫しており、予期せぬ安全性シグナルを示さなかったことも心強く思っています。
本試験は進行中であり、ASCO 2023で最新のデータを共有できることを楽しみにしています。これらの有効性と安全性のデータは時間とともに成熟していきますが、この4回目の中間解析は、私たちの共同DOMの臨床開発プログラムおよびTIGIT経路を遮断することの重要性を完全に裏付けています」と述べています。今日までのデータを総合すると、Fcサイレント設計のDOMは、この分野の他の抗TIGIT分子と比較して差別化できる可能性があると、私たちは強く確信しています」と述べています。現在進行中の非小細胞肺がんを対象とした抗PD-1治療にDOMを追加する第3相試験は、この活性を確認する機会を提供するものです。
現在進行中の4つのフェーズ3試験を含む、コンセプト実証試験と後期試験の両方において、パートナーとともに非常に迅速に取り組んでいます。次に、抗CD47抗体治療薬、メグロリマブについてです。スライド20では、6つの固形腫瘍の適応症で、3つの進行中の主要試験と6つの概念実証試験が行われています。先月お伝えしたように、独立データモニタリング委員会が開催され、高リスクMDSのファーストラインにおけるEnhance試験の最初の中間解析のデータを検討しました。
新たな安全性シグナルは認められず、本試験は変更なく継続されることをお知らせします。注意事項として、FDAとのこれまでの議論に基づき、当社は現在、申請に向けて成熟したOSデータを追求しています。本試験はOSの最終解析のための検出力を有しており、試験の完全性を保つためにギリアド社はデータの盲検化を継続しています。この中間解析はイベントドリブンであるため、タイミングは暫定的なものであることに留意して、2回目の中間解析後、2023年後半に再度アップデートする予定です。
スライド 21 に移ります。クリスティとカイトチームを代表して、細胞治療プログラムの臨床的進展の詳細についてお知らせします。ASHにおいて、カイトは25以上のデータを発表し、細胞療法の変革的インパクトをさらに示しました。その中には、ZUMA-5の3年フォローアップデータがあり、Yescartaで治療した低悪性度リンパ腫患者の52%が引き続き反応していることが示されています。2021年のASHで共有されたフロントラインLBCLにおけるイースカルタの魅力的なZUMA-12データに続き、フロントライン高リスクLBCLを対象とした第3相試験ZUMA-23のFPI達成を今年前半に見込んでいます。
また、セカンドラインLBCLを対象とした第2相ZUMA-24外来試験も進行中で、今年前半に安全性の中間データを共有できることを期待しています。イースカルタとテカルタスにはまだ多くの探索が可能ですが、カイトが新しい適応症と次世代細胞治療技術でリーダーシップを発揮できるよう、パイプラインも構築しています。12月には、多発性骨髄腫の治療薬として評価中の後期臨床製品候補であるCAR-T-DDBCMAについて、当社のSelexと戦略的提携を行うことを発表しました。承認されれば、当社の業界をリードする製造能力とともに、患者さんが切望する治療を確実かつ安定的に提供できるものと考えています。
さらに、カイトにアーマードCAR Tプラットフォームと迅速な製造技術を追加するコミュニティ・セラピューティクス社の買収を発表しました(申請中)。Arcellxの買収は今週初めに完了し、Communityは今四半期末に完了する予定です。どちらもカイトの細胞治療における継続的なリーダーシップと、細胞治療における強固でエキサイティングなパイプラインの構築へのコミットメントを強調するものです。スライド22のまとめです。
2023年に期待されるパイプラインの主要なマイルストーンを共有しています。ご覧の通り、がん領域と泌尿器領域におけるFPI、データリードアウト、アップデート、規制当局の承認に及んでいます。これは、適応症とステージの多様性に富んだ59の臨床プログラムによって、ギリアドが変革の旅路を歩んできたことを浮き彫りにしています。臨床パイプラインが拡大するにつれ、私たちはその実行に重点を置くようになり、2023年までの進捗に応じて、私たちのプログラムについて皆様にご報告できることを楽しみにしています。それでは、アンディに電話をつなぎます。
アンディ?
アンディ・ディキンソン — 最高財務責任者
メルダッドさん、皆さん、こんにちは。ギリアドは、Biktarvy、Veklury、オンコロジーに牽引され、好調な第4四半期で年を締めくくることができました。通年では、Vekluryを除く当社の売上高は8%増となり、これはHCVの売上がピークを迎えた2015年以降、ギリアドが報告した通年の成長率としては断トツの強さです。特筆すべきは、AtriplaとTruvadaのLOEの影響を除くと、HIVは前年比8%増で、2021年から20%増の104億ドルとなったBiktarvyの好調が続いていることに牽引されていることです。
Biktarvy は、2023 年以降もさらなる成長のための強い可能性を示し続けています。オンコロジー通期売上は初めて20億ドルを超え、2021年比71%増となりました。スライド24から始まる四半期業績に移ります。第4四半期も、当社の事業全体で力強い業績が示されました。
Vekluryを除く製品売上高は、FXによる約1億3,000万ドルの逆風にもかかわらず、前年同期比9%増となりました。HIV LOEの影響に加え、為替を除外すると、第4四半期の基礎的な売上高の伸びは前年同期比12%となります。スライド25に移ります。ベクルーリーは、予想通り前年同期比で減少しましたが、前四半期比では8%増となり、COVID-19が流行期に入ったとしても、ベクルーリーが引き続き重要な役割を果たすことが浮き彫りになりました。
非GAAPベースの製品売上総利益率は86.8%で、主に2021年第4四半期に売上原価に計上された訴訟和解に関連する12億5000万ドルの費用により、前年から16ポイント以上増加しました。2022年第4四半期の非GAAPベースの研究開発費は、2021年同期の13億ドルに対し、15億ドルでした。研究開発費の増加は、費用に対するインフレの影響に加え、主にオンコロジーにおける臨床投資のタイミングによるものです。第4四半期の獲得IP研究開発は、主にマクロジェニックス社との提携とジャウンス社とのライセンス改正を反映して1億5800万ドル、2021年第4四半期のArcus資産のオプトイン権行使に関連する6億2500万ドルの費用により前年を下回る結果となりました。
非GAAPベースの販管費は20億ドルで、前年比23%増となりましたが、これは主にEverest MedicinesとのTrodelvy共同研究の終了に伴う費用4億600万ドルを反映したものです。この4億600万ドルの費用には、中国およびその他のアジア地域におけるトロデルヴィの開発・販売権を取得するためにエベレストに支払うことで合意した2億8,000万ドルに加え、その他の提携解消関連費用が含まれています。このエベレストの影響を除くと、販売管理費は前年同期比2%減でした。第4四半期の非GAAPベースの営業利益率は37%で、エベレスト社の費用4億600万ドルを含む前述の要因によって前四半期比で低下し、前年同期比では上昇しました。
エベレスト社の費用を除くと、非GAAPベースの営業利益率は42%でした。第4四半期の非GAAPベースの実効税率は、2021年第4四半期に計上された個別の税金費用により、前年同期を下回る16.8%となりました。全体として、当社の非GAAPベースの希薄化後1株当たり利益は、2021年第4四半期の0.69ドルに対し、第4四半期は1.67ドルとなりました。特筆すべきは、エベレストの契約終了が非GAAPベースの希薄化後1株当たり0.25ドルの影響を与えたことです。
これは10月に発表したガイダンスには反映されていません。スライド26では、通期についてご説明します。製品の総売上高は270億ドルでした。Vekluryを除くと、製品総売上は231億ドルで、主にBiktarvyとオンコロジーが牽引し、2021年比で8%増となりました。
約3億8000万ドルの為替逆風と、トゥルバダとアトリプラのLOEの影響3億5000万ドルを除いた製品売上高は、2021年比で11%増となりました。概要で主な損益影響に触れましたが、2022年の非GAAPベースの実効税率が19.3%、非GAAPベースの希薄化後EPSが2021年の1株当たり7.18ドルの報告に対して7.26ドルだったことをスライド27で強調します。次に、スライド28のガイダンスに移ります。マクロ環境は引き続き不透明であると認識しています。
2023年のガイダンスでは、マクロ環境は全体的に安定し、為替も現在のレートで比較的安定していることを想定しています。インフレは緩やかになると予想していますが、2023年のガイダンスでは、2022年に経験したインフレに伴う費用の増加を通年で見込んでいます。この点を踏まえ、製品売上高は、260億ドルから265億ドルの範囲になると予想しています。Vekluryを除く製品売上高全体では、240億ドルから245億ドルの範囲を見込んでおり、これはベースビジネスが前年比4%から6%の成長であることを示しています。
そして、Biktarvyの売上は約20億ドルを見込んでいます。ビクタービーの売上は、これまでと同様、入院患者数に連動しており、急増の頻度や程度によって大きく変動することが予想されます。注目すべきは、ここ数週間、入院率が低下していることで、今後も注意深く状況を観察していきます。その結果、昨年と同様、ビクタービーについては、四半期ごとに予想を更新していきます。
残りの損益に移ります。非GAAPベースの製品売上総利益率は、2022年の実績をわずかに下回り、主にオンコロジーからの寄与の増加を反映して、約86%になると予想しています。非GAAPベースの営業費用については、成長戦略分野への継続的な投資と後期臨床試験による活動の増加を反映し、研究開発は2022年の水準と比較して1桁台後半の割合で増加するものと予想しています。ちなみに、2022年には8本の第3相臨床試験が開始され、2023年末には23本の有効な第3相臨床試験が実施される予定です。
今後は、臨床データに基づく有望なプログラムをサポートするために、必要に応じて投資を強化するものの、研究開発の伸びは緩やかになると予想しています。買収したIPの研究開発費には、既に発表したPhenexコミュニティに対する支払いや、既存の共同研究に対するマイルストーン支払いが含まれます。2022年のアプローチと同様に、追加の取引を発表した際にも、予想される買収IP研究開発費を分担していきます。最後に、販売管理費は2022年比で一桁台前半の減少を見込んでいます。
ただし、これは主に2022年に計上された費用のうち、2023年には繰り返さないと思われるものがあるためです。2022年の販管費をこれらの項目で正規化すると、2023年通期の販管費は、2022年の約51億ドルを基準に一桁台半ばの割合で増加すると予想しています。合わせて、2023 年度の非 GAAP 型営業利益は 110 億ドルから 116 億ドルになると予想しています。非 GAAP 型の実効税率は、今年も約 20%となる見込みです。
最後に、通期の非GAAPベースの希薄化後1株当たり利益は6.60ドルから7ドル、GAAPベースの希薄化後1株当たり利益は5.30ドルから5.70ドルになると予想しています。スライド29の資本配分に移ります。私たちの優先順位は変わっていません。2022年、私たちは50億ドル以上を株主に還元しました。
これには配当金の支払いや14億ドルの自社株買いが含まれています。第4四半期の自社株買いは約8億ドルでした。2023年については、本日、四半期ごとに現金配当を2.7%増やし、1株当たり0.75ドルとすることを発表しました。また、厳選されたパートナーシップや事業開発取引を通じて、社内外において当社のビジネスに対する賢明な投資を継続することを期待しています。
さらに、株式の希薄化を抑制するために自社株買いを継続するとともに、機動的な追加取得を行います。それでは、オペレーターから質問をお受けします。
質疑応答
オペレーター
確かに。[ご質問を承りましたので、ここで一時停止させていただきます。最初の質問はコーウェンのタイラー・ヴァン・ビューレンからです。どうぞよろしくお願いします。
タイラー・ヴァン・ビューレン — コーウェン・アンド・カンパニー — アナリスト
やあ、みんな。質問をありがとうございます。今期もコアビジネスの素晴らしい業績を見ることができ、大変うれしく思います。中間報告では、Vekluryを除く製品売上高が前年同期比5%増とされていますが、非GAAPベースのEPSガイダンスでは6%の減少を想定しています。
パイプラインへの積極的な投資を継続し、10年後半に向けた収益拡大を図るため、今後2~3年間はほぼ横ばいの収益を見込んでよいのでしょうか?それとも、それはあまりに保守的でしょうか?また、近い将来および中期的に収益を増加させるために、どのような手段があるのでしょうか?
アンディ・ディキンソン — 最高財務責任者
タイラー、アンディです。ご質問ありがとうございます。ありがとうございます。これまで述べてきたように、長期的なガイダンスは提供しませんが、改めて申し上げますと、ご指摘のとおり、ベースビジネスは非常に好調に推移しています。
Vekluryは今年も好調でしたが、COVID-19の市場は今後もダイナミックに推移すると予想しています。今年もまた、EPSを見ると、経費の増加にもかかわらず、ベースビジネスの成長がVekluryの減少を補っています。今後も、多くの株主が、ご存知のように、仮定に基づくVekluryを除く非GAAPベースのEPSに注目しています。私たちは、このような指標を用いてEPSが成長し、その成長が長期的に加速することを期待しています。これは、当社の製品が商業的承認の追加や適応症の拡大、新製品の市場投入など、成果を上げ続けるためです。
また、Vekluryの影響を考慮することの難しさを強調されているように思います。ベースとなる事業を見ると、事業の健全性と、トップラインとボトムラインの両方で長期的にもたらされる成長という点で、私たちは大きな確信を持っています。
ジャッキー・ロス — インベスター・リレーションズ担当副社長
ハンナさん、次の質問をお願いします。
オペレーター
次の質問はバンク・オブ・アメリカのジェフ・ミーチャムからです。続けてください。
ジェフ・ミーチャム — バンクオブアメリカ・メリルリンチ — アナリスト
こんにちは、皆さん。質問をありがとうございます。質問は1つだけにしておきます。米国でのレナカパビルについて、最近の承認後の予想される損失ダイナミクスと、支払者のアクセスに関するハードルを考慮して教えてください。
また、貴社は長い歴史をお持ちですが、パンデミック前と現在では環境が異なるのでしょうか?ありがとうございました。
Johanna Mercier — チーフ・コマーシャル・オフィサー
Geoffさん、ご質問ありがとうございます。ジョアンナです。サンレンカの承認には、とても期待しています。しかし、これは非常に特殊な患者集団が対象であり、治療経験の多い多剤耐性集団が対象です。
HIVに感染していない人の約1%から2%が該当します。つまり、米国では約5,000人の患者がいることになります。ですから、このパズルの1ピースについて、少し考えてみてください。今のところ、私たちは発売したばかりです。
まだ始まったばかりですが、私たちはこの製品にとても期待しています。医師からの反応も非常に強いと思います。半年に一度、何かが届くという革新性と、予防の適応や治療の組み合わせなど、将来的な可能性を見据えているのでしょう。
この点については、まだまだこれからです。サンレンカの認知度を高め、診療報酬制度に活用するための素晴らしい機会だと思います。また、COVID以前からCOVIDへの移行についてのご指摘ですが、実は、市場は本当に正常化したと思っています。HIVに関しては、スクリーニング、診断、治療ともに軌道に乗ったと思います。
ですから、2023年に向けては、おそらくそのようなことはないと考えています。しかし、繰り返しになりますが、収益は小さく、アンメット・メディカル・ニーズは非常に大きく、患者にとっては、HIV陽性であることよりもエイズに近い状態にならないようにするための何かを手に入れる素晴らしい機会なのです。
ジャッキー・ロス — インベスター・リレーションズ担当副社長
ハンナさん、次の質問をお願いします。
オペレーター
ありがとうございます。次はジェフリーズのマイケル・イーからです。どうぞよろしくお願いします。
マイケル・イー — ジェフリーズ — アナリスト
質問をありがとうございます。Merdadにも質問があるかもしれません。Trop-2について、競合のアストラゼネカ第一はかなり強気で、実際、肺がんフェーズ3試験の結果も出ており、ストリートはTrop-2に対してかなり強気になっています。差別化についてのお考えをお聞かせください。研究結果を評価し、そこでどのように競争するか、あるいは差別化するか、またその安全性について評価すべきと思いますが、そのあたりを説明して、競合品に対するTrop-2の理解を深めるのに役立つと思います。
ありがとうございました。
Merdad Parsey — チーフメディカルオフィサー
そうですね。ありがとう、マイケル。こちらはメルダド。おっしゃるとおりです。
差別化について考えるとき、私たちは2つのことを考える必要があります。1つ目は、「Trodelvy」については、すでに市販され、いくつかの承認を得ています。これは、重要な適応症で上市されていることの重要な要素だと思います。ご指摘のとおり、肺がんについては、競合他社にやや遅れをとることになるでしょう。
これまでのところ、幸運なことに、当社の開発プログラムではILDは見つかっていません。ですから、これからも積極的にプログラムを進めていくつもりです。これまで多くの成功を収めてきましたので、今後も差別化された臨床開発プログラムを進め、できるだけ多くの人々に投与できるようにしていきたいと考えています。
オペレーター
ありがとうございました。次の質問は、Piper SandlerのGuyn Kimです。どうぞよろしくお願いします。
Guyn Kim — Piper Sandler — アナリスト
私の質問を聞いてくださってありがとうございます。Trodelvyを使い続けています。Merdad、今年後半に開始する化学療法前のHR陽性、HER2陰性乳がんについてもう少し詳しく教えていただければと思います。
その試験デザインはどのようなものでしょうか?また、この集団にとってこれが次善の研究であるという結論に至った経緯は?
Merdad Parsey — チーフメディカルオフィサー
はい。ありがとうございます。素晴らしい質問ですね。私たちはまだデザインについて話したことがないと思います。
その患者集団においてどのようなアプローチがベストなのか、治験責任医師や規制当局の方々と一緒になって考えているところです。私たちは、このような大規模な集団には重要なニーズがあると考えています。そして、その道筋を慎重に進めたいと考えています。ですから、プロトコルの開発とともにプログラムを発展させれば、より詳細な情報を共有できるようになると思います。
ジャッキー・ロス — インベスター・リレーションズ担当副社長
ハンナさん、次の質問をお願いします。
オペレーター
ありがとうございます。次の質問はUBSのコリン・ブリストウからです。続けてください。
コリン・ブリストウ — UBS — アナリスト
はい。こんにちは、そしてすべての進展におめでとうございます。TIGITとdompenanumabについて一つ。少なくとも動物実験では、Fcサイレント・コンストラクトは好ましくないことが示唆されていますが、何が正しいアプローチであると確信させるのでしょうか?次に、ARC-7の試験についてお聞かせください。
比較試験とスキャンの頻度に関して、少なくとも議論されてきた点なので、スキャンの頻度について話していただけますか?
Merdad Parsey — チーフメディカルオフィサー
はい、またMerdadです。素晴らしい質問です。ありがとうございました。
私たちの自信という点では、ご指摘の通り、数年前にも多くの議論があったと思います。私たちは、前臨床データが示していることを、その議論の中で共有しました。ご存知のように、前臨床データには相反するものがあり、NFCサイレントが効かない可能性を示唆するデータもありました。しかし、だからこそ、私たちはこのような方法で研究を行い、また非常に重要なことですが、なぜARC-7を実施したかというと、NFCサイレントがNFC活性分子と比較して有効かどうかを立証することが目的でした。
仮説の1つは、末梢で何が起こっているのか、TIGITでエフェクター細胞を枯渇させると、NFC非分子に比べてNFC活性分子が有害なのかどうかということです。そして、その確信はARC-7のデータから得たものです。ARC-7のデータは、その疑問に答えるものだと思います。
PFSのデータは、私たちが前進するためのハードルを超えています。FCが重要かどうかという臨床上の疑問に対して、私たちは本当に答えを出したと考えています。
オペレーター
ありがとうございます。次の質問は、JPMorganのChris Schottからです。どうぞよろしくお願いします。
Chris Schott — JPモルガン・チェース・アンド・カンパニー — アナリスト
素晴らしい。ありがとうございます。COVIDビジネスについて質問です。COVIDビジネスが不安定であることは承知していますが、同時に、ストリートはVekluryやGS-5245の今年以降の数字にあまり尾を引くモデルを描いていないように思います。
ファイザーなどは、2023年以降に持続可能なCOVIDビジネスについて話しています。そこで、この事業を長期的にどのように考えているのか、あなたの考えが知りたいのです。また、この事業は長期的にみて重要なフランチャイズなのでしょうか?それとも、今年以降もフェードアウトしていくとお考えでしょうか?ありがとうございました。
Johanna Mercier — チーフ・コマーシャル・オフィサー
もちろんです、クリス。ヨハンナです。ヨハンナです。確かに、私たちは少し変わりました。
この件に関する我々の立場は、2020年から今日に至るまで明らかに進化してきました。ベクルーリーの事業は、これまで見たこともないほど持続可能であると確信していますし、ましてやCOVID-19の方向性については、Merdadが話してくれたような経口投与も含めて、考えています。1つは、2020年10月からVekluryが商業モデルの一部になっていることです。そのため、他の企業が経験したような政府レベルでの大きな在庫の底打ちはありません。
ですから、2022年の収益のおそらく85%から90%は、2022年のVekluryに対する需要を真に反映しているのです。したがって、2023年に向けては、Vekluryは現時点でも病院レベルで適応される唯一の抗ウイルス剤であり、世界中の多くの国で、入院患者の治療を決定する際に選択される治療法であるため、非常に強く感じています。Vekluryがすべての患者さんにとって利用しやすいものであることを確認することは、私たちにとって非常に重要な機会だと考えています。そのため、このモデルは今後も持続可能だと考えています。
私たちは、死亡率を含む非常に強力なエビデンスを有していますし、NIHやWHOのガイドラインに承認されています。ですから、これらの要素がすべて揃えば、23年以降もVekluryの強力なカラー・ポジションを確立することができます。それでは、Merdadに代わって、COVID-19について、全体としてどのように考えているか、経口投与について少しお話ししてもらいましょう。
Merdad Parsey — チーフメディカルオフィサー
はい。2秒だけ。私たち全員が持っている不確実性や、外来患者のCOVIDで見てきたことを指摘するのは正しいと思います。5245の作用機序については、分子そのものに関する我々の専門知識と、それがいかにうまく機能しているかを考慮すれば、大きな自信を持っています。
そして、ハイリスクとスタンダードリスクの両方の試験を推進し、ベストを尽くすつもりですが、パンデミックという不確実な要素が、ここから先の展開を決定します。ですから、今後どうなっていくのか、ぜひ最新情報をお伝えしていきたいと思います。
オペレーター
ありがとうございます。次の質問は、RBCのBrian Abrahamsです。どうぞよろしくお願いします。
Brian Abrahams — RBC Capital Markets — アナリスト
こんにちは、四半期決算おめでとうございます。そして、私の質問にお答えいただきありがとうございます。5245のCOVIDのテーマ、Oaktreeの研究の続きですね。標準リスク患者に対する主要評価項目を設定する際の前提条件について、もう少し詳しく教えてください。また、OaktreeとBirchがどのように組み合わされ、米国および米国外の承認をサポートすることができるのか、ご理解をお願いします。
また、オークツリーとバーチがどのように組み合わされ、あなたが研究している2つの集団の米国および米国外での承認をサポートするのか、教えてください。ありがとうございました。
Merdad Parsey — チーフ・メディカル・オフィサー
もちろんです。非常に簡潔に言うと、ご指摘の通り、1つはハイリスク集団ですね?これは重要なことだと思います。ワクチン接種の有無にかかわらず、危険因子を持つ人たちと、危険因子を持たない標準的な人たちです。これらは非常に異なる集団です。
ハイリスクでは、入院などを予防できるかどうかを調べます。そして、標準的なリスクでは、症状の改善などを見ることになるでしょう。繰り返しになりますが、これらの要因には不確実性があり、重要なことは、根本的なイベント発生率が現実的であるということです。そのため、背景となる事象の発生率について、いくつかの仮定を立てています。
そして、その仮定が正しいかどうかを確認するためのチェックポイントを試験に組み込んでいます。そして、基礎となる事象の発生率に基づいて、プログラムを修正する能力も持っています。このように、リスクと不確実性を軽減することができます。ですから、私たちはこの点に関してかなりオープンな姿勢で臨んでいます。
オペレーター
ありがとうございました。次の質問は、ウェルズ・ファーゴのモヒット・バンサルです。続けてください。
Mohit Bansal — Wells Fargo Securities — アナリスト
素晴らしい 私の質問を受けてくださってありがとうございます。進展におめでとうございます。HIVの分野での全体的な市場シェアと、その進捗状況についてコメントいただけますか。
私が理解したいのは、現時点でのシェア拡大により、御社の事業全体の成長が市場の成長よりも高くなるようなシナリオがあるのかということです。ありがとうございました。
Johanna Mercier — チーフ・コマーシャル・オフィサー
こんにちは、Mohit。Johannaです。HIV全体として見ると、前年比5%程度の成長と見ています。
もちろん、これはほとんど需要、つまりBiktarvyによってもたらされています。ですから、そこでのシェアについてお話することが重要でしょう。ギリアドのシェアは70%台前半で、この水準ではかなり安定しています。TruvadaとAtriplaのLOEを取得したときに少し落ち込みましたが、それ以外は安定しています。
Biktarvyの対前年成長率は、発売後50年間で20%です。これが、HIVビジネス全体を牽引するパズルのピースだと思います。さらに、PrEPではDescovyで何が起こっているのでしょうか?市場成長についてのご指摘ですが、米国でも欧州でも、市場の成長は前年比2~3%程度であり、今後数年間はそのような状況を想定しています。そして、この市場には、継続的な成長のための大きな機会がまだあると思います。
その主な理由の1つは、診断から治療までの治療率を高める機会がまだあることと、十分な治療を受けていない患者層への浸透をさらに進めることができることです。現時点では、国連の検査、治療、ウイルス学的抑制の目標が95,95,95であるのに対し、私たちは70%から75%程度にとどまっているのが現状です。ですから、この目標を達成するためには、さらに35万人以上の患者をシステムに取り込む必要があります。ですから、おっしゃるとおりだと思います。
ビクタービーとギリアドのHIV事業を継続的に成長させる大きな機会があると思います。
オペレーター
ありがとうございます。次の質問は、EvercoreのUmer Raffatからです。どうぞよろしくお願いします。
Umer Raffat — Evercore ISI — アナリスト
こんにちは、皆さん。今日はモデルについて質問させてください。コンセンサスモデルでは、Gileadの長期予測に営業レバレッジが多く含まれているように感じます。コンセンサスは、販管費と研究開発費で1桁台前半の成長しか見込んでいません。
販売管理費は一過性のものを除いて今年一桁台半ばの成長で、研究開発費は一桁台後半の成長ですが、すべての提携や最近の買収を考慮すると、研究開発を現在のレベルから大幅に成長させる必要があると考えるべきでしょうか?私は、OPEXが長期的にどのような方向に向かっているのかを理解しようとしているのです。
アンディ・ディキンソン(Andy Dickinson) — 最高財務責任者
オマル、アンディです。ご質問ありがとうございます。まず、ご期待どおり、私たちは経費に留意しており、研究開発費や販売管理費が無制限に増加するとは考えていないことを強調したいと思います。
しかし、パイプラインへの慎重な投資を続け、その具体的な効果はすでにご覧いただいていると思います。これは本当に重要なポイントです。私たちは研究開発の側面からスタートしました。ご存知のように、今年は8つのフェーズ3試験を開始しました。
2023年には少なくとももう5つの試験を開始する予定です。つまり、私たちは投資サイクルの中にいるのです。もうひとつ、長期的な展望をお話する前に、競合他社と比較した場合の話ですが、ご存知のように、歴史的に見ると、販売管理費と研究開発費の両方が過小でした。そのため、当社が目指している4分の1クラスの持続的成長を推進するためのパイプラインがなく、現在ではその達成に向けた軌道に乗っていると考えています。
ですから、私たちはこれからも投資を続けていくつもりです。ご承知の通り、特に後期第3相臨床試験を開始しましたが、パイプラインを再構築してきた過去4、5年のようなペースやレベルではなく、引き続きBDに取り組んでいきます。しかし、昨年度の売上高に対する研究開発費の比率は、業界平均を下回る19%程度だったと思います。売上高に対する販売管理費の割合も同様です。
また、当社のガイドによると、コンプに対して妥当な支出水準であると思われます。より長い目で見れば、ご指摘のように、私たちはより長いサイクルで物事を考えていますので、研究開発や販管費が利益の伸び率以上に伸びることはないと考えています。また、このモデルには多くのレバレッジがあり、長期的にはそれを見込んでいます。そして、今後数年間は、ボトムラインにもそれが反映されると考えています。
ご質問をありがとうございました。
運営担当者
ありがとうございました。次の質問は、カントール・フィッツジェラルドのオリビア・ブレイヤーからです。どうぞよろしくお願いします。
オリビア・ブレイヤー — カントール・フィッツジェラルド — アナリスト
こんにちは、皆さん。質問をありがとうございます。マグロリマブの規制当局への対応について、最新の見解はいかがでしょうか?質問としては、今年の後半にEnhance interimから生存データを見ることができるのか、申請できるほど成熟しているのか、ということです。また、FDAが完全な申請パッケージのために指摘したOSの利点以上のものはありますか?ありがとうございました。
Merdad Parsey — 最高医学責任者
こんにちは、オリビア。メルダドです はい。一歩下がって、私たちの研究の中間解析への取り組み方を明確にしたほうがいいかもしれませんね。
つまり、ピボタル・マクロ試験は、最終解析時のイベントに対して動力を与えています。もちろん、安全性などを評価するために、業界の標準に従って中間解析を行いますが、主要評価項目で劇的な改善が見られる場合に備えて、アルファ値を少し使い、早期に開始して患者さんに利益をもたらす機会も提供しています。ですから、OSデータは引き続き成熟しています。今年の次の中間解析は、もちろんイベント次第ですが、最終的な解析ではありません。
OSの改善度合いがどの程度かによって、試験の中止や盲検化の解除につながるかどうかが決まります。私たちが期待しているのは、OSの最終解析に進むことです。もちろん、それ以前の中間解析でサプライズがあることを常に願っています。それから、承認に関しては、OSが本当に必要だと思います。
私たちは当初、例えばCR率だけで早期承認が得られると期待していました。完全奏効率だけでなく、OSのデータも必要だと考えています。
オペレーター
ありがとうございました。次の質問は、RedburnのSimon Bakerからです。どうぞよろしくお願いします。
Simon Baker — Redburn Partners — アナリスト
NICEの推奨についてありがとうございます。NICEの勧告は、英国の観点からは良いことですが、より多くの国々で密接にフォローされているのが実情です。しかし、NICEの勧告は、より多くの国々で支持されています。
ということです。今回の承認は、英国でどの程度重要なのでしょうか?
クリスティ・ショー — カイト社最高経営責任者
こんにちは、サイモン。クリスティです。ご質問をありがとうございます。まず、患者数は450人と非常に少ないのですが、患者さんが承認されるまでのプロセスは明らかにもっとスムーズであるべきで、患者さんがより早くアクセスできるようにするために、この勧告は非常に重要だと考えています。
また、ご指摘の通り、この承認が他の国にも影響を与えることを期待しています。例えば、20カ国以上でのYescartaの償還を見ると、1つずつ償還が進んでいることがわかります。そして、ある国では改善され始めています。そして、ある国が改善し始めると、他の通貨も同じように改善することがわかりました。ですから、セカンドラインのZUMA-7試験も踏まえて、次のステップとして、患者さんに1回限りの治療を提供することが医療制度を本当に助け、患者さんの転帰を改善するというデータを提供し続けるつもりです。
そう、私たちは、この試験が何らかの影響を与えることを強く期待しているのです。
運営担当者
ありがとうございました。次の質問は、TruistのRobyn Karnauskasからです。続けてください。
Nicole Germino — Truist Securities — アナリスト
こんにちは、そして私たちの質問に答えてくれてありがとう。ロビンに代わってニコルです。Trodelvyとpembroのレベル3について、ある意味での安全性のシグナルは出ていますか?安全性プローブは両方の集団に匹敵するようなものですか?もしそうであれば、ファーストラインでの導入に支障をきたすのでしょうか?
Merdad Parsey — 最高医学責任者
ニコルさん、こんにちは。Merdadです。安全性については、まだ何も公表していません。これらの研究は、本当に始まったばかりです。
ですから、まだ何もお伝えすることはないと思います。もちろん、何か出てくるかどうか、追っていきますよ。あなたのご質問は、まさに私たちが前進する中で確実に対処していきたいものです。しかし、現時点ではまだ十分なデータがなく、どちらか一方にしかコメントできません。
オペレーター
ありがとうございました。最後の質問は、BMOのEvan Seigermanからです。どうぞよろしくお願いします。
エヴァン・セイガーマン — BMOキャピタルマーケッツ — アナリスト
どうも、皆さん。私の質問に答えてくれてありがとう。クリスティに一つ。細胞治療製品で年商10億ドルを大きく超えていますね。
製造業を拡大するために最近行った作業と、それが今年以降のさらなる成長をどのように支えることができるとお考えか、お話しいただけますか?ありがとうございました。
クリスティ・ショー — カイト社最高経営責任者
もちろんです。ですから、私たちの焦点は供給サイドにあり、患者さんに提供する能力を確保することにあります。これが、業界をリードする当社の製造部門をご覧いただいている理由だと思います。カリフォルニアのGCFO3、アムステルダムのTCFO-4、メリーランドのTCFO-5を見れば、現在ある資産だけでなく、将来のパイプライン、特に骨髄腫との提携のために、その足跡を活用することができるのです。
ですから、私たちは、現在および将来の供給能力と、これまでに構築したキャパシティに非常に自信を持っています。そして、次の焦点は、マージンの改善で本当に良い成果を上げていることです。しかし、製造拠点の最適化については、今後も継続していく必要があります。そうですね、生産能力を確保し続ける必要がありますが、これは本当にできたと思っています。
そして、最適化の部分にも大きな焦点を当てることができるようになり、これは進展していますが、さらにいくつかのレバーを引く必要があります。ですから、患者さんに提供する能力という点で、大きな自信を感じていただければと思います。
運営担当者
ありがとうございました。以上で本日の質疑応答は終了です。では、最後に経営陣からご挨拶をお願いします。
ダン・オデイ — 会長兼最高経営責任者(CEO
素晴らしい。ダンです。ここで2、3のことをお話ししたいと思います。まず最初に、ご参加いただいた皆様、そしてギリアドに継続的な関心とご質問をいただいた皆様に感謝いたします。
いつも通り、ご質問にお答えしきれなかった場合は、インベスター・リレーションズまでご連絡をお願いします。ご存知のように、私たちは喜んで継続的にご質問にお答えします。さて、最後に、ギリアドは、チームが会社の変革に取り組んできたおかげで、数年前とはまったく異なる場所にいることを強調して、私の話を終わらせていただきます。2023年に向けては、現在の医薬品が順調に推移し、神経治療薬や開発中の医薬品にも大きな成長の可能性があるため、非常に強い態勢で臨むことができます。
今後、前四半期に引き続き、より迅速な実行と、より大きなインパクトが期待できます。本日はお時間をいただきありがとうございました。
以上です。他の翻訳希望やご感想をいただけると嬉しいです。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>


