モデルナ (MRNA)2023年第2四半期決算説明会の日本語訳です。
COVID-19ワクチン頼みなので売上が前年比94%減と酷いですね。予想よりも良かったですがこのままでは厳しいと思われます。
インフルエンザやがん領域での新薬が上市されれば状況は一気に状況は変わりそうなのでしばらくは注目していきます。
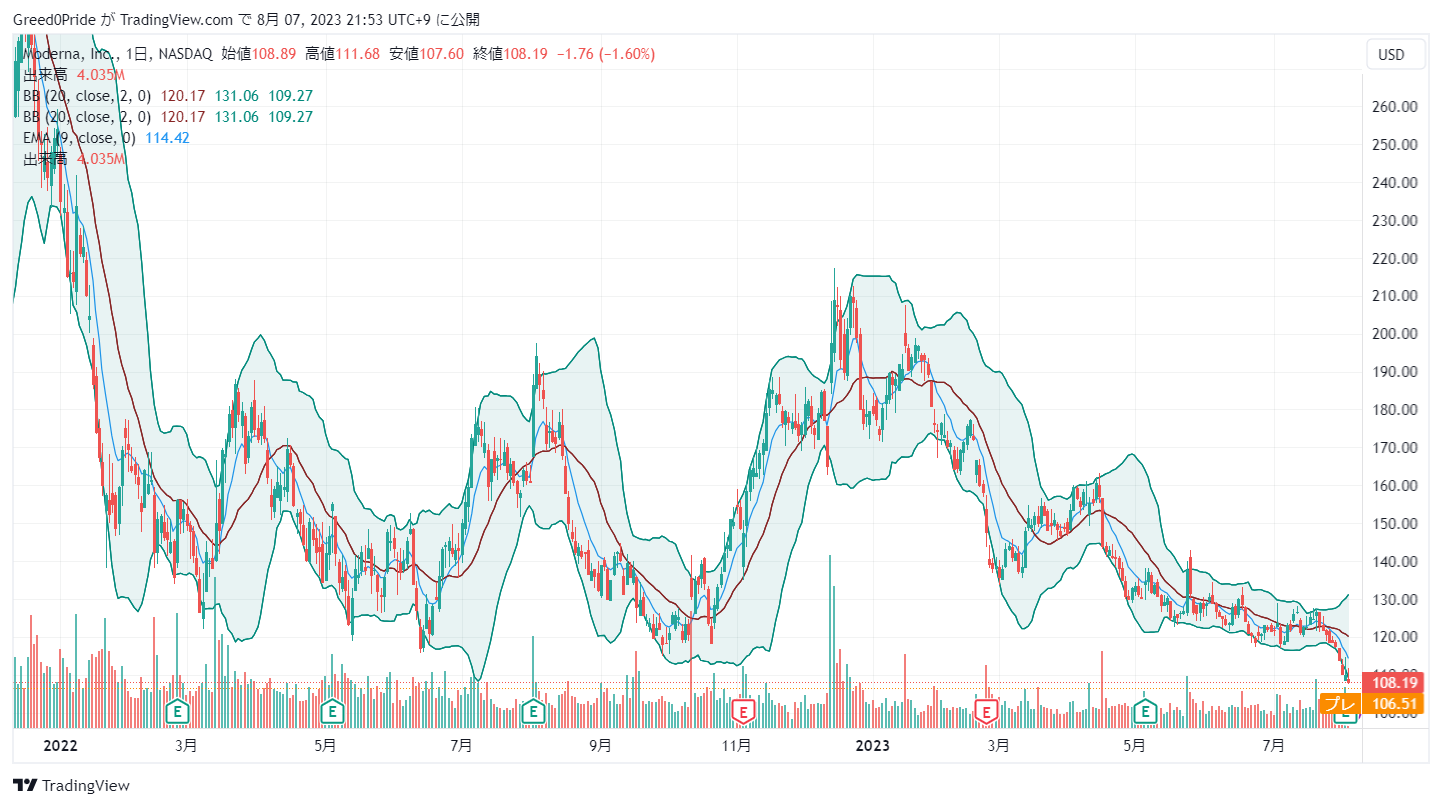
モデルナ (MRNA)株価
モデルナ (MRNA)2023年第2四半期決算説明会
Call participants:
Lavina Talukdar — Head of Investor Relations
Stéphane Bancel — Chief Executive Officer
Stephen Hoge — President
Arpa Garay — Chief Commercial Officer
Jamie Mock — Chief Financial Officer
Salveen Richter — Goldman Sachs — Analyst
Tyler Van Buren — TD Cowen — Analyst
Gena Wang — Barclays — Analyst
Dina Elmonshed — Jefferies — Analyst
Unknown speaker
Luca Issi — RBC Capital Markets — Analyst
Edward Tenthoff — Piper Sandler — Analyst
Manos Papadakis — Deutsche Bank — Analyst
Alex Hammond — Bank of America Merrill Lynch — Analyst
Evan Wang — Guggenheim Partners — Analyst
Simon Baker — Redburn Partners — Analyst
More MRNA analysis
2023年8月3日午前8時00分(米国東部時間)
オペレーター
こんにちは、お待たせいたしました。モデルナの2023年第2四半期電話会議にようこそ。[本日の電話会議は録音されております。それでは、本日のスピーカー、IR部長のラヴィナ・タルクダーさんにお願いしたいと思います。
どうぞ。
ラヴィーナ・タルクダー — IR部長
ありがとう、ケビン。皆さん、おはようございます。本日は、Modernaの2023年第2四半期決算と事業アップデートに関する電話会議にご参加いただき、ありがとうございます。今朝発表したプレスリリースと、これからご覧いただくスライドは、当社ウェブサイトの投資家向けセクションからご覧いただけます。本日の電話会議には、最高経営責任者のステファン・バンセル、社長のスティーブン・ホーゲ、最高商業責任者のアルパ・ガライ、最高財務責任者のジェイミー・モックが出席します。
この電話会議では、1995年米国私募証券訴訟改革法のセーフハーバー条項に基づき、将来の見通しに関する記述が含まれていることにご留意ください。当社の実際の業績や結果が、これらの将来見通しに関する記述に明示的または黙示的に示されたものと大きく異なる原因となりうる重要なリスク要因については、添付プレゼンテーションのスライド2および当社のSEC提出書類をご覧ください。それでは、ステファンに電話を回します。
ステファン・バンセル — 最高経営責任者
ありがとう、ラヴィーナ。おはようございます。本日はまず、第2四半期のビジネスレビューから始めさせていただきます。その後、アルパが商業的な進捗状況と計画について最新情報をお伝えする前に、ステファンが臨床プログラムについてレビューします。
その後、ジェイミーが決算を発表し、私が最後に感想を述べます。第2四半期は、流行性の呼吸器系ワクチンの季節性を反映し、約3億ドルの売上を計上しました。フェーズ3段階にある4つの感染症ワクチンプログラムと、同じくフェーズ3段階にあるがん領域プログラムへの投資を考慮すると、このオフシーズン四半期の売上高は、GAAPベースの純損失14億ドル、GAAPベースの希薄化後1株当たり損失3.62ドルとなりました。当四半期の現金および投資残高は146億ドルでした。
当社は引き続き資本配分戦略を実行し、事業への投資とともにプラットフォームの有機的成長を優先しています。第2四半期は研究開発費に11億ドルを投資し、後期臨床プログラムへの投資を継続し、パイプラインを進展させた。販管費は約3億ドル。設備投資は約2億ドルでした。
累計の外部投資は、買収であった日本のオリシーロを除き、すべて戦略的提携であった。OriCiroはModerna Enzymaticsと改名され、Modernaの製造プロセス開発組織に統合されています。資本還元の面では、第2四半期に440万株、総額6億2,800万ドルの自社株買いを行いました。次に、当四半期の商業的および後期臨床試験に関する最新情報に移ります。
XPVワクチンに更新したCOVIDワクチンの申請書を世界各国の規制当局に提出し、2024年秋の販売開始の承認を待っているところです。間もなくアルパから発表される予定ですが、2023年のCOVID-19の売上予想を60億ドルから80億ドルの範囲に更新します。この幅は、米国の商業市場およびその他の国における追加契約を反映したものです。
米国のワクチン接種率の不確実性を考慮すると、この幅は広い。当社の商業チームはまた、2024年の次の呼吸器系商業製品であるRSVの上市に向けて準備を進めています。世界中の主要市場で承認申請が提出されています。
また、発売に向けてmRNA-1345の製造も開始しました。念のため申し上げておきますが、この製品は上市時にはプレフィルドシリンジ製剤となり、強力な有効性プロファイルと相まって、医療従事者向けの製品として非常に優れた位置づけとなります。がん領域では、当社の個別化新抗原治療(INT)であるmRNA-4157について、臨床開発および商業市場をサポートするため、製造の規模を拡大し続けています。アジュバント・メラノーマを対象とした第3相試験が7月に患者登録を開始したことをご報告できることを大変嬉しく思います。
スライド6に会社概要の更新を計画しています。当社の後期パイプラインの幅広さは、24年、25年、26年に複数の上市が可能であることを意味します。次にスライド7をご覧ください。モデルナがボストン・コンサルティング・グループにより、AIを活用したイノベーションのパートナーとして、2023年に世界で最も革新的な企業の1社に選ばれたことを誇りに思います。
ご存知の方も多いと思いますが、AIは数年前からModernaの研究開発プログラムの基盤の一部となっています。私たちは、バイオファーマにおけるAIリーダーであり続けるために、タンパク質やmRNAのエンジニアリング、アセットデータ分析、規制当局とのやりとり、その他多くのユースケースのための独自のAIモデルを構築してきました。Modernaの重要な考え方のひとつは、可能な限りあらゆるものをデジタル化するということです。2023年現在、モデルナの全メンバーにはAIトレーニングが義務付けられており、私たちはAIアカデミーを通じて企業レベルでのこのトレンドを促進しています。
私たちはModernaとして、すべてのビジネス機能において、AIを日常のワークフローに取り入れることに挑戦しています。モデルナのAI導入が加速していることをお伝えできることを嬉しく思います。私たちの安全な大規模言語モデルはmChatと呼ばれています。グラフでご覧いただけるように、5月18日に導入して以来、mChatの利用率は従業員の間で急速に伸びています。
開始からわずか60日で、すでに約50%の社員が利用しています。それでは、開発プログラムに関する最新情報をスティーブンにお伝えします。
スティーブン・ホーゲ — プレジデント
ありがとう、ステファン。皆さん、おはようございます。本日は、モデルナの主要な臨床プログラムの進捗状況についてレビューさせていただきます。スライドの左側には、3つの重要な呼吸器系ウイルスに対する商業化および後期臨床パイプラインプログラムがあります: COVID-19、インフルエンザ、RSVです。
COVID-19、インフルエンザ、RSVです。mRNA-1283は第3相試験で参加者を登録中であり、次世代インフルエンザ・ワクチンは第2相試験中です。当社は現在、成人および小児を対象とした6つの混合ワクチンプログラムを有しています。当社の混合ワクチンは、呼吸器感染症による最大の医療負担に対処するよう設計されており、コンプライアンス向上や投与コストの削減など、複数の利点を備えています。
COVIDプログラムについて説明します。私たちは、XBB.1.5変異体を標的とした更新型一価COVID-19ワクチンであるmRNa-1273.815の承認・認可申請書を提出しました。6月のVRBPAC会議で、委員会はXBB.1.5株を優先したXBB標的一価ワクチンを推奨したことを思い出してください。この勧告はFDAによって採用され、EMAとWHOのガイドラインと一致している。
米国では、CDC ACIPが今秋の承認・認可後、更新されたCOVID-19ワクチンの使用に関する推奨とガイドラインを発表する予定です。スライド11に示すのは、6月のVRBPAC会議で私たちのチームが発表した臨床データで、mRNA-1273.815を用いた第2/3相試験のサブセットのデータであり、XBB.1.5およびXPV系統の他の変異体に対する強力な中和作用を実証しました。XBB.1.5候補の臨床データをシーズン前に発表した唯一の企業であることを誇りに思います。RSVに話を移します。
先ほどステファンが述べたように、私たちは2024年の承認に向けて順調に進んでいることを嬉しく思っています。今月初めには、FDAへの計画的な申請を発表し、優先バウチャーを利用して審査を加速させる予定です。我々はmRNA-1345のプロファイルに非常に勇気づけられており、来年の商業的発売を心待ちにしている。
次に、季節性インフルエンザ・プログラムについてです。P303試験の登録が完了したことをお知らせできることを嬉しく思います。P303試験は、B抗原に対するHAI中和力価を上昇させるようにデザインされたmRNA-1010のアップデートを試験するものです。これは安全性と免疫原性の第3相試験であり、mRNA-1010のアップデート候補の早期承認をサポートするものと考えています。
次にスライド14の潜在性ワクチンについてです。妊娠可能な年齢の女性を対象とした第3相CMVワクチン試験が進行中で、80%以上の参加者が登録されたことを嬉しく思います。近々、この試験に全例が登録されることを楽しみにしています。初期の臨床プログラムでは、EBV、HIV、VZVワクチンの試験が進行中です。
HSVプログラムは前臨床段階にあります。それでは次のスライドでmRNA治療薬のポートフォリオを見てみましょう。INTを用いた第3相メラノーマ試験が現在登録中であることをお知らせできることを嬉しく思います。プロピオン酸血症、メチルマロン酸血症、GSD1aのアンメット・メディカル・ニーズに対応する希少疾患プログラムは進行中であり、データが成熟した時点で最新情報をお伝えしたいと思います。
実際、当四半期には、ASGCTでPAプログラムのデータの一部について最新情報を発表しました。プロピオン酸血症試験の用量確認は現在進行中です。そして最後に、バーテックス社の共同研究者は、第1相試験の単回投与部分において嚢胞性線維症患者の登録と投与を継続しています。さて、本日の最後のスライドでは、当社の個別化新抗原療法(INT)に関するエキサイティングな第3相試験のデザインについてお話ししたいと思います。
この第3相試験は、再発リスクの高い切除メラノーマ患者を対象に、INT+KEYTRUDA併用療法とプラセボ+KEYTRUDA併用療法を比較する無作為化二重盲検プラセボ対照試験です。本試験では、ステージ2bから4の切除メラノーマ患者約1,089人を1対1の無作為割付で登録する予定です。各患者は、有効群ではINTを3週間ごとに最大9回、KEYTRUDAを6週間ごとに投与され、比較群ではプラセボを3週間ごとに最大9回、KEYTRUDAを6週間ごとに投与される。主要評価項目は無再発生存期間、副次的評価項目は無遠隔転移生存期間と全生存期間です。
この第3相試験を迅速に立ち上げ、登録を開始したModernaとMerckの科学・臨床チームの協力体制には大変感心しています。それでは、アルパに話を移します。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
スティーブン、ありがとうございます。まず、当四半期と2023年上半期の売上高についてご説明します。2023年第2四半期のCOVIDワクチンの売上は約3億ドルで、これは流行性呼吸器疾患ワクチン事業の季節性を考慮すると予想通りでした。2023年上半期の売上高は21億ドルで、当社の予想通りでした。
念のため申し上げておきますが、上半期の売上は主にmRNA-1273.222によるもので、BA45変異体を標的とするCOVIDワクチンです。先ほどスティーブンから聞いたように、世界中の規制当局と保健当局は2023年秋のシーズン用にXBB.1.5変異型を選択しました。私たちは世界中の規制当局にワクチンの更新申請を提出し、現在承認と認可を待っているところです。規制当局の承認が得られれば、2023年後半にmRNA-1273.815を中心に追加売上を見込んでいます。
次に、2023年のCOVIDの売上見通しについて説明します。2023年のCOVIDの売上高は60億ドルから80億ドルの範囲になると予想しており、主な変動要因は米国のワクチン接種率です。2023年の売上構成は、今年上半期にすでに計上した売上21億ドルと、このスライドの真ん中の欄に記載されている国を含むいくつかの国から下半期に納品される先行購入契約をすでに締結している売上20億ドルです。世界中の顧客との最近の協議の結果、今年下半期に納入する20億ドルの契約が確定し、当初見込んでいた30億ドルから更新された。
当初の30億ドルのうち約10億ドルは2024年に繰り延べられる見込みです。また、2023年のCOVIDの売上予想総額60億~80億ドルには、日本やEUなどの他の市場だけでなく、米国での商業契約締結および商業契約見込みによる追加売上20億~40億ドルも含まれることになった。米国での
米国での商業契約は、今年下半期に予想される新たな売上高のかなりの部分を占めています。ご承知の通り、米国におけるCOVIDワクチン市場は、パンデミック期からエンデミック期への移行に伴い、コマーシャル市場に移行しました。米国の商用ワクチン市場は、小売薬局、卸売業者、グループ購買組織、統合配送ネットワーク、医療システム、政府機関、雇用主、その他のプロバイダーなど、さまざまな顧客セグメントで構成されています。
本日、これらの各顧客セグメントで契約を締結し、さらに追加契約を継続中であることをご報告できることを嬉しく思います。規制当局の承認が下り次第出荷できるよう、十分な供給準備が整っています。科学分野の契約により、今後数週間以内に予定されている米国での上市の見通しが立ち、2023年後半には新たな受注による追加売上が期待できます。
次にスライド21をご覧いただき、2023年秋の米国COVID市場についてご説明いたします。先ほども申し上げましたように、米国の市場規模を決定する重要な要素は、来る9月から12月にかけてのワクチン摂取率、あるいは予防接種の実施状況です。
前にも申し上げましたが、2023年の予想売上高60億ドルから80億ドルの範囲は、主に米国市場でのワクチン接種率によって左右されます。年初に、2023年の米国における秋季のワクチン接種数量の予測に必要なパラメータを提示しました。
2022年秋に米国で投与された約5,000万回分、ハイリスクカテゴリーの米国人8,200万人(50歳以上で合併症を有する人、または65歳以上の人)、過去9年間の米国でのインフルエンザワクチンの平均投与量1億5,000万回分、これは季節性呼吸器ワクチンの妥当な代用品であり、特にCOVIDの疾病負担の大きさを考慮すれば、妥当な代用品であると考えています。これらのパラメータは、2023年秋の米国市場における1億回投与という数量予測の裏付けとなった。
しかし、商業的流行市場への最初の移行年である今、市場規模を正確に予測し、この秋に何人のアメリカ人が予防接種を受けに来るかを予測することは難しいのが実情である。そのため、COVIDのシーズンが秋から冬にかけて実施される南半球の国々に注目し、米国でのワクチン接種の可能性を探っている。特に、2023年のCOVIDシーズンを終えたばかりのオーストラリアでは、接種率は19%で、ブースター・ワクチンの接種が推奨される集団もあった。
オーストラリアのデータと前年との比較から、2023年秋の米国市場規模は5,000万から1億回接種の範囲になると思われます。スライド22に移ります。
更新されたカバーワクチン発売のための秋のワクチン接種キャンペーンをご紹介したいと思います。1つ目は疾患啓発プログラムによる市場規模の拡大、2つ目はブランドプロモーションによるモデルナの市場シェアの拡大です。疾患啓発キャンペーンでは、疾患負担に関する教育、ACIPからの最新の推奨事項の明確化、COVID-19と季節性インフルエンザワクチンとの関連付けを行い、この秋のワクチン接種を消費者に促すことを目標としています。ブランド・プロモーション・キャンペーンでは、主要なメディア・チャネルを通じた消費者への直接キャンペーンや医療従事者とのプロモーションを実施し、Modernaのワクチンによるブランド選好を促進することに重点を置きます。
コマーシャル・チームは、COVIDワクチンの発売に向けて大きなエネルギーを注いでいます。スライド23に移ります。私たちは2024年のRSVワクチン発売に向けて準備を続けており、目の前にあるチャンスに興奮しています。私たちのワクチンはクラス最高のプロファイルを持っていると信じています。
これには、我々が共有している強力な臨床データに示されているように、脆弱な集団や高齢者集団において一貫した高い有効性が含まれます。さらに、当社の安全性プロファイルは十分に確立されています。私たちは現在、RSVワクチンと同じmRNA技術を用いてCOVIDワクチンを10億回以上接種しています。私たちの第3相試験では、勧誘された有害事象のほとんどは軽度から中等度であり、RSV第3相試験のmRNA-1345では、4月30日の締切日現在、GBSの報告例はありません。
最後に、上市時の当社および顧客にとっての重要な差別化要因のひとつは、すぐに使用できるプレフィルドシリンジに限定した製品形態です。このパッケージにより、医療従事者はすぐに使える製剤を消費者に投与することができます。このパッケージにより、医療従事者はすぐに使用できる製剤を消費者に便利に投与することができます。これにより、市場に出回っている再構成製剤と比較して、時間を節約し、ミスを減らすことができると考えています。当社は上市前活動への投資を続けており、来年の上市に向けて準備を整えています。
当社のコマーシャル・チームはグローバルに活動しており、製造組織はワクチンを供給するための十分な準備ができています。それでは、ジェイミーに話を移します。
ジェイミー・モック — 最高財務責任者
ありがとう、アルパ。そして皆さん、こんにちは。今朝は、第2四半期の業績についてご説明し、通期の業績見通しについてご説明いたします。スライド25から始めます。
製品売上高は、主に販売量の減少により、前年比94%減の2億9,300万ドルであった。2023年は、パンデミック(世界的大流行)から大きな季節性を伴う流行市場へと移行する過渡的な年になると引き続き予想しています。予想通り、第2四半期の売上高は比較的低水準であった一方、当社としては想定していた範囲の高水準で推移しました。2023年度第2四半期の売上原価は7億3,100万ドルでした。
これには、単価主導の製造原価に加え、過剰で陳腐化したCOVID-19製品に関連する在庫評価損4億6,400万ドル、未稼働製造能力1億3,500万ドル、確定購入コミットメントに係る損失7,500万ドルが含まれています。ロイヤリティ以外のこれらの費用は、主に製品需要が最新の一価XBB.1.5 COVIDワクチン候補にシフトしたこと、および年初の予想と比較して市場規模が全体的に縮小したことによるものです。2023年秋のシーズン開始時に十分な供給量を確保するため、菌株選択のさまざまな結果に備え、その結果、損益に追加コストが発生しました。また、一価が選択されたことで、過去に製造した半製品を使用することができなかった。
研究開発費は11億ドルで、前年比62%増となった。研究開発費の増加は、引き続き臨床試験関連費用、特にRSV、季節性インフルエンザ、CMVの第3相試験によるものです。研究開発費の増加は、研究および後期開発への取り組みをサポートするための人員増による人件費の増加にも起因しています。販管費は前年同期比57%増の3億3,200万ドルでした。
販管費の増加は主に、当社のデジタル・イニシアティブ、市販製品、関連する商業化活動、および会社拡大を支援するための人件費および外部サービスへの継続的な投資によるものです。法人税は、主に営業損失により、第2四半期に3億6,900万ドルの利益となりました。当期純損失は14億ドルで、前年同期は22億ドルの純利益でした。また、希薄化後1株当たり損失は、2022年の希薄化後1株当たり利益5.24ドルに対し、3.62ドルであった。
第2四半期の現金および投資残高は、第1四半期末の164億ドルに対し、146億ドルとなった。この減少は、当期純損失と約6億ドルの自社株買いによるものです。将来の製品供給のための現金預け金は、当四半期中に約1億ドル減少し、第2四半期末には17億ドルとなりました。次にスライド 27 をご覧ください。
資本配分の優先順位に関する進捗状況についてご説明します。私たちの最優先投資は、これまでも、そしてこれからも、ベースビジネスへの再投資です。2023年上半期の研究開発費は前年同期比80%増の23億ドルで、通期では45億ドルの研究開発投資を行う予定です。また、デジタル機能、組織の商業的強化、製造拠点の拡大にも投資しています。
海外と米国の製造拠点を拡大するため、2023年の設備投資を前倒ししました。第2の投資優先順位は、当社のプラットフォームを実現・補完する魅力的な外部投資や提携の機会を模索することです。私たちは規律あるアプローチを続けており、複数の活発な話し合いを行っています。
社内外の投資機会を評価した後、現金の追加的な使途を検討します。2023年上半期には800万株を約12億ドルで買い戻し、2023年6月30日現在、17億ドルの自社株買い戻し枠が残っています。それでは、スライド28の2023年の財務フレームワークをご覧ください。私たちは、先行購入契約以外の考え方についても共有したいと思います。
先ほどアルパが申し上げましたように、2023年の製品売上高は60億ドルから80億ドルの範囲を見込んでおり、その内訳は既存のAPAによるものが約400万ドル、米国、日本、EU、その他の国々への追加販売によるものが約20億ドルから40億ドルです。世界中の顧客との最近の話し合いの結果、当初のAPA総額50億ドルのうち約10億ドルが2024年に延期される見込みとなった。下期の販売タイミングは、世界各国の規制当局の承認のタイミングと第3四半期の出荷可能日数に左右されます。現在のところ、第3四半期に30%、第4四半期に70%の販売比率を見込んでいる。
現在、通年の売上原価は35億~40億ドルの範囲になると予想している。この時点では、生産コストはほぼ固定されており、販売結果に左右される部分はごくわずかです。従って、モデル作成のためには、絶対的な金額の範囲を提示した方がより有益だと考えています。研究開発費および販売費および一般管理費については、通期で約60億ドル、研究開発費で約45億ドルを引き続き見込んでいます。
営業損失、研究開発費控除、国際引当金、非経常的な項目の計上により、通期で7億ドルから10億ドルの範囲の税効果を見込んでいます。最後に、資本的支出は引き続き約10億ドルを見込んでいます。以上で私の挨拶は終わり、ステファンに電話を戻します。
ステファン・バンセル — 最高経営責任者
ジェイミー、アルパ、ステファン、ありがとう。Modernaは、COVIDを皮切りに有望な商業的見通しを立てています。パンデミックからエンデミックへの移行に伴い、ワクチン接種率には不確実性がありますが、2023年のCOVIDの売上は60億ドルから80億ドルの範囲になると予想されます。
私たちは、このストレスのかかる流行終息期が、経常的な収益ストリームの可視化につながると考えています。当社はCOVIDワクチンを非常に長い期間販売することになると信じており、COVIDとインフルエンザを1つのワクチンに統合するよう取り組んでいます。RSVに話を移します。RSVワクチンには強力な製品プロファイルと差別化されたプレフィルドシリンジがあり、2024年の上市を見込んでいます。
がん領域では、INTの製造能力を拡大し、商業化に備えています。フェーズ2のデータは非常に強力で、現在メラノーマを適応症とするフェーズ3に入っています。パートナーのメルク社とともに、すでに発表したメラノーマと非小細胞肺がん以外の適応症の優先順位付けに取り組んでいます。一歩下がって、幅広いポートフォリオを見てみましょう。
私は、基本的にワクチン、腫瘍学、肝臓の希少遺伝性疾患においてポジティブな臨床データを持つModernaのハイケース・シナリオでプレーしていることに非常に興奮しています。今後3年間(24年、25年、26年)、私たちはワクチンと治療薬のポートフォリオ全体で複数の製品を上市し、会社を力強い売上成長へと導くことを期待しています。収益源が多様化し、パイプラインが充実した新時代を迎えた今、モデルナにとって非常にエキサイティングな時期です。プラットフォームは機能しており、その結果、非常に短期間で前例のない数のmRNAが上市されるでしょう。
9月30日に開催されるR&Dデーで、さらに詳しいご報告ができることを楽しみにしています。このイベントはニューヨークで生中継され、もちろんオンラインでもご覧いただけます。12月7日には、第2回ESGデーを開催します。このイベントはオンラインでもご覧いただけます。
当社の使命は、mRNA医薬品を通じて人々に最大限のインパクトを与えることです。この使命は、人の命を延ばし、患者の苦しみを和らげる複数の新薬の上市を間近に控えた今、特に重要な意味を持ちます。Modernaがその潜在能力を発揮し続けることで、当社のすべての利害関係者が利益を得る態勢が整っています。この会社の一員であることは、私たち全員の特権です。
質問を受け付けます。オペレーター?
質疑応答
オペレーター
[最初の質問はゴールドマン・サックスのサルヴィーン・リヒターです。回線は開いております。サルヴィーン・リヒター — ゴールドマン・サックス — アナリスト
おはようございます。私の質問にお答えいただきありがとうございます。下期の追加販売見込みについて、米国でのワクチン接種率に加えて、そのレンジの上限を達成するために影響を与える可能性のある要因について教えてください。また、秋のシーズン終了後、追加契約が2024年にずれ込むことはないと確信していますか?ありがとうございました。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
ご質問ありがとうございます。20億ドルから40億ドルの追加売上ということですが、ご指摘の通り、60億ドルから80億ドルの売上を達成するための重要な要因は、この秋に何人のアメリカ人が予防接種を受けに来るかということです。つまり、ワクチン接種率がその範囲内で最も大きな変動要因となります。私たちは、米国における市場シェアとこれまでの商業契約の進展に自信を持っています。
さらに、米国以外では、追加契約が延期される可能性があるとのご質問ですが、私たちは事前購入契約を結んでいるすべての国と会談し、2024年に延期された10億ドル以外の今年下半期の納入をすでに確認しています。ですから、私たちは自信を持って20億ドルの範囲内と申し上げています。
サルヴィーン・リヒター — ゴールドマン・サックス — アナリスト
ありがとうございます。
オペレーター
次の質問まで少々お待ちください。次の質問はTDコーウェンのタイラー・ヴァン・ビューレンです。どうぞよろしくお願いいたします。
タイラー・ヴァン・ビューレン — TDコーウェン — アナリスト
やあ、みんな。おはようございます。COVID-19ワクチンの年間売上高が60億ドルから80億ドルになると予想されていますが、COVID-19ワクチンのフランチャイズ・テールについて考える上で、この売上高が実需に与える影響についてどのように考えるべきでしょうか?40億ドルはすでに年初のAPAから過年度にロックインされているので、20億ドルから40億ドルでしょうか?もしそうでないなら、40億ドルのAPAのうち、どれくらいの割合が本当の年間ブースター需要だと思われますか?おそらく、下半期に期待される20億ドルでしょうか?ご意見をお聞かせください。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
ご質問ありがとうございます。2024年についてどのように考えているかということですが、2023年の上半期に注目したいと思います。そのうちの一部は、ほとんどの国が秋の予防接種キャンペーンに向けて毎年予防接種を実施していることから、今後数年間は定期的な売上を見込んでいない数量です。残りの40億ドルから60億ドルについては、ワクチン需要は維持され、やがてCOVIDワクチン接種率が上昇傾向に転じると思われるインフルエンザの数量について考えるにつれて、最終的には増加すると考えています。
先ほど申し上げたように、たとえば米国では毎年秋に約1億5000万本のインフルエンザ・ワクチンが接種されています。2023年については、5,000万から1億の範囲でモデル化しています。私たちは、高い疾病負担を考慮し、また将来的な組み合わせも考慮しながら、時間の経過とともに1億5,000万人程度に近づいていくと考えています。
オペレーター
次の質問に移ります。次の質問はバークレイズのゲーナ・ワンです。お待たせしました。
ジーナ・ワン — バークレイズ — アナリスト
ありがとうございます。簡単な質問を2つ。今回のCOVIDの米国での商業契約について、最初の在庫発注は確定しているのでしょうか?もう1つは、RSVワクチンについてですが、ファイザーとGSKのラベルの文言、そして初回発売が遅いということですが、承認と発売準備について何かお分かりになることがあれば教えてください。
アルパ・ガレイ — チーフ・コマーシャル・オフィサー
ありがとうございます。それでは、最初に米国での契約に関する質問をさせていただきます。私どもの契約の進捗状況ですが、私どもの商業契約の多くに最低数量コミットメントがありますが、ほとんどの契約は最低数量コミットメントを検討していました。
しかし、ほとんどの契約は最小限の契約しか結んでいません。また、顧客との綿密な情報交換により、ワクチンの接種率次第では、契約数量が増加する可能性もあります。先日のRSV ACIP会議については、ACIPが推奨する臨床的意思決定の共有により、承認された最初の2つのワクチンの接種がより緩やかになると考えています。しかし、私たちの臨床プログラムとGSKとファイザーの臨床プログラムの両方から、より多くのデータが得られれば、この勧告を更新する可能性があり、そうすればRSVワクチンをより広く普及させることができると考えています。
オペレーター
次の質問に移ります。次の質問はジェフリーズのマイケル・イーです。どうぞよろしくお願いいたします。
ディナ・エルモンシェド — ジェフリーズ — アナリスト
マイクに代わってディナです。質問にお答えいただきありがとうございます。インフルエンザのアップデートについてちょっと質問させてください。
2つ目の免疫原性試験について第3四半期にアップデートを行い、そのデータを第3四半期に出すということですね。しかし、2回目の感染症による有効性試験、あるいは前回の感染症による有効性試験のスケジュールはどうなっていますか?それは変更されましたか?また、PCVに関しても、第3四半期にはデータが出るのでしょうか?また、PCVに関して、規制当局が進める道筋について、何か追加的な最新情報を共有する予定はありますか?また、肺などに関する最新情報も教えてください。ありがとうございました。
スティーブン・ホーゲ — 社長
素晴らしい。ディナ、ご質問ありがとうございます。まず、1010インフルエンザ・プログラムについてですが、ご指摘の通り、現在進行中の第3相試験が2つあります。ご指摘のP302試験については、有効性試験の最新情報を提供する予定です。
また、ご存知のように、ワクチン・デーでは、シーズン終了後のアップデートについてお話しました。また、P303免疫原性試験の進捗状況についてもお知らせします。また、P303免疫原性試験の進捗状況についてもお伝えする予定です。PCBではなくINTですが、INTに関連して、ちょうど1カ月前にASCOで皆さんに最新情報を提供する機会を得ました。
もちろん、R&Dデーでもその再演を行う予定です。また、INTプログラムで起こっている他の進展についてもお話ししますと、非小細胞肺がんでの立ち上げと実行に懸命に取り組んでいることは明らかですが、私たちは本当に — 極めて重要な試験 — に取り組んでいます。しかし、メラノーマを対象とした最初の第3相試験が開始されたことで、私たちは本当に興奮しています。
ディナ・エルモンシェド — ジェフリーズ — アナリスト
素晴らしい。ありがとうございます。
オペレーター
次の質問の前にもう1つ。次の質問はUBSのエリー・メルルです。回線は開いています。
発言者不明
サラです。質問にお答えいただき、ありがとうございます。先ほどのタイラーの質問の続きです。
今後のCOVIDの数量についてですが、上期と下期をどのように考えているか、もう少し詳しく教えていただけますか?特に来年上半期の見通しについて教えてください。また、CMVについては、いつ頃登録が完了するのでしょうか?また、いつデータが取れるかについてどのように考えるべきでしょうか?また、イベント発生率について、ブラインドベースで何かおわかりになることはありますか。ありがとうございました。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
では、最初の質問をお受けして、CMVのスティーブンに引き継ぎたいと思います。上期と下期をどのように考えているかということですが、上期は秋から冬にかけての南半球での売上を見込んでいます。また、一部の国では、特に免疫不全患者や高齢者、リスクの高い患者を対象に、春のキャンペーンやブースターが引き続き実施されます。そのため、南半球でのハイリスク・スプレーのブーストや、今年の晩冬から1月にかけてのキャリーオーバーの売上も見込んでいます。
しかし、売上の大半は北半球と秋のワクチン・キャンペーンから予想されるため、引き続き下半期に期待されます。
スティーブン・ホーゲ — 社長
素晴らしい。CMVの登録に関する質問ですが、最近、登録が完了に向かって加速していることにとても興奮しています。80%を超えました。まもなく登録を完了したいと考えています。
今年の前半は順調に進んでいますので、特に目標は設定していませんが、今年中に確実に登録したいと思っています。CMV第3相プログラムを追跡する上で、非常に興味深いのはここからだと思います。ワクチン・デーでお話ししたように、すでに症例登録が始まっています。フル登録になれば、有効性に関する最初の中間解析に症例を提供できる参加者が増えるでしょう。
オペレーター
次の質問に移ります。
発言者不明
ありがとうございます。
オペレーター
次の質問はRBCキャピタルのルカ・イッシです。お待たせしました。
ルカ・イッシ — RBCキャピタル・マーケッツ — アナリスト
素晴らしい。私の質問に答えてくれてありがとう。1つだけ、ジェイミー、マージンについて質問させてください。以前のガイダンスでは売上総利益率が60%から65%であったのに対し、今日の新しいガイダンスでは中間値で売上総利益率が47%となっていますね。
この変化の要因をもう少し詳しく教えてください。それからスティーブンさん、インフルエンザについてです。サノフィは、B型株の免疫原性の低さはクラス効果であると主張したと思います。では、どのmRNA製剤についても、B株に対する免疫原性は高いのでしょうか?皆さんのご意見をお聞かせください。ありがとうございました。
ジェイミー・モック — 最高財務責任者
ルカ、ありがとう。最初の質問にお答えします。マージンについては、その通りです。
60%から65%を計画していました。2024年までの10億ドルのAPAを例にとりますと、これは主に数量に左右されるものです。他の市場も含めて、35億ドルから40億ドルにはまだその費用が含まれています。ですから、今期以前の販売数量は、プッシュアウトの影響もありますが、全体的な販売数量の増加もあり、少し高めに予想していたと思います。
スティーブン・ホーゲ — 社長
サノフィがクラス効果について主張したことは承知しています。私は同じようには考えていません。推測ではなく、データを見て答えを出そうと思います。次の四半期にP303第3相試験の進捗状況を報告することを楽しみにしています。
ルカ・イッシ — RBCキャピタル・マーケッツ — アナリスト
素晴らしい。ありがとうございました。
オペレーター
次の質問まで少々お待ちください。次の質問は、パイパー・サンドラーのエドワード・テントオフです。お待たせしました。
エドワード・テンスフ — パイパー・サンドラー — アナリスト
素晴らしい。ありがとう。おはようございます。聞こえますか?
アルパ・ガレイ — チーフ・コマーシャル・オフィサー
はっきりと
エドワード・テンスフ — パイパー・サンドラー — アナリスト
素晴らしい。素晴らしい。私の質問は、もう少し長期的な戦略的なものです。COVIDが進化し続け、最終的に1010、さらにはRSVの承認を目指すとして、規制上の観点からこれらを組み合わせる計画はどのようなものでしょうか。また、商業的な観点からも、現在承認されたワクチンが1種類、来年には2~3種類承認されるかもしれない状態から、どのようにして1種類のコンボワクチン、あるいは複数のコンボワクチンが承認されるようになるのでしょうか?お答えいただきありがとうございました。
スティーブン・ホーギー — 社長
そうですね。テッド、質問をありがとう。ご存じのように、私たちは6種類のコンボワクチンを保有しています。たくさんの臨床データがありますし、新しい組み合わせも検討し続けています。
そして、インフルエンザ、RSV、COVIDが承認され、さらに第2世代のCOVIDも承認されるような状況になった場合、私たちはそれらの複数の異なる組み合わせを検討し、公衆衛生と柔軟性の面で最大の効果を発揮するような選択肢を提案しようとしていますので、ご安心ください。これらの試験は、一価ワクチンが承認された後、免疫の橋渡しをするための試験であり、これらの試験で免疫原性や安全性が劣らないことを証明するためのものです。これらの試験は非常に短期間で実施できます。また、ご存知のように、シーズン中に実施する必要もありません。
ですから、私たちの目標は、今年を通して申し上げてきたように、3つの一価ワクチンの承認申請、そして最終的には承認に向けた作業を完了させ、少なくとも1つ、そして複数の併用ワクチンの極めて重要な第3相試験に速やかに移行することです。私たちの目標は、25年以降にこれらのワクチンを上市することです。その理由は明らかで、コンプライアンスを改善し、より高い価値を提供し、実際に医療の管理コストを削減するためです。特にRSVのデータの強さとCOVIDの進捗状況を考えると、ここからの道筋は非常に明確であり、インフルエンザについても間もなく最新情報を提供したいと思います。
その後、すぐに第3相試験を開始し、コンボ製剤の上市を可能にします。
エドワード・テンスフ — パイパー・サンドラー — アナリスト
本当に助かります、スティーブン。それから、もしよろしければ、1点だけ明確にさせてください。極めて重要な第3相試験とおっしゃいましたが、これはイムノブリッジング試験でしょうか?
スティーブン・ホーギー — 社長
免疫原性ですね。免疫原性と安全性の試験です。一価ワクチンの有効性が確認されたら、その後の有効性試験を行わなければならないとは考えていませんし、規制上の観点からも通常ではありません。
エドワード・テンスオフ — パイパー・サンドラー — アナリスト
ええ、素晴らしい。ありがとうございました。
オペレーター
次の質問まで少々お待ちください。次の質問はドイツ銀行のマノス・パパダキスさんです。ただいまより回線をお開けします。
マノス・パパダキス — ドイツ銀行 — アナリスト
こんにちは。私の質問にお答えいただきありがとうございます。基本的には、売上原価ガイダンスについてお聞きしたかっただけです。これは売上高の範囲に関係なく適用されるのでしょうか?そうでない場合、感応度はどの程度になるのでしょうか?ありがとうございました。
ジェイミー・モック — 最高財務責任者
ご質問ありがとうございます。はい、準備した発言で申し上げたように、それは関係なく適用されます。この費用の大半は現時点で固定されています。
原材料はすでに発注済みです。製造はすでに開始しています。規制当局の承認が下り次第、すぐにでも使えるように多くの供給体制を整えています。ですから、35億ドルから40億ドルというのは、どちらにしても販売結果に大きく左右されるものではありません。
また、長期的な話になりますが、今年私たちが苦しんでいるのは予測不可能な市場だと思います。ですから、先の35%から40%、あるいは60%から65%の粗利益率という質問に戻りますが、より予測しやすくなれば、適切な量の材料を発注することができるようになり、適切な量のコミットメントができるようになります。しかし、長期的には全体として75%から80%の売上総利益率を確保できると確信しています。
オペレーター
次の質問まで少々お待ちください。次の質問はバンク・オブ・アメリカのジェフ・ミーチャムです。どうぞよろしくお願いいたします。
アレックス・ハモンド — バンク・オブ・アメリカ・メリルリンチ — アナリスト
おはようございます。私の質問にお答えいただきありがとうございます。ジェフに代わってアレックスです。INTワクチンについて、他にどのような適応症が考えられるか教えてください。また、どの適応症を最初に追求するかはどのように決定するのでしょうか?また、どの適応症を最初に追求するかはどのように決定するのでしょうか?次に、RSPにおけるインフルエンザについて、競合と新規参入のそれぞれについて、どのような商業的ハードルを想定していますか?ありがとうございました。
スティーブン・ホーゲ — プレジデント
ありがとうございます。ご質問ありがとうございます。まずRSVについてです。ご存じのように、メラノーマを進めています。
そして、非小細胞肺がんを進めています。非小細胞肺がんのアンメット・ニーズが非常に大きいことは明らかです。ご承知のように、免疫療法にとって肺がんは最も大きな治療機会のひとつです。以前にも申し上げましたように、他の適応症がどのようなものになるのかについては、パートナーのメルク社とともにまだ公表していません。
しかし私たちは、PD-1 KEYTRUDAが成功を収めたすべての適応症について、PD-1抗体で達成されたことを大幅に改善する余地や機会がまだあると考えている適応症について、その道をたどるつもりであると述べています。そのため、アジュバント療法やおそらくステージ4のいくつかの療法で、そのような利点があり、私たちが短期間でそこに移行することを期待しています。当社とメルク社は現在、このような計画を最終化しているところです。そして適切な時期になれば、当然ながら、それらの研究の開始についてご案内します。
メラノーマと非小細胞肺がんはその最初の2つにすぎません。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
RSヴァン・フローについてのご質問をお受けします。来年、RSVを発売できることを大変うれしく思っています。第3の製品を市場に投入することになりますが、高リスク群に対する一貫した高い有効性、RSVに対する唯一のmRNAプラットフォームにおける確立された安全性プロファイル、そして最後に、先ほど申し上げたように、すぐに使えるプレフィルドシリンジを備えた唯一の製品であることなど、クラス最高のプロファイルであると確信しています。そのため、RSVの上市準備については非常に良い感触を得ており、2024年に実行に移す準備ができています。
インフルエンザの観点からは、当社の第一世代インフルエンザ・ワクチンとなる1010の利点のひとつは、市場投入までのスピードが速いことで、将来、より優れた株とのマッチングが可能になることだと考えています。また、先ほどスティーブンが述べたように、商業的な観点から、インフルエンザのプロファイルが強化されるにつれて、患者からも医療システムからも、当社の混合ワクチンに非常に多くの関心が寄せられています。ですから、RSVとインフルエンザを併せ持つということは、将来的に素晴らしい組み合わせの機会を与えてくれるのです。
アレックス・ハモンド — バンク・オブ・アメリカ・メリルリンチ — アナリスト
ありがとうございます。
オペレーター
次の質問まで少々お待ちください。次の質問はグッゲンハイム証券のエヴァン・ワンさんです。回線は開いております。
エヴァン・ワン — グッゲンハイム・パートナーズ — アナリスト
やあ、みんな。COVIDについてフォローアップしたいと思います。米国以外の市場について考えているのですが、日本のようないくつかの市場における受注規模や市場でのポジショニングについて、詳細を教えていただけますか?また、2024年に何が変わる可能性がありますか?また、インフルエンザについては、P303の研究がフル稼働していることをうれしく思っています。
アルパ・ガレイ — チーフ・コマーシャル・オフィサー
それでは最初の質問にお答えします。アメリカから見た場合、日本との最小限のコミットメントが発表されました。日本と交わした最低限のコミットメントは、早ければ8月中に製品を日本へ導入するというもので、今秋には実行に移す準備ができています。
もし日本でのワクチン摂取が拡大すれば、日本からの追加注文も期待しています。それ以外の地域については、最初のコラムの末尾にすでに概説したように、先行購入契約を結んでいますし、EUを含む他のいくつかの国際市場とも継続的に話を進めています。2024年に関しては、変化があります。米国以外で予想されることは
アメリカ以外の国で予想されるのは、中央政府による調達から、より一般的な商業市場へと移行する市場が増えるということです。ですから、私たちは変化を予測しています。
そのような変化のほとんどは、調達先の変更と、今後の価格設定や償還に関する変化です。
スティーブン・ホーゲ — プレジデント
インフルエンザの質問です。そうですね、P303は完全に登録されています。P303試験のスケジュールは決まっており、今四半期中にデータを提供する予定です。B株に関しては、P302試験でB株の非劣性を達成したことを、今年の初めにすでにアップデートしています。
P301試験ではそれを逃していたのです。そして、P303試験で一連の変更を加え、免疫原性を向上させるB株でのベネフィットをもたらすと確信しましたし、今もそう確信しています。ですから、私たちの科学的な理解は本当に強く、クラス最高のものだと考えていますし、P303試験のデータを見れば、私たちはB株に関して非常に強い立場にあり、A株に関しても引き続き非常に強い立場にあると、私は楽観視しています。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
それではケビンさん、最後の質問になります。
オペレーター
わかりました。最後の質問はレッドバーンのサイモン・ベイカーです。少々お待ちください。サイモンさん、どうぞ。
サイモン・ベイカー — レッドバーン・パートナーズ — アナリスト
ありがとうございます。私からの質問は2つだけです。1つは、競合他社の2年間のデータとASICの勧告を踏まえて、RSVの機会に対する見方はどのように変わりましたか?どのような点で、クラス最高のプロファイルを達成できるとお考えですか?もう1つは、CMVの第3相登録についてもう少しお伺いしたいのですが、今四半期までにフル登録ができるとお考えでしょうか。ありがとうございます。
アルパ・ガライ — チーフ・コマーシャル・オフィサー
RSVの質問から始めます。ACIPの共有意思決定勧告や、今年共有された再接種に関するいくつかのデータを考慮すると、当初はワクチンの摂取が遅れると予想しています。この市場における当社のポテンシャルについては、クラス最高のプロファイルを有していると引き続き確信しています。また、当社独自のワクチン・プログラムから追加データが得られれば、ACIPの勧告が導入され、数年後にはより早い普及が可能になると期待しています。
スティーブン・ホーギー — プレジデント
そして、開発面で唯一付け加えるとすれば、我々は明らかに複数の異なるバージョンのRSV混合ワクチンを検討しており、その利点のひとつは明らかに利便性とコンプライアンスの向上でしょう。そして、医療システムの価値を創造することができれば、それは……それは進化し続けると思います。CMVに関連することですが、登録がいつ完了するかというガイダンスは設定していません。しかし、すでに80%を超えていることから、今年中に、今四半期中とは言いませんが、今年中に登録が完了すると確信しています。
申し上げたように、本当に重要なのは、80%か99%か100%かということではありません。症例とイベントの発生が、これから先の最初の中間解析の原動力となるのです。登録患者数が多ければ多いほど、イベントの発生件数や発生ペースが増加することは明らかです。そのため、私たちはこの作業に非常に注力しており、今年中に完了させたいと考えています。
サイモン・ベイカー — レッドバーン・パートナーズ — アナリスト
ありがとうございました。
オペレーター
では、最後にステファンにお願いします。
ステファン・バンセル — 最高経営責任者
ご質問ありがとうございました。特に9月13日のR&Dデーでは、多くの方々に直接お会いできることを楽しみにしています。素晴らしい一日をお過ごしください。ありがとうございました。
以上です。他の翻訳希望やご感想をいただけると嬉しいです。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>


