米国の大手バイオ医薬品企業のバーテックス・ファーマシューティカルズ (NSDQ:VRTX)2022年第1四半期決算説明会の日本語訳です。
CF(嚢胞性線維症)の画期的な新薬で今後の希少疾病の成長をリードすると言われており、今回の決算は良かったですが弱かったですね。
有望とは思ってますので今後に期待して行きたいと思います。
アッヴィ(NSDQ:ABBV)もCFでも新薬を開発してましたがP2での思ったような結果がでませんでした。そのため、市場参入には時間が掛かる為しばらくは市場を独占できそうです。
もっているのもおもしろそうです。
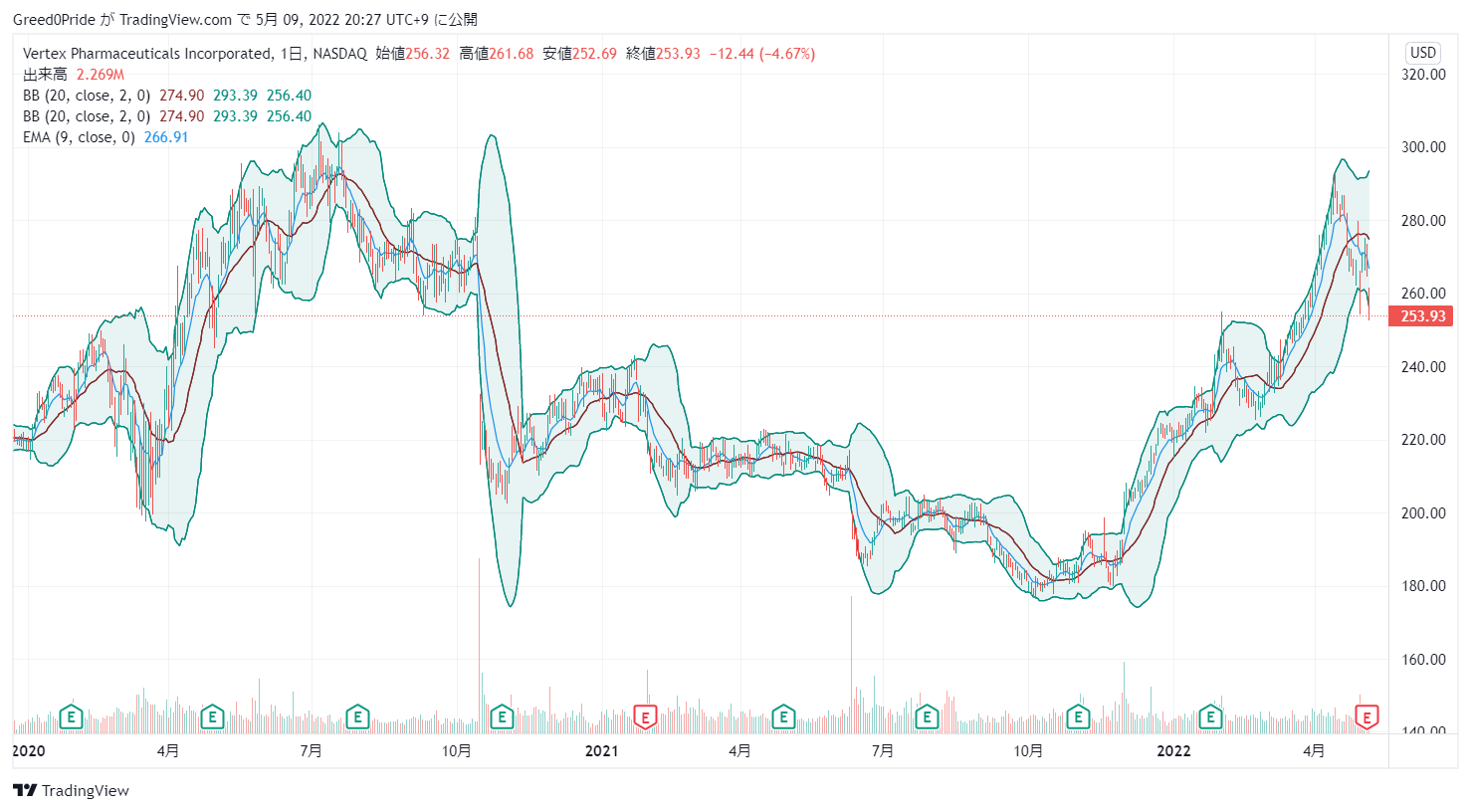
バーテックス・ファーマシューティカルズ (NSDQ:VRTX)株価
バーテックス・ファーマシューティカルズ (NSDQ:VRTX)2022年第1四半期決算説明会
Call participants:
Michael Partridge
Reshma Kewalramani — Chief Executive Officer and President
Stuart Arbuckle — Chief Operating Officer
Charlie Wagner — Chief Financial Officer
Cory Kasimov — J.P. Morgan — Analyst
Unknown speaker — Bank of America Merrill Lynch — Analyst
Robyn Karnauskas — Truist Securities — Analyst
Salveen Richter — Goldman Sachs — Analyst
Bastiano Sanna — Chief of Vertex Cell and Genetic Therapies
Michael Yee — Jefferies — Analyst
Phil Nadeau — Cowen and Company — Analyst
Colin Bristow — UBS — Analyst
David Altshuler — Executive Vice President, Global Research and Chief Scientific Officer
Mohit Bansal — Wells Fargo Securities — Analyst
Evan Seigerman — BMO Capital Markets — Analyst
Liisa Bayko — Evercore ISI — Analyst
More VRTX analysis
2022年5月05日午後4時30分(米国東部時間)
マイケル・パートリッジ
こんばんは。マイケル・パートリッジでございます。バーテックス社の2022年第1四半期決算の電話会議にようこそ。今夜の電話では、準備のために、バーテックスのCEO兼社長であるレシュマ・ケワラマニ博士、スチュアート・アーサム博士にご挨拶をいただいております。
Reshma Kewalramani(バーテックス社CEO兼社長)、Stuart Arbuckle(最高執行責任者)、Charlie Wagner(最高財務責任者)です。質疑応答には、Vertex Cell and Genetic TherapiesのチーフであるBastiano Sanna博士と、チーフサイエンティフィックオフィサーのDavid Altshuler博士が参加される予定です。
この通話をお聞きになる際には、ウェブキャストのスライドにアクセスされることをお勧めします。本通話は録音されており、再生は当社ウェブサイトにてご覧いただけます。この電話会議では、本日のプレスリリースおよび米国証券取引委員会に提出した書類に詳述されているリスクや不確実性を前提とした、将来の見通しに関する記述を行う予定です。これらの記述は、バーテックスが販売するCF医薬品、パイプラインおよびバーテックスの将来の財務実績に関するものを含みますが、これらに限定されるものではなく、経営陣の現在の仮定に基づくもので、実際の結果や事象は大きく異なる可能性があります。また、今晩の電話会議で確認する一部の財務結果およびガイダンスは、非GAAP方式であることに留意してください。それでは、レシュマ・ケワラマニ博士に電話をつなぎます。
レシュマ・ケワラマーニ — 最高経営責任者兼社長
マイケル、ありがとうございます。始める前に、これがマイケル・パートリッジの最後の四半期電話会議になりますので、この場を借りて、バーテックスに対する彼の優れた奉仕と貢献を称えたいと思います。25年間、彼はアナリストや投資家に対するバーテックスの顔として、その冷静かつ堅実なアプローチで、数え切れないほどのマイルストーンと会社の多くの進化を通じて、当社のIRチームを率いてきました。最近では、4つの嚢胞性線維症治療薬の上市や、幅広い中・後期パイプラインの出現を通じて、マイケルはバーテックスのリーダーシップチームの重要な一員として、当社のストーリーを世界と共有する手助けをしてきました。
マイケルは、バーテックスと私たちがサービスを提供する患者さんに真の情熱を注いできました。私たちは彼の献身に感謝するとともに、彼がバーテックスのためにしてくれたことすべてに個人的にお礼を申し上げ たいと思います。四半期レビューに移ります。バーテックスは、CF事業の好調、パイプラインの急速な進展、卓越したオペレーションの継続により、全体として素晴らしいスタートを切っています。
第1四半期のCF製品の売上は、世界的に治療を受けているCF患者数の継続的な増加を反映し、前年同期比22%増の21億ドルとなりました。また、社内外のイノベーションに多大な投資を続けているにもかかわらず、当社の非GAAPベースの営業利益率は56%と業界トップクラスを維持しています。当社は、研究および臨床段階のパイプラインにおいて急速な進展を維持し、現在、6つのプログラムがPOC段階を終えています。また、当四半期は強固なバランスシートと82億米ドルの現金および投資で終了しました。
CFは、当社の研究開発戦略の模範となるものです。この6~12ヶ月でそれが明確になりました。当社の研究開発戦略は、CF以外にも、多くの疾患領域で低分子治療薬や細胞・遺伝子治療薬の発見・開発で実証されています。この連続的なイノベーションは、複数の疾患を治癒させないまでも変容させる可能性があり、そうすることでより多くの患者さんを助け、会社の長期的な成長を促進することができるのです。
基本的に私たちの戦略の目標は、ベンチからベッドサイド、そして重要な開発段階まで、因果関係のあるヒト生物学、検証されたターゲット、バイオマーカーに基づき、創薬と開発の成功確率を高めることにあります。CF、鎌状赤血球症、βサラセミアで得られたデータ、そして現在、APOL1を介した腎臓病、疼痛、1型糖尿病で相次いで肯定的な概念実証がなされており、当社の臨床段階のパイプラインは、疾患領域の数という点ではかつてなく幅広く、様式という点ではより多様で、より高度なものとなっています」。CFの継続的な成長、数十億ドルのビジネスチャンスをもたらす中・後期開発段階の6つのプログラムによる幅広い臨床パイプラインの進展、そして臨床に近づきつつある次の治療法の可能性によって、当社は今、新たな変曲点を迎えているのです。IND-enabling試験を開始した次のプログラム群には、CFのmRNAプログラム、1型糖尿病の細胞+デバイスプログラム、AATVの低分子矯正薬の次の波、DMDのin vivo遺伝子編集プログラムが含まれます。
これらのプログラムの多くは、今年末のIND申請とその後の臨床試験開始に向けて進行中です。当社の研究開発戦略とビジネスモデルを組み合わせることで、当社は、世界中のより多くの患者さんに革新的な医薬品をお届けするために、継続的なイノベーションと持続的な成長を実現することができるのです。それでは、当四半期の研究開発ハイライトをご覧ください。CF の将来を見据え、当社は引き続き長期的な視点に立ったリーダーシップを強化していきます。
Trikaftaの実体験は蓄積されつつあり、Stuartが語るように、開発中のレジメンの水準を高めています。とはいえ、もしTrikaftaを凌駕することが可能であれば、私たちはそれを成し遂げたいと考えています。VX-121/テザカフター/561のネクストインクラスの3剤併用療法は、極めて重要な開発段階を経て、急速に進行しています。180以上の臨床試験施設がオープンしており、Skylineの第3相プログラムに患者を登録しています。
2022年末から2023年初めには、登録が完了する見込みです。念のため申し上げますが、VX-121/tezacaftor/561はTrikaftaよりも高い臨床効果が期待でき、より便利な1日1回の治療法であり、バーテックスにとってロイヤリティ負担が軽減されるものです。CFTRタンパク質が作られず、CFTRモジュレーターの効果が得られない5,000人以上の患者さんのために、当社はパートナーであるModerna社と共同でmRNA治療薬を開発しています。このプログラムのIND取得可能試験は終了しており、2022年後半にINDを提出し、その後臨床開発を開始する予定であることに変わりはありません。
CF以外のパイプラインに目を向けると。まず、鎌状赤血球症とベータサラセミアの機能的治癒の可能性を提供するために設計された当社の遺伝子編集アプローチであるCTX001から始めましょう。CTX001は、2022年末までに米国とEUの規制当局にベータサラセミアと鎌状赤血球症を適応として承認申請する予定であり、これが次の商業的上市になると予想しています。
両方の第3相試験の登録は完了し、現在、両方のプログラムで75人以上の患者さんに投与しています。CTX001については、より長期のフォローアップやより多くの患者さんを含む臨床データを、今年の医学フォーラムで共有できることを楽しみにしています。次に、APOL1を介した腎疾患(AMKD)を対象とするファーストインクラスの低分子阻害剤であるVX-147は、重要な開発段階へと急速に進展しています。12月には、前例のない第2相の概念実証の結果を報告しました。
APOL1が介在する特殊な腎臓病であるFSGS患者において、VX-147の投与により、ベースラインと比較して47.6%のタンパク尿の減少をもたらしました。VX-147は概して良好な忍容性を示しました。VX-147に関連するSAEはなく、すべてのAEは軽度から中等度の重症度でした。1つは、2つのAPOL1遺伝子変異を有し、タンパク尿と腎機能低下を伴う患者を対象とした適応的な第2/3相単一試験デザイン、2つは、米国および欧州の約10万人のAMKD患者を含む幅広い集団におけるVX-147の評価、3つめは、VX-147の臨床的な開発計画について、3月末にFDAと合意して、VX-147の重要な開発を開始しました。
3)中間解析が可能であり、これが良好であれば、米国での早期承認への道筋をつけることができます。3月下旬、ファーストインクラスの非オピオイド系NaV1.8阻害剤であるVX-548が、急性痛に関する2つのフェーズ2試験において、統計的に有意かつ臨床的に意味のある緩和を達成し、当社の高い期待に応えたと発表しました。2つの試験(腹部形成術後および外反母趾切除術後)において、VX-548の最高用量は、主要評価項目であるSPID48(初回投与時から48時間後までの痛みの強さの時間加重和)において、プラセボと比較して迅速、持続的、かつ一貫して痛みの強さを減少させることを確認した。
SPID48スコアの評価において重要なことは、スコアが高いほど痛みの軽減が大きいことを示すということです。VX-548はプラセボに対して、腹部形成術で37.8、外反母趾手術で36.8という統計的に有意な平均SPID48を示し、優越性を示しました。また、本試験の参照群である標準的なオピオイド療法では、プラセボとの平均SPID48の差はそれぞれ12.5および14.7であった。安全性および忍容性の観点からは、VX-548はすべての用量で良好な忍容性を示しました。
VX-548に関連する重篤な有害事象はなく、有害事象の大部分は軽度または中等度であった。有効性と忍容性に優れた非オピオイド系鎮痛剤のアンメット・ニーズが高いことから、当社はVX-548の開発を急ピッチで進めています。私たちの目標は、オピオイドのような依存性や副作用がなく、効果的に痛みを緩和する可能性のある新しいクラスの疼痛治療薬を世に送り出すことです。規制当局との協議を経て、2022年後半にVX-548を急性痛に対する極めて重要な開発段階に進める予定です。
最後に、1型糖尿病プログラム、そして1型糖尿病の患者さんに機能的な治療法を提供する可能性のある、当社の幹細胞由来の完全分化型膵島細胞補充療法であるVX-880についてお話します。米国と欧州だけで、1型糖尿病は250万人以上の患者さんを抱えています。今週初めに発表したように、VX-880プログラムは米国で臨床保留となりました。
を発表しましたが、米国ではVX-880プログラムがFDAにより臨床保留となり、我々は緊急に詳細の把握に努めています。その際、これまでに治療を受けた最初の3人の患者さんの安全性と有効性のデータも共有しました。要約すると、最初の患者さんは、目標量の半分の細胞で治療され、270日目にインスリン自立を達成し、ヘモグロビンA1C値は5.2%となりました。2人目の患者さんも、半分の投与量で150日目まで良好な結果が得られました。
この患者さんは、膵島細胞機能の測定値が堅調に増加し、グルコースコントロールが改善されると同時に、外因性インスリンの使用量が30%減少した。このように、1例目と2例目の半量投与に関しては、VX-880のコンセプトが実証されたことになります。VX-880を初めて全量投与された3人目の患者さんは、29日目のマイルストーンに到達しました。29日目の時点で、この患者はC-ペプチド値の上昇と血糖コントロールの改善という、心強い初期効果を示しました。
本試験では、90 日目に膵島機能および血糖コントロールの詳細な評価が初めて行われます。本プログラム全体では、これまでに投与された3名の患者さんにおいて、VX-880に関連するSAEは発生していません。有害事象の大部分は軽度から中等度であり、全体的な安全性プロファイルは、本試験で使用した免疫抑制レジメンおよび周術期と一致しています。以上が現在までのデータである。
もちろん、3名の患者さん全員について、試験プロトコールに従ったフォローアップが継続されます。米国でできるだけ早く臨床試験を再開できるよう、FDAと建設的かつ迅速に協力し、FDAの疑問点を理解し、対処していきたいと思います。 1型糖尿病の最後に、当社の細胞プラスデバイス・プログラムについて簡単に説明します。販売とデバイスのアプローチについては、引き続き進展しています。
このプログラムでは、細胞を免疫システムから守るために免疫抑制剤を使用する代わりに、免疫保護デバイスがその機能を果たすように設計されています。このプログラムについては、今年後半のIND申請に向けて、引き続き順調に進んでいます。まとめると、バーテックスはCFにおいて著しい成長を続けており、中・後期開発段階にある6つの疾患領域のプログラムで急速な進展を遂げています。そのうちの5つのプログラムは、すでに重要な開発段階にあるか、あるいはこれから臨床に入る予定で、今年後半にはさらに多くのプログラムが臨床入りの予定です。当社は、連続的なイノベーションを推進するための継続的な投資を可能にする強固な財務基盤とバランスシートを有しています。
それでは、スチュアートに話を譲りたいと思います。
Stuart Arbuckle — 最高執行責任者
ありがとう、リシュマ。今夜は、CFにおける当社の継続的で力強い商業的業績、CFにおける将来の成長への明確な道筋、そして新たな疾患領域への拡大計画についてお話しできることを嬉しく思います。バーテックスのCF事業は、米国におけるTrikaftaの安定した業績と、米国外におけるTrikafta/Kaftrioの継続的な堅調な取り込みに牽引され、昨年来の国際的な償還の大きな進展に続き、急速なペースで成長を続けています。
第1四半期のCF製品売上は、治療開始患者数の増加に伴い、前年同期比22%増の21億ドルでした。米国の売上は、2021年半ばの承認後、6歳から11歳の小児を中心にTrikaftaによる治療を開始する患者さんが増えたことが牽引し、9%増の13億7,000万ドルとなりました。米国外での売上は
は2021年第1四半期比55%増の7億2900万ドルで、償還協定を結んだ国々でのTrikafta/Kaftrioの急速な普及に牽引されました。当社は、北米、欧州、オーストラリアにおいて、CFTRモジュレーターの効果が期待できるにもかかわらず、まだ治療を受けていない25,000人以上の患者さんを対象に、本年をスタートしました。これらの患者さんは、主に3つのカテゴリーに分類されます。1つは、主に当社が最近保険償還を受けた国において治療を開始していない患者さんであり、したがって上市の初期段階にあること、2つは、当社がまだ保険償還を受けていない地域の患者さん、3つは、継続中の適応拡大により対応することになる若年層の患者さんです。私たちは、これらの患者さんの大半に、時間をかけてアプローチできると確信しています。
Trikafta/Kaftrioは現在、25カ国以上で販売され、保険償還されています。最も顕著な例はオーストラリアで、12歳以上の患者さんに対してTrikaftaが償還されるようになりました。また、若年層の患者さんへの治療拡大も進んでいます。1月には、欧州と英国で、6歳から11歳までの小児患者を対象としたカフ トリオの承認を取得しました。
の承認を取得しました。また、4月にはカナダ保健省から「トリカフタ」の販売許可を取得しました。米国では、「Orkambi」の1歳~2歳未満の小児に対する承認申請(sNDA)を最近行いました。また、「Trikafta」の2~5歳児を対象とした第3相試験の登録が完了し、米国での承認申請を行う予定です。
この年齢層については、2022年末までに米国での承認申請を行う予定です。Reshmaが述べたように、Trikaftaの強力な実環境での長期にわたる経験は、この併用療法の臨床的価値提案をさらに強化するものです。当社はこれまでにも、当社の医薬品であるKalydeco、Orkambi、Symdekoによる治療が、CF患者さんの疾患進行の特徴の1つである肺機能の低下を遅らせるという証拠を示してきました。今回、Trikaftaで治療した患者さんと未治療のマッチングコントロールの肺機能を経時的に比較したデータを得ました。
そして、これらのデータは、Trikaftaを使用した患者さんが、平均して2年間のフォローアップ期間中に肺機能を全く失っていないことを示しています。一般に、CF患者は毎年1%から3%の肺機能を失うと言われています。WEは、この重要な新データを近々開催される医学フォーラムで発表する予定です。レシュマが述べたように、この6〜12ヶ月は、複数のプログラムが開発後期に到達し、バーテックスにとって目覚ましい期間となりました。
私は、次の商業的機会となり得る開発後期の2つのプログラムについて、いくつかの考えを述べたいと思います。まず、ヘモグロビン異常症に対するCRISPR/Cas9ベースの遺伝子編集治療薬であるCTX001は、年内に承認申請を行う予定となっています。鎌状赤血球症およびβサラセミアに対する商業化および上市準備活動も順調に進行しています。この1年間で、当社は鎌状赤血球とTDTの市場について深く理解し、これらの疾患の患者さんが集中している場所、患者さんを治療に紹介する医師、患者さんの旅を促進する主要な治療センターなどを把握しました。
本年末の申請に向けて、上市準備活動は急速に進展しています。メディカル、コマーシャル、マニュファクチャリングを含む複数の機能において、主要なリーダーシップのポジションとチームが配置されています。米国と欧州の少数の拠点が、重症鎌状赤血球およびサラセミア患者さんの大部分を治療することになります。
当社の調査によると、米国の患者さんの約90%は24の州に居住し、欧州の患者さんの約75%は4カ国に居住していることが判明しています。私たちは、これらの国々で潜在的な施設とその紹介ネットワークを特定しました。米国と欧州では、すでに公的および商業的な支払者に働きかけています。
また、治療期間を通じて患者さんをサポートするため、強固な患者サービスプログラムを開発しています。私たちは、CTX001が患者さんを支援する大きな可能性を見出し続けており、この画期的な治療法を鎌状赤血球症やベータサラセミアの患者さんに提供できる可能性を期待しています。最後に、最近、急性痛を対象とした2つの第2相試験が終了し、両試験で良好なPOC結果が得られたことから、Reshmaが述べたように、今年の後半にはVX-548を急性痛の主要開発段階に進める予定です。ここで、私たちが考える痛みの市場機会について、簡単にご説明させていただきます。
中等度から重度の疼痛治療には膨大なアンメット・ニーズがあり、特に標準的なオピオイドの副作用や習慣性を回避するなど、ベネフィット・リスク・プロフィールを改善した医薬品が求められています。VX-548の最初のターゲット市場である急性痛の市場について少し説明すると、米国では毎年、急性痛の治療日数が15億日を超え、そのうちの多くの割合でオピオイドが処方されています。これらの処方の中には、一部の患者さんに依存症の問題を引き起こし、米国におけるオピオイドの蔓延を助長するものがあることは残念な事実です。 CDCの国立保健統計センターの2021年4月までの最新12カ月間の暫定データによると、米国におけるオピオイドによる過剰摂取による死亡者数は75,000人を超え、前12カ月間と比較して35%増加していると最近推定されています。このような安全性の懸念がない、新規で効果の高い薬物クラスは、非常に大きな可能性を持っています。例えば、NSAIDsから始めてNaV1.8阻害剤にエスカレートし、最後の手段としてオピオイドを処方するというステップセラピーのパラダイムが考えられる。VX-548の最初の適応症は中等度から重度の急性痛で、この分野はVertexの商業化モデルに適した専門市場であると認識しています。
しかし、VX-150が急性痛、神経因性痛、筋骨格系痛で良好なPOCを示したように、このメカニズムは他のタイプの痛みにも適用可能です。今後の電話会議で、これらの適応症の計画についてお話できることを楽しみにしています。私は、世界中のより多くの患者さんに当社のCF薬をお届けするための継続的な進展と、当社の後期開発パイプラインの有望性に非常に期待しています。それでは、チャーリーに電話をお繋ぎします。
チャーリー・ワグナー — 最高財務責任者
ありがとう、スチュアート。バーテックスは、研究開発パイプラインが引き続き重要なマイルストーンを達成し、2022年に素晴らしいスタートを切っており、第1四半期も堅調な財務実績をあげました。第1四半期の製品総売上は21億ドルで、2021年第1四半期と比較して22%増加しました。当社の成長は、昨年、多くの地域で保険償還のアクセスが拡大したことを受け、国際的にKAFTRIOが引き続き堅調に推移したことや、米国でTrikaftaが引き続き成長したことなど、前年と比較して新たに治療を受けている患者が増えたことが主な要因となっています。
当社の2022年第1四半期の非GAAPベースの研究開発費および販売管理費の合計は、2021年第1四半期の5億3,100万ドルに対し、6億8,700万ドルとなっています。前年同期比で費用が増加したのは、研究費の増加と、現在、複数のプログラムが中・後期開発段階にあり、進行中のパイプラインへの投資によるものです。さらに、今年末の薬事申請に向けて、CTX001のプレコマーシャル活動への投資を継続しています。2022年第1四半期以降、当社は、最近同業他社が採用している報告方法と同様に、共同研究、資産買収、第三者の知的財産のライセンスに関連した一時金または偶発的なマイルストーン支払による研究開発費を非GAAPベースの業績から除外しなくなりました。
また、前年度に報告された非 GAAP 型の数値を新しい表示方法と整合させるために更新しました。この変更は非 GAAP 型の数値にのみ影響し、’22 年第 1 四半期および ’21 年第 1 四半期の報告業績に 対する影響は軽微です。当四半期の非 GAAP 型営業利益率は 56%、非 GAAP 型営業利益は前年同期比 16%増の 11 億 7,000 万ドルとなりま した。2022 年度第 1 四半期の非 GAAP 方式の実効税率は 22%でした。
当四半期の現金及び短期投資は82億ドルで、引き続き非常に強固なバランスシートプロファイルを維持しています。次にガイダンスです。2022 年通期の CF 製品売上および非 GAAP 型有効税率に関するガイダンスは、前回発表したものを維持し ています。先ほどご説明したアップフロントとマイルストーンに関する報告の変更を反映し、非GAAPベースの研究開発費と販売管理費の合計に関するガイダンスを調整します。
具体的には、CF製品全体の売上高に関するガイダンスは、84億ドルから86億ドルに据え置きます。中間値では、前年同期比で約10億ドル、12%の増収となります。非GAAPベースの営業費用については、既存または進行中の共同研究からの契約一時金やマイルストーン支払いを含め、28億2,000万ドルから29億2,000万ドルの範囲になると予想しています。最後に、非 GAAP 型の実効税率は、引き続き 21%から 22%の範囲と予想しています。
今年後半から2023年にかけて、当社の継続的な進歩を示す重要なパイプラインのマイルストーンがいくつかあります。これらはウェブキャストのスライド16に記載されています。要約すると、2022年は8年連続で2桁の収益成長に向けて順調に推移しています。CF事業が好調で、CFでのリーダーシップを長期的に維持するための投資を行っています。同時に、変革をもたらす可能性のある医薬品の幅広いパイプラインの進展に伴い、VertexをCF以外の新しい疾患領域へ多様化する道も順調に進んでおり、企業として変曲点を迎えています。
その結果、高い収益性を維持しながら、社内外のイノベーションに多額の再投資を行うことができる当社独自の事業戦略により、当社は長期的にさらなる大きな価値創造に向けて非常に有利なポジションにあります。当年度の進捗に応じ、皆様にさらに情報をお伝えできることを楽しみにしています。それでは、質問をお受けします。
質疑応答
オペレーター
ありがとうございました。それでは、質疑応答を始めさせていただきます。[まず最初の質問は J.P.のコーリー・カシモフ氏です 最初の質問はJ.P.モルガンのコーリー・カシモフです
モルガンです どうぞ
コーリー・カシモフ — J.P.モルガン — アナリスト
素晴らしい。こんにちは。まずはマイケルに、長年にわたる協力に感謝したいと思います。とても感謝しています。
そこで質問ですが、VX-147とAMKDの第3相試験についてです。タンパク尿の減少が48週時点のeGFR曲線の傾斜に重大な影響を与えるという予測的性質に基づいて、早期申請の可能性について確信が持てるかどうか、お聞きしたいのです。ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
147のプログラムについてですが、試験デザインの主な特徴は、単発の第2/3相試験であることです。この試験には、この薬剤の投与対象となりうる10万人の患者さんをすべて登録する予定です。そして、3つ目の特徴は、ご質問の通りです。
48週時点であらかじめ指定した中間解析を組み込んでいます。そして、その解析が良好であれば、早期承認への道筋が示されます。第2相試験で調べたタンパク尿との関係は非常に緊密で、腎機能の指標であるeGFRと高い相関があります。私が中間解析に高い信頼性を持っている理由は、第2相試験で確認されたタンパク尿の減少が、FSGSという非常に特殊で攻撃的なAMKDの型において、前例のない47.6%の減少であったからです。
タンパク尿が47.6%減少したことで、GFRに換算すると、中間解析の信頼度は高くなります。ですから、第2相試験の終了時に、先ほど申し上げた3つの特徴について、当局と合意しておくことが非常に重要だったのです。
Cory Kasimov — J.P. Morgan — アナリスト
非常に参考になりました。ありがとうございます。
オペレーター
次の質問はBank of AmericaのGeoff Meachamからです。どうぞよろしくお願いします。
発言者不明 — バンクオブアメリカ・メリルリンチ — アナリスト
Geoffの代わりのJasonです。質問にお答えいただき、ありがとうございます。四半期決算おめでとうございます。そして改めて、マイケルにおめでとうと言いたいです。
いくつか簡単な質問をさせてください。希少疾病に焦点を当てた場合、疼痛プログラムが商業的ポートフォリオの中でどのように戦略的に位置づけられるかについて説明していただけますか?基本的に、これは潜在的に提携を考えている資産ですか?前進なのでしょうか。それとも、必要な商業的インフラを確立することを検討しているのでしょうか?80の臨床試験中止は、ちょっと驚きでしたね。しかし、遺伝子治療や細胞治療に対して、規制当局が過剰なまでの警戒心を持ち始めているように見受けられます。CTX001の申請に対して、ネガティブなリーディングスルーの可能性はありますか?それとも、規制当局が安全性と有効性のパッケージにかなり満足しているように見えますか?ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
ジェイソン、いくつか質問があるようですね。CTX001について、私たちは試験の勢いに非常に満足しています。CTX001については、試験の勢いに非常に満足しています。準備段階で申し上げたように、登録は完了しました。
75人以上の患者さんに投薬しました。PRIME、RMAT、オーファンなど、利用可能なすべての薬事指定をこことヨーロッパで確保しました。そして、今年末の申請に向けて計画を進めています。疼痛プログラムについては、私から2点コメントさせていただき、スチュアートにもう少し詳しく説明してもらいます。
私たちは、急性痛と神経因性疼痛を完全にVertexianとして捉えています。筋骨格系の痛み、例えば腰痛や膝痛など、筋骨格系に分類されるような痛みについては、同じようには感じません。とはいえ、VX-150による薬理検証や遺伝子検証を踏まえれば、このメカニズムが3つの主要な状態にわたって有効であることを期待しています。スチュアート、商業化についてもう少し詳しく教えてください。
スチュアート・アーバックル — 最高執行責任者(COO
そうですね。ジェイソン、私たちのことを希少価値の高い会社だと誤解している人がいるようですが、Reshmaが説明したように、私たちは希少価値の高い会社ではありません。Reshmaが説明したように、それは私たち自身を定義する方法ではありません。私たちの研究戦略は、ヒトの生態を理解し、レシュマが言ったように、遺伝学的あるいは薬理学的に有効なターゲットが存在し、専門的なインフラでアクセスできる市場にある特定の病気に焦点を当てることです。
私たちは、疼痛がその説明にぴったりだと考えています。Reshmaが言ったように、痛みの市場には、急性痛、神経障害性、慢性筋骨格系など、さまざまなセグメントがあります。急性痛の分野での商機は非常に大きいです。急性痛は、米国だけで年間15億ドル以上の治療日数を占めています。
急性痛は、米国だけで年間15億ドル以上の治療日数を占めています。そして、その処方の90%以上がジェネリック医薬品であるにもかかわらず、その市場規模は40億ドルにものぼります。ですから、オピオイドや他の鎮痛剤のような副作用の心配がなく、オピオイド以上の効能を持つ薬を開発できれば、急性痛の分野で数十億ドル規模のビジネスチャンスがあると考えています。また、Reshmaが言ったように、神経障害性疼痛についても同様に、数十億ドル規模の機会があります。
これも専門性の高い市場であり、専門性の高いインフラを通じてサービスを提供することができます。
発言者不明 — バンクオブアメリカ・メリルリンチ — アナリスト
完璧です。ありがとうございました。
運営者
次の質問は、Truist SecuritiesのRobyn Karnauskasからです。どうぞよろしくお願いします。
Robyn Karnauskas — Truist Securities — アナリスト
わかりました。ありがとうございました。そして、マイケル、あなたが去るのは悲しいですが、すべてのハードワークおめでとうございます。では、いくつか簡単なものを。
AMKDの第3相試験の組み入れ基準についてです。登録はどの程度困難だと思われますか?10万人の患者さんがいるとのことですが、実際に遺伝子型を持つ患者さんは何人いるのでしょうか?実際にジェノタイプを持ち、治療を受けているのは何人ですか?実際にジェノタイプを取得するために、より多くの作業が必要なのでしょうか?2つ目の質問は、CTX001に関するものです。より多くの施設と話をする中で、1つの薬剤に最も適した初期患者となる患者群や、その特徴について、もう少し詳しく教えてください。また、治療を開始する意思のある患者さんのレジストリやリストを作成されているのでしょうか?ありがとうございます。
Reshma Kewalramani — 最高経営責任者兼社長
それでは、まずAMKDについて、次にCTX001プログラムの鎌状赤血球症とβサラセミアの患者について、Stuartさんに解説していただこうと思います。ロビン AMKD試験への参加条件は、タンパク尿と腎機能低下、そしてジェノタイピングによるAPOL1対立遺伝子が2つあることです。実際のジェノタイピング検査は、かなりシンプルです。簡単な血液検査ですが、一般的に行われていないのはご指摘の通りです。
なぜ一般的に行われていないかというと、これまでは、APOL1を介した腎臓病の患者さんに対して、何も提供することがなかったからです。そのため、私たちはこの第2/3相臨床試験にいくつかの特徴を持たせ、私たちが求めるような登録者を確保し、この薬を迅速に提供できるようにしました。1つ目は、米国とEUで多くの施設が稼動しているグローバルな試験であるということです。
もうひとつは、すべての患者さんが標準治療を受けていることです。つまり、この試験に参加するためにプラセボに移行しなければならないような患者さんはいないのです。この試験では、一方の群には標準治療とVX-147を、もう一方の群には標準治療を投与します。そして3つ目は、ジェノタイピングを同時に行う試験で、患者さんはジェノタイピングを受け、希望すれば第2/3相試験に登録することができるのです。
これらの施策は、登録が進むにつれて非常に有用になってくると思います。スチュアートさん、CTX001と患者さんについてお聞きします。
スチュアート・アーバックル — 最高執行責任者
ええ、Robyn、ご質問ありがとうございます。以前にもコメントしましたが、米国とEUには、鎌状赤血球症や輸血依存性サラセミアの患者さんが約15万人いらっしゃいます。しかし、ご想像のとおり、現在の治療法では、CTX001の適応となる患者さん全員がこのような状況にあるとは思えません。
ですから、私たちの研究の対象基準に基づき、また私たちの研究や他の方々の研究、医師が候補となりそうな患者さんのタイプについて話を聞いた結果、15万人のうち約3万2,000人が対象となると考えています。つまり、既存のブスルファンベースの治療法においてCTX001の候補となる可能性があると考えられる患者さんです。
Robyn Karnauskas — Truist Securities — アナリスト
ありがとうございました。
オペレーター
次の質問は、ゴールドマン・サックスのサルヴィーン・リクターからです。どうぞよろしくお願いします。
サルビーン・リヒター — ゴールドマン・サックス — アナリスト
私の質問を聞いてくださってありがとうございます。そして、マイケル、あなたと一緒に働けてよかったです。あなたがいなくなるととても寂しくなります。臨床に関する質問が2つあります。
1つはCTX001についてです。商業的な面では、特にEUでの困難を考えると、ブルーバードによって世界的に支払者の前例がどの程度できているのでしょうか?次に、デュシェンヌ遺伝子編集プログラムについてです。このプログラムについて、もう少し詳しく教えてください。また、これはCRISPRとの提携ですか?ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
サルヴィーン DMDの質問から始めて、CTXの話はスチュアートに任せます。DMDプログラムについては、サルヴィーン、以前にも質問されましたが、ちょっとお待ちください。このプログラムでは、本当に素晴らしい進展がありました。これは遺伝子編集をベースとしたプログラムで、来年のIND計画でIND取得可能な試験を行っています。
Bastianoさん、もう少し詳しく教えていただけますか?
Bastiano Sanna — Vertex Cell and Genetic Therapiesのチーフです。
DMDに対する私たちのアプローチは、他のすべての遺伝子治療アプローチとは少し異なります。なぜなら、私たちは意図的に、ほぼ全長のエキソンスキッピングジストロフィンのアプローチを選択したからです。遺伝子治療のアプローチは、他の文脈では、様々な長さのジストロフィンの切断版を提供するだけですが、それがマイクロジストロフィンと呼ばれるのには理由があります。遺伝子編集は、ほぼ完全な長さのタンパク質を提供できる可能性を持つ唯一のアプローチであり、耐久性のある変革的な機能的治癒に必要なものです。
このプログラムは、エクソニックス社の買収によってもたらされたことを覚えていらっしゃるでしょうか。それ以来、私たちは、私たちの技術の分析開発とプロセス開発の両方に、本当に一生懸命取り組んできました。この分野で起こったことを考えると、私たちは純度や分析開発、プロセス開発といったものに細心の注意を払い、技術的に最高の製品ができるように、科学と一緒に取り組んできました。2023年にINDを申請し、その後すぐに臨床開発を開始することを目指しています。
Stuart Arbuckle — 最高執行責任者
サルヴィーン、革新的な治療と支払いモデルについてですが、これは質問の基本だと思います。ブルーバードで起こったことが、EUやその他の地域で、変革的な一回限りの機能的治療が決して支払われないという前例になったとは思えません。明らかに、ライセンスの取り下げについて、コミュニティには失望があります。しかし、私たちは、上市前の計画の一環として、米国内外の支払者に働きかけています。
しかし、私たちは、上市前の計画の一環として、米国内および海外の支払者に働きかけています。私たちのチームがCFの償還を確保するために示した能力に基づいて、CTX001が持つ変革の可能性を考えると、ライセンス承認が下りるまでは、世界中の患者さんにこの薬を届けることができると楽観視しています。
マイケル・パートリッジ
オペレーター、次の質問の準備ができました。
オペレーター
次の質問は、ジェフリーズのマイケル・イーからお願いします。どうぞよろしくお願いします。
Michael Yee — Jefferies — アナリスト
ご質問ありがとうございました。また、Mikeにも感謝します。本当に感謝しています。APOL1を介した腎臓病について、2つの質問をさせていただきます。1つ目の質問は、第2相の登録に対する自信と、年末にデータを期待するかどうか、それについて何か言えることはあるかということです。患者さんを特定し、患者さんを登録するスピードと自信という点で、フォローアップのようなものになります。
2つ目の質問は、第3相試験に関するもので、eGFRに関するものです。これらの患者さんの一定期間の減少の傾きについて良い考えがあるかどうか、AMKD内の異なる疾患間の不均一性があるかどうか、第3相試験で減少について何を想定しているか、についてです。ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
そうですね。マイク、登録に関してですが、VX-147の登録のダイナミクスについてコメントするのは、本当に早すぎると思います。12月に第2相のデータを発表し、共有したばかりで、第3相はその3カ月後の3月に開始しました。ですから、まだ時期尚早です。
しかし、コメントしたように、ジェノタイピング試験、世界中に開設する試験施設の数、両群で治療を受ける試験であることが、登録に役立つと思います。第3相のGFRの質問ですが、このグループの患者さん、つまりAPOL1対立遺伝子を2つ持つ患者さんは、非常に急速に低下しています。つまり、1年に5CC以上低下しているのです。そのような急速な減少があれば、薬剤の影響を評価する機会が与えられます。だからこそ、この1年間の加速エンドポイントの可能性が本当に重要なのです。
第2相試験で明らかになったのは、タンパク尿の減少です。これは約50%、47.6%の減少です。これは、腎機能の指標であるeGFRと非常に強い相関があり、APOL1対立遺伝子を2つ持つ人の腎機能の指標は、FSGSと呼ぶか他の疾患と呼ぶかにかかわらず、非常に高い数値を示しています。ですから、臨床試験を立ち上げ、実行に移すという点では、私たちは非常に良い状態にあると思いますし、タンパク尿とeGFRの両方に関するエンドポイントの設計についても、非常に良い状態にあると思います。
Michael Yee — ジェフリーズ — アナリスト
わかりました。ありがとうございます。
オペレーター
次の質問はコーウェンアンドカンパニーのフィル・ナドーからです。どうぞよろしくお願いします。
フィル・ナドー — コーウェン・アンド・カンパニー — アナリスト
こんにちは。マイケル、長年の協力に感謝します。次の冒険で幸運を祈る。君がいなくなるのは寂しいよ
私たちから2つ質問をします。まず、簡単なコマーシャルとVX-880についてです。前四半期のコマーシャルでは、在庫の積み増しを訴えていましたね。今回の電話会議では、まだ在庫について言及されていませんね。
前四半期のコマーシャルでは、在庫の積み増しについて言及されていませんでしたが、今四半期の在庫の状況や、在庫調整の有無についてお聞かせください。次に、VX-880についてですが、臨床試験を開始してまだ日が浅いということは理解しています。しかし、FDAが納得していない理由について、何かお分かりになりますか?プレスリリースでは、ベネフィット・リスクがプラスに働くとは考えていないとのことでしたね。それとも、何らかのリスクを懸念しているのでしょうか?次に、VX-880についてですが、米国での臨床試験終了施設が1つありますね。
もうひとつは、VX-880で、米国での臨床試験を終了した施設がひとつあります。米国でホールドされている患者さんの登録を継続するために、人数を増やしたいという希望があれば教えてください。最後に、もちろん、ホールドを解除するために必要な予備的な考えがあればお聞かせください。ぜひお聞かせください。
ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
まずチャーリーに、今期の在庫に関する質問からお伺いします。チャーリー、今期の収益と在庫の見通しについて少しお話いただけますか?
チャーリー・ワグナー — 最高財務責任者
はい、ご質問ありがとうございます。以前にも申し上げましたが、チャネル在庫や患者在庫が四半期ごとに2000万ドルから5000万ドルのオーダーで変動することはまったく珍しいことではありません。第4四半期に在庫が増加したのは、そのためです。
第1四半期には若干の在庫削減がありました。ただ、具体的に呼んでいるわけではありません。
レシュマ・ケワラマーニ — 最高経営責任者兼社長
VX-880に関するご質問ですが、フィル、今週初めにお話ししたことは、私たちが知っていることです。規制により、当局は30日以内に質問リストや情報提供の要請を行うことになっています。私たちはこのプログラムに大きな自信を持ち、1型糖尿病に深くコミットしています。そして、できるだけ早く米国での臨床試験を再開できるよう、当局と建設的かつ迅速に協働していきたいと考えています。
と述べています。ご指摘のとおり、現在、米国とカナダの2つの地域で試験が進行中です。カナダでは、現在も試験が進行中です。
カナダ保健省からは、疑問や懸念について何も言われたことはありません。また、追加施設の開設については、常に計画されていることです。米国での保留とは何の関係もありませんし、いずれはさらに拠点を増やすつもりです。
Phil Nadeau — Cowen and Company — アナリスト
それはとても助かります。ありがとうございました。
オペレーター
次の質問はUBSのColin Bristowからです。どうぞよろしくお願いします。
コリン・ブリストウ — UBS — アナリスト
どうも、ありがとうございます。こんにちは、コリンです。四半期決算おめでとうございます。マイケル、ありがとうございます。
DavidとReshma、私たちは以前、AbbVieの読み上げの前に話をしましたが、あなたは競合他社の情報をどれだけ集めてきたかについて話し、それが最終的にAbbVieのトリプレットが脅威にはならないという確信を与えてくれたのですね。明らかに、これは的を得ていました。次世代補正剤について、初期の考えや洞察があったのかどうか、気になります。臨床に進める予定なのは、アッヴィー576だと思います。また、競争相手としては、NBD1ドメインをターゲットとする資産を持つAffinia Therapeuticsについて、最近いくつか報道されていました。
このアプローチについても、ぜひご意見を伺いたいと思います。ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
そうですね。まずはコリンから、それからデビッドに少しコメントをお願いします。Colin、私は競合他社に直接話しかけません。それは私のやり方ではありません。
しかし、一般的なCFについてお話ししましょう。長年にわたり、私たちはCFのリーダーとしての地位を確立し、それを維持するだけでなく、拡大してきました。そして、可能であればトリカフタよりも効能の高い医薬品を前倒しで提供し、最後の5,000人の患者さんには絶対に核酸医薬を前倒しで提供するという、私たちの目標は変わりません。トリカフタは今日の標準的な治療法です。
そして、トリカフタの最も近い競合品は、これまでも、そして今も、私たちのVX-121/561/tezacaftorです。私たちの分子とHBEアッセイになぜこれほどまでに自信があるのか、Davidに少しコメントしてもらいたいと思います。デイビッド、私たちの自信について、また、なぜ私たちが研究室で何かを得たとき、それが臨床に反映されることを知っているのか、少しコメントをお願いします。
David Altshuler — エグゼクティブ・バイスプレジデント、グローバルリサーチ担当、チーフサイエンティフィックオフィサー
その通りです、Reshma。長年にわたってご覧いただいているように、バーテックスによるHBEアッセイの展開は、何度も何度も、臨床的な関連性と臨床結果を予測することが証明されています。カリデコ、オカンビ、シンテコ、VX-445、トリカフタ、そしてVX-121では、HBEアッセイで塩化物輸送の改善が見られました。また、ご記憶の通り、第2相試験で汗の塩化物も改善されましたし、FEV1の変化など、非常に有望な特性も確認されました。
ですから、私たちはこの試験法を本当に信じていますし、それを実証してきました。トリカフタだけでなく、第3相試験中のVX-121を上回る低分子化合物の開発を続けています。VX-445に対抗しうる最も有望な分子は、私たちの121トリプルと、それを超えるものであると信じています。
Colin Bristow — UBS — アナリスト
ありがとうございます。
オペレーター
次の質問はWells FargoのMohit Bansalからです。どうぞよろしくお願いします。
Mohit Bansal — Wells Fargo Securities — アナリスト
素晴らしい。私の質問を聞いてくださってありがとうございます。そして、改めておめでとうございます。糖尿病プログラムについて、いくつか質問させてください。最初の患者さんの270日目のC-ペプチド値についてコメントいただけますか?150日目以降に増加が見られましたか?また、C-ペプチドのプラトー効果を期待できるのはいつ頃でしょうか?そして、最後に関連することとして、最終的にインスリン自立につながるような、これらの患者の目標C-ペプチド値をお持ちですか?ありがとうございました。
Reshma Kewalramani — 最高経営責任者兼社長
そうですね。本当にいい質問ですね。質問を少し組み替えて、バスティアーノにコメントをもらうつもりですが、このことをきちんと説明しておきたいと思います。患者さんがインスリン依存症でないことを知るには、実はとても厳しい基準があるんです。
その厳しい基準とは、もうインスリンを打っていない、外来インスリンを打っていない。空腹時グルコースレベルが126未満で、食後グルコースレベルが180未満であることです。このような条件をすべて満たしているからこそ、患者No.1をインスリン非依存型とすることができるのです。
さて、効果の持続性という点で、何を期待するかという良い質問がありました。死体移植の経験、私たちの細胞の量と質、そして私たちのアプローチがなぜ耐久性があり、長期的に持続するアプローチであると考えるかについて、Bastianoに話を譲りたいと思います。バスティアーノ?
Bastiano Sanna — Vertex Cell and Genetic Therapiesのチーフです。
ありがとう、Reshma。この問題で本当に重要なこと、つまり私たちの細胞の品質と性質についてお話しすることができます。私たちの細胞は完全に分化しており、自然に発生するベータ細胞と見分けがつきません。つまり、両者は共通の生物学的特徴をもっているのです。
ベータ細胞の生物学についてわかっていることは、まず、その数と分化度に関してはほぼ決まっていて、つまり、一生使えるということです。それが、この細胞について知られていることです。患者さんが免疫抑制療法をきちんと行い、移植が成功した場合、この細胞は非常に長い間持ちこたえることができるのです。ですから、私たちの細胞は、同じ生物学であり、死体移植という同じような治療法のもとで、天然のベータ細胞と同じように、一生使える可能性があると信じています。
となると……。
Reshma Kewalramani — 最高経営責任者兼社長
それは[聞き取れず]だったと思います。
Mohit Bansal — Wells Fargo Securities — アナリスト
ありがとうございます。
Reshma Kewalramani — 最高経営責任者兼社長
もちろんです。
オペレーター
次の質問はBMOキャピタル・マーケッツのエヴァン・セイガーマンからです。どうぞよろしくお願いします。
エヴァン・セイガーマン — BMOキャピタル・マーケッツ — アナリスト
こんにちは、皆さん。私の質問を受けてくださってありがとうございます。マイケル、長年の間、ありがとう。あなたがいなくなるととても寂しくなります。
チャーリー、あなたにも一つ。為替が北米の売上に与える影響についてお聞かせください。準備書面では何もおっしゃらなかったと思いますが。償還が拡大しているにもかかわらず、ガイダンスを引き上げなかったのは、そのことが影響しているのでしょうか。
チャーリー・ワグナー — 最高財務責任者
はい。エヴァン、ご質問ありがとうございます。繰り返しになりますが、収益のガイダンスを84億ドルから86億ドルとし、今年も非常に好調な年になることを改めてお伝えしておきます。これは2021年を10億ドル上回り、12%の成長率です。
ガイダンスの再提示にあたり、私たちはいくつかの点を検討しました。オーストラリアはもちろん、今年に入ってからの良いニュースです。また、為替による在庫の変動なども考慮しましたが、これは非常に緩やかな逆風となりました。これらを総合すると、ガイダンスの下限と上限の間にある2億ドルの範囲に正確に収まっていると考えています。
エヴァン・セイガーマン — BMOキャピタルマーケッツ — アナリスト
素晴らしい。それから、FXの影響もありませんし、もう少し話していただけますか?
チャーリー・ワグナー — 最高財務責任者
ええ、かなり控えめです。当社は非常に積極的かつ効果的なヘッジ・プログラムを導入しており、為替変動の影響をある程度和らげています。
そのため、為替による影響は、12%の成長率というベースラインでは、同業他社に比べて非常に小さく、控えめなものとなっています。
エヴァン・セイガーマン — BMOキャピタルマーケッツ — アナリスト
素晴らしい。ありがとうございます。ありがとうございました。
マイケル・パートリッジ
オペレーター、もう1つ質問の時間があります。
オペレーター
次の質問は、Evercore ISIのLiisa Baykoからお願いします。どうぞよろしくお願いします。
Liisa Bayko — Evercore ISI — アナリスト
マイケルの努力に感謝するのは、私が最後になると思います。そして、これからもよろしくお願いします。
マイケル・パートリッジ
そうですね。ありがとうございました。
Liisa Bayko — Evercore ISI — アナリスト
1型糖尿病の指標について、もう少し詳しく知りたいのですが。例えば、患者2の90日目のHBA1cの数値がわからないんです。それがどのように追跡されているのか、確認できればと思います。外来患者からの流入が減ったというニュースは知っているので、それはいいことです。
それから、C-ペプチドについて言及しなかったのは、まだ適切なレベルに達していなかったということでしょうか。ピークシミュレーターも、いくつかのエンドポイント(これらの時点)では表示されなかったので、ちょっと気になるんです。ですから、この穴埋めをしたいだけなのです。
Reshma Kewalramani — 最高経営責任者兼社長
そうですね。もちろんです。Liisa 今日までに投与した3人の患者さん全員について、かなりの量のデータを共有しました。最初の2人は半量投与で、最初の全量投与の患者さんは30日目のマイルストーンにいます。有効性に関しては、すべての患者さんにおいて、非常に優れた有効性が確認されています。
そして、1人目の患者さんについては、270日目まで投与し、インスリンから自立しています。しかし、ヘモグロビンA1c、C-ペプチド値、刺激・空腹時値、CGM(持続グルコースモニタリング)データ、そしてもちろん安全性など、すべての詳細について、今年の学会で発表することを期待しています。
もちろん安全性についても、今年の学会で発表する予定です。
Liisa Bayko — Evercore ISI — アナリスト
わかりました。素晴らしい。それから、もう1つだけ質問させてください。すみません、先ほど聞き逃したかもしれませんが、CTX001について、FDAに提出する必要があるものは確定しているのでしょうか?それから、データを発表する場所、次のデータを発表する場所の目安を教えてもらえると助かります。
ありがとうございます。
Reshma Kewalramani — 最高経営責任者兼社長
CTX001については、昨年の欧州血液学会で、確か22人の患者に関する最後のデータを発表しました。現在、75人以上の患者さんに投与しています。そのため、かなり多くの情報を持っており、今年の次の学会ではそれを見ることができると期待しています。
当局へのデータ提供については、これまで述べてきたように、当局との協議を完了させる必要があります。その中で、2つの未解決の論点は、申請資料で確認したい患者数とフォローアップ期間です。私たちはRMATやオーファンなどの指定をすべて受けているのはご存知の通りです。だから、私たちはこの時点に至るまで会話をする機会を持ちました。
現在は、米国とEUの両方との会話をまとめ、数字と期間に関する議論を終えているところです。
Liisa Bayko — Evercore ISI — アナリスト
素晴らしい。市場についていろいろとお聞きになったようですが、市場は比較的集中しているように見えます。現在のシナリオで年間何人の患者を治療できるのか、キャパシティはどの程度なのか、どのように考えればよいのか、おわかりでしょうか。
レスマ・ケワラマニ(Reshma Kewalramani) — 最高経営責任者兼社長
そうですね。Liisaさんは、米国とEUで、CTX001の治療を受けられる患者さんのベッドのキャパシティをどのように見ているかということを尋ねておられるのだと思います。時間がないので、手短に説明します。
スチュアートとそのチームは、この地図を作りました。EUでこの治療法の適応となる患者さんの圧倒的多数が、4つの国に集中しています。米国では、この治療法の対象となる患者さんの圧倒的多数が25州以下に集中しており、その患者さんが治療を受けるであろうセンターを地図上に示しました。
そして、そうです。私たちが期待している数の患者さんが、適切な専門知識を持つ施設で治療を受けられるようになることがわかりました。
Liisa Bayko — Evercore ISI — アナリスト
ありがとうございました。
オペレーター
これで質疑応答は終了です。最後に、マイケル・パートリッジ氏からご挨拶をいただきたいと思います。どうぞよろしくお願いします。
マイケル・パートリッジ
ありがとうございます。皆さん、今夜はありがとうございました。また、たくさんの温かいお言葉をありがとうございました。バーテックスを代表することは名誉であり、特権であり、また、皆さんといつも交流できることは楽しいことです。
また、いつも皆さんと接することができ、とても嬉しく思っています。お元気で、そして良い夜をお過ごしください。
以上です。他の翻訳希望があればご連絡いただければ検討いたします。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>


