バイオンテック (NASDAQ:BNTX)2022年第1四半期決算説明会の日本語訳です。
COVID-19ワクチンのmRNAワクチンの開発で一気に株価を上げましたが最近では下落傾向です。mRNAワクチンの技術は素晴らしいと思いますがCOVID-19ワクチンの需要は今後下がって行くことから他での売り上げがないと株価を維持するには厳しいと思われます。
がん領域での開発成功などのニュースがないと今後も上げて行くには難しそうですね。
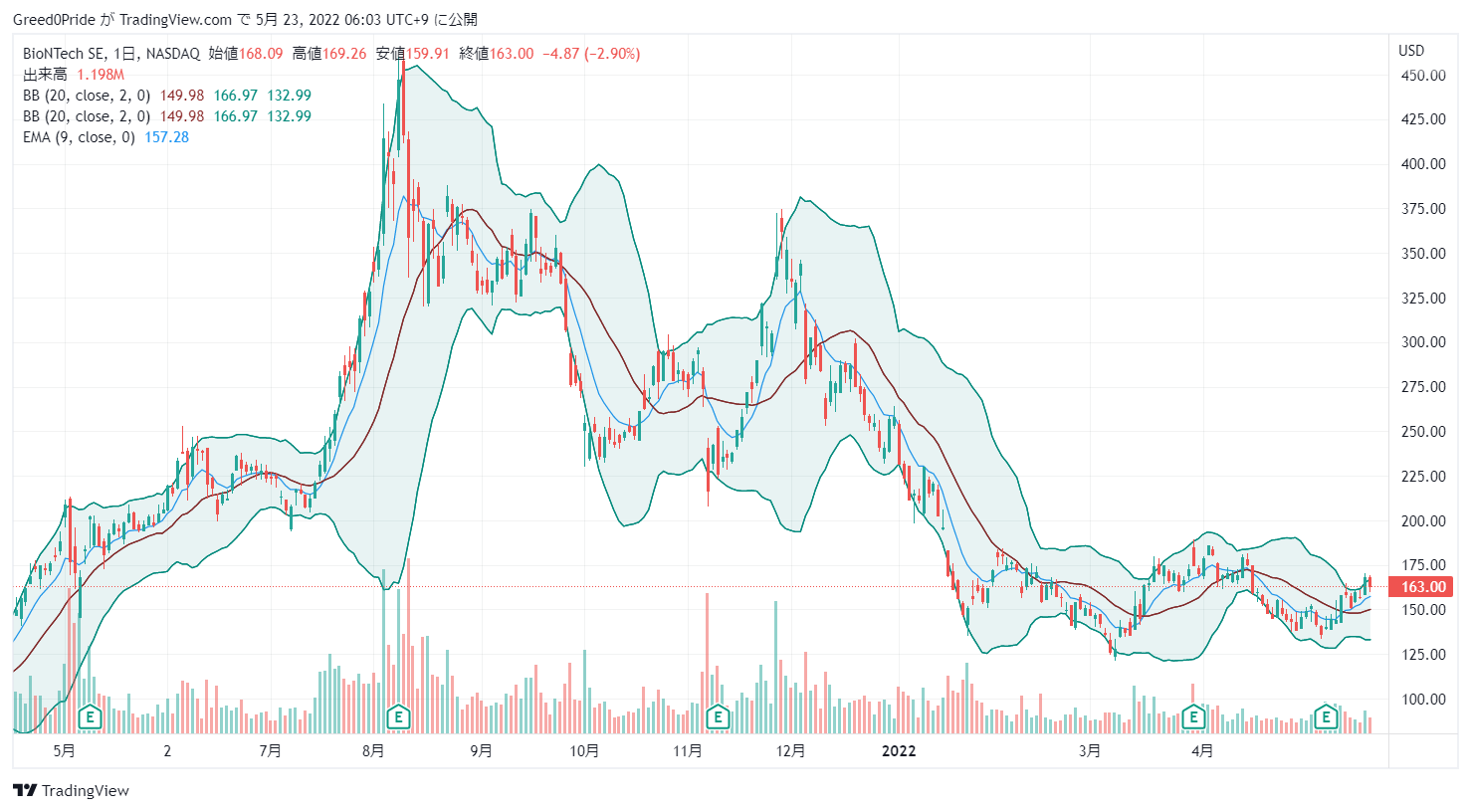
バイオンテック (NASDAQ:BNTX)株価
バイオンテック (NASDAQ:BNTX)2022年第1四半期決算説明会
Call participants:
Sylke Maas — VP Investor Relations
Uğur Şahin — Chief Executive Officer
Ozlem Tureci — Chief Medical Officer
Jens Holstein — Chief Financial Officer
Ryan Richardson — Chief Strategy Officer
Matthew Harrison — Morgan Stanley — Analyst
Cory Kasimov — J.P. Morgan — Analyst
Christopher Zopf — Goldman Sachs — Analyst
Akash Tewari — Jefferies — Analyst
Daina Graybosch — SVB Leerink Partners — Analyst
Shu Zhiqiang — Berenberg Capital Markets — Analyst
Unknown speaker
More BNTX analysis
2022年5月09日午前8時00分
オペレーター
BioNTech 2022 年第 1 四半期アップデートコールへようこそ。電話を投資家向け広報・戦略担当副社長のシルケ・マースに引き継ぎたいと思います。シルケさん、どうぞよろしくお願いします。
シルケ・マース — 投資家向け広報担当副社長
バイオテックの2022年第1四半期の臨床およびオペレーションの進捗と財務結果を確認するため、本日はご参加いただきありがとうございます。始める前に、いくつかのハウスキーピングアイテムをご紹介します。ウェブキャストに添付されているスライドと2022年第1四半期のプレスリリースをご利用ください。どちらも今朝発行されたもので、当社ウェブサイトの投資家向けセクションに掲載されています。
本日のプレゼンテーションのスライド2にあるように、私たちはいくつかの将来見通しに関する記述を行います。これらの将来予想に関する記述には、当社のパートナーから提供された予備的推定値に由来する数値を含む当社の現在のCOVID-19ワクチンの収益、2022年の当社の推定業績、当社のCOVID-19ワクチンに対する世界的需要の継続、2022年とそれ以降の当社の目標ワクチン生産能力、などがありますが、これらに限定されるものではありません。当社のCOVID-19ワクチンを供給する当社の能力、当社のパイプライン・プログラムにおける計画された次のステップ、当社の前臨床試験および臨床試験からのデータの登録、開始、完了および報告の時期、当社の製品候補の規制上の承認の取得および維持の時期ならびに当社の能力、その他米国証券取引委員会への当社の提出書類に記載されているリスクなどです。 また、Form 20-Fを含む米国証券取引委員会への提出書類に記載されたその他のリスクもあります。また、スライド3および4には、当社のワクチンCOVID-19に関する詳細かつ重要な安全性情報が記載されています。最後に、スライド5で本日の電話会議のアジェンダをご覧いただけます。本日の電話会議に参加しているBioNTechの経営陣のメンバーを紹介させていただきます。本日は、CEO兼共同創業者のウール・シャヒン、最高医学責任者兼共同創業者のオズレム・トゥレシ、最高財務責任者のイェンス・ホルスタイン、最高戦略責任者のライアン・リチャードソンにご出席いただいています。
それでは、Uğur Şahinに代わって、通話を開始したいと思います。
Uğur Şahin — 最高経営責任者
シルケさん、ありがとうございます。おはようございます、そしてこんにちは、参加者の皆様を暖かくお迎えいたします。そして、今後ともよろしくお願いいたします。本日は、第1四半期の主なハイライトと今年の目標について概要をご説明します。
詳細は当社チームからご説明し、その後、質問をお受けします。スライド6より 当社の特徴について少しお話しさせていただきます。当社のビジョンは、免疫系を利用して人間の病気と闘うことです。
COVID-19のパンデミックへの対応は、当社初の承認製品によって10億人をはるかに超える人々を守るのに役立つという、またとない機会を与えてくれました。また、次世代の免疫療法を患者さんに提供するという長期的なビジョンに向けた前進を加速させる歴史的な機会でもありました。当社は、バイオ医薬品の開発において、探索研究、トランスレーショナル・リサーチ、開発、GMP製造、商業機能を完全に統合した能力を有しており、成功に向けて非常に有利な位置にあります。技術にとらわれない、ソリューション重視のマルチプラットフォーム戦略を追求し、さまざまな新技術をカバーするイノベーションエンジンを構築しています。
当社は、がんや複数の感染症におけるアンメット・メディカル・ニーズに応えるため、多様な免疫療法の製品パイプラインを推進しています。私たちは、グローバルな社会的責任を果たすことを使命とし、21世紀の免疫療法大国を築き上げます。私たちは、グローバルヘルスにポジティブなインパクトを与え、最先端の医薬品へのアクセスを民主化することを目指しています。第1四半期のハイライトは、スライド7にまとめました。
2021 年の好調な第 4 四半期に続き、2022 年第 1 四半期も堅調な業績を維持しました。第1四半期は、総収益64億ユーロを計上しました。当社は、ドイツ連邦共和国との間で、2027年まで続く初のパンデミック対策契約を締結しました。この枠組み契約は、ドイツにおける新たな状況下でのmRNAワクチンの開発・製造・供給を含むパンデミックへの備えを目的としたものです。
また、当四半期には、社内のイノベーション・エンジンを補完するための共同研究契約を締結しました。Matinas 社との提携では、当社の mRNA ワクチン開発に関する専門知識と Matinas 社の脂質ナノ結晶のデリバリー・プラットフォーム技術を組み合わせ、他のすべてのワクチンに対する製剤の可能性を含む mRNA ワクチンの新規製剤を開発します。リジェネロン社とは、進行性非小細胞肺がんを対象に、FixVac候補のBNT116とLibtayoを併用した臨床試験を共同で実施する予定です。世界中の人々の健康と経済に与える当社の影響は、2022 年も継続します。
当社は、第1四半期末までの2022年における当社のCOVID-19ワクチンのグローバルでの請求量は約7億5,000万回分となっています。また、より多くの人々への投与に関して、最近、いくつかの認可を取得しました。小児用ワクチンの適応症では、5歳以上の小児への接種と5歳以上のブースターが複数の地域で追加されました。がん領域では、当社初のリボマブプログラムであるBNT141が、1月に固形がんを対象としたファーストインヒト試験を開始しました。
BNT141は、タンパク質18.2を標的とするmRNAエンコード型IgG抗体です。4月には、AACR年次総会で、固形がんを対象とした次世代CLDN6標的CAR-T細胞、BNT211の第1/2相試験において、評価可能な14名の患者から得られた有望な予備的臨床データを発表しました。CAR-T細胞の投与量が少ない患者さんでも抗腫瘍効果が確認され、CLDN6を標的としたCARVacの有効性が示されました。スライド8
パンデミックの発生以来、当社は175以上の国と地域の人々に約34億回分のコモナリティを提供し、COVID-19との闘いにおける当社の確固たる地位を示しています。2022年末までに低・中所得国に合計20億回分以上を届けるという公約の達成に向け、今後も順調に進んでいます。COVID-19の先を行くために、私たちはワクチンの革新と最適化を続けています。今年は、毎日の家賃を必要としないReady-to-Use製剤を導入し、その後マイナス90℃からマイナス60℃で保管することで保存期間を9カ月から12カ月に延長する承認を取得しました。
さらに小児への表示を拡大するために、5歳から12歳未満の小児におけるブースターの承認申請を行いました。この申請は、この年齢層で初回投与時に中和抗体を6倍に増加させるという、最近のポジティブなデータによって裏付けられています。また、生後6カ月から5歳未満の小児を対象とした一次投与レジメンの評価も行っており、今後数週間のうちにデータが得られる見込みです。パンデミック対策への取り組みの一環として、当社はこの新しい研究を、世界中で入手可能なシークエンスデータを分析し、SARS-CoV-2の高リスク分散を予測する早期警告システムに共同で行っています。
この警告システムにより、データに基づいた方法で、当社のワクチン製品候補を迅速に適応させることができます。変異に対する先制アプローチの一環として、当社は現在、包括的な開発プログラムを実施しており、変異適応型ワクチンを含む複数のCOVID-19ワクチンの後続品および次世代ワクチンの評価を行っています。また、ワクチン接種後のブースターやインフルエンザ感染後の免疫プロファイルを調査する研究プログラムも開始しています。この研究プログラムは、私たちのワクチン開発戦略に活かされています。
冒頭の挨拶の最後に、スライド9に示すように、私たちは、免疫療法の新しい時代を複数の方法で切り開くことができると信じて、差別化されたパイプラインを構築しています。当社のCOVID-19ワクチンプログラムは、医療を変革するという当社のビジョンに沿って、パイプラインを拡大し、市場に向けて加速するための位置づけとなる、当社の変革を可能にしています。がん領域では、5つの無作為化第2相試験を含む16のプログラムが20の臨床試験で進行中です。感染症領域では、進行中の第1相臨床試験1プログラムと10以上の前臨床試験プログラムがあり、そのうちの4つは今年中に臨床試験を開始する予定です。
当社は、今後3年から5年の間に、がんおよび感染症分野で複数の新製品を上市することを目標としています。当社の技術革新エンジンは、現在の中核疾患であるがんや感染症以外にも、幅広い疾患に対応できる可能性を持っていると考えています。現在、新たな疾患領域で複数のプログラムが進行中で、リード候補の選定段階にありますが、当社の技術をこれらの新領域に進めることは、バイオテックの未来を広げ、長期的なビジョンをサポートすることになるでしょう。それでは、Ozlemに電話を回します。
オズレム・トゥレシ — 最高医学責任者
ウグルさん、ありがとうございます。本日、皆さんとお話しし、パイプラインの最新情報を提供できることを嬉しく思います。スライド11にある当社のCOVID-19ワクチンの研究開発戦略は、ランドスケープ・リサーチ、プロダクト・リサーチ、プロダクト・デベロップメントという3つの柱から成り立っています。ランドスケープ研究では、ワクチンや感染症によって誘導される免疫の中で、ウイルスがどのように進化していくかを解明することを目的としています。
私たちは、ワクチン接種の継続的なブースターの繰り返しと、懸念されるさまざまな変異体への感染によって、免疫力が時間とともにどのように形成されるかを研究しています。私たちが継続的に収集しているデータは、パンデミックに対する私たちの進化した対応に情報を提供するものです。最近の研究により、私たちの理解はさらに深まり、次世代ワクチンの開発において極めて重要なものとなる可能性があります。このデータは、ハイレートジャーナルに査読を申請し、プレプリントサーバーで公開されています。
本研究では、オミクロン感染が免疫に与える影響を明らかにするため、当社のオリジナルワクチンを2回または3回接種した後に、オミクロンに破たん的に感染した人の割合を評価しました。その結果、ワクチン接種者がオミクロンスパイクに曝露することで、オミクロンBA.1に対する中和活性のみならず、BA.2のみ、SARS-CoV-2の過去の変異体、さらにはSARS-CoV-1に対しても広く免疫を増強することが明らかになった。オミクロン・ブレイクスルー感染は、オミクロン特有の抗原に対して、新しいB細胞を誘導するよりも、異なる変種によって広く共有される抗原を認識する記憶B細胞の拡張を中心とした、幅広いB細胞リコール反応を媒介した。これらの結果は、過去のワクチン接種によって免疫応答が刷り込まれた可能性があるにもかかわらず、異なる株のスパイクタンパク質に曝露することによって、形成前のB細胞記憶プールが再集中し、定量的にリモデルされる可能性があることを示唆している。
これにより、以前に確立した中和抗体反応を回避する変異体の中和が可能になると考えている。また、この観察結果は、オミクロン株のスパイクに適応したワクチンも同様にB細胞記憶のレパートリーを再構築する可能性があり、したがって、元の株に対する既存のワクチンによる長期のブースターシリーズよりも有益である可能性を示唆しているのかもしれない。また、このデータは、先祖株ワクチン経験者がオムロンスパイク一価ワクチンを接種することで、同様の株間免疫が得られることを示唆していると考えています。BNT162b2の承認以来、COVID-19を予防するためのさまざまな後続ワクチンや新規の次世代ワクチンを検討し、将来直面するかもしれない課題に備えるために、非常に強力な製品研究に取り組んでいます。
これらは現在開発中であり、いくつかのプロジェクトは今年中に臨床に移行する可能性があります。私たちは、単価および多価ワクチン、T細胞増強アプローチ、汎コロナウイルスカバーワクチンのコンセプトについて評価しています。当社の景観研究は、現在、オミクロンとそのトップラインの出現によるワクチン適応の必要性に対応することに重点を置いている当社の製品開発戦略に役立っています。当社の臨床プログラムは、複数の臨床試験において様々な変異型適応型ワクチンの安全性、忍容性、免疫原性を評価するもので、現在進行中です。
これらの試験から得られた新たなデータは、今後数週間のうちに規制当局と検討・協議され、単変種または二変種の適応型ワクチン製品候補の適切な規制当局への対応を決定する予定です。スライド12は、オミクロン・バリアントに対する包括的な臨床反応戦略を示しています。私たちは、例えば18歳から55歳の個人を対象に、単変量オミクロン適応型ワクチンのさまざまな投与スケジュールを調査しており、二変量アプローチも評価しています。これらの試験から得られるデータは、今後数週間のうちに利用可能になると考えています。
現在、オミクロン適応型ワクチンの有用性に関する規制当局のコンセンサスはありませんが、臨床的に意義のあるデータが入手可能になれば、規制当局の動向も変わってくるものと思われます。データを待つ間、私たちは、私たちのワクチンがCOVID-19の現行および新興の変異体に対する強固な防御を提供することを確実にするために、技術と製造工程を適応させる準備を続けています。スライド13では、高価ながん領域のパイプラインを紹介しています。これは、当社の包括的で革新的なマルチモダリティのツールボックスと、2021年および2022年を通じての重点的な実行の結果です。
私たちは、腫瘍細胞を直接標的とするか、腫瘍に対する免疫反応を調節することによって、補完的な戦略を用いる可能性のある、異なる免疫治療様式にわたって開発中の複数の資産を有しています。当社の製品候補の多くは、当社のパイプライン資産と組み合わせることが可能です。当社のがん領域のパイプラインには、4つの異なる薬物クラスにわたる合計16の製品候補があり、現在進行中の20の臨床試験(うち5つは無作為化第2相臨床試験)において、その効果を検証しています。2022年は、パイプラインの継続的な進展と拡大、および進行中の試験からのさらなるデータの読み出しが期待されます。
2022年は、スライド14のように、複数の腫瘍種を対象とした5つの第2相臨床試験において、集中的に実行する年になると考えています。まず、当社の既製のmRNAワクチン免疫療法プラットフォームであるFixVac、抗PD-1抵抗性の再発進行性メラノーマで評価中のBNT111、皮膚メラノーマ患者の90%以上をカバーする腫瘍抗原を評価する2つの第2相臨床試験が進行中です。当社のアプローチは、抗PD-1と併用することで、治療成績を改善する可能性があります。当社は、このプログラムについて、FDAのファストトラックおよびオーファンドラッグの指定を受けています。
HPV-16のオンコプロテインE6とE7を含むBNT113は、HPV-16陽性でPD-L1陽性の頭頸部がんを対象に、抗PD1との併用で評価中です。次に、パートナーであるジェネンテック社と共同で、2つの個別化ネオアンチゲンベースのワクチンプログラム(iNeSTプログラム)を進めています。自己遺伝子のセブメロンまたはBNT122を評価する第2相試験で、一つはフロントラインのメラノーマで、一つは大腸癌で、アジュバント環境での評価を行っています。メラノーマの試験が成功し、規制当局に受け入れられれば、抗PD-1療法に未適応の進行がんにおいて、抗PD-1と併用したフロントライン治療としてiNeSTを使用する可能性を解除することができます。大腸がんでは、再発の主な原因となる標準治療後に残存するがん細胞への対処を目指します。
最後に、パートナーであるジェネンテック社と共同開発しているバイスペシフィック抗体BNT311は、難治性・再発性非小細胞肺がんを対象とした第II相試験を実施中です。この次世代免疫療法は、PD-L1阻害と同時に条件付き4-1BB共刺激を行い、腫瘍をターゲットにT細胞やナチュラルキラー細胞の機能を高めることを目的としています。次に、スライド15をご覧ください。先日、AACR年次総会において、当社の次世代CAR-T細胞プログラムであるBNT211の有望な有効性と安全性に関するデータを発表しました。
BNT211は、作用機序が相補的であると考えられる当社の2つのプラットフォーム、CLDN6 CAR-T細胞と、他のがんワクチンプログラムに使用されている当社のリポプレックス技術に基づくCARVacと呼ばれるCAR-T細胞増幅型ワクチンを組み合わせたものです。つまり、これらのCLDN6 CAR-T細胞は、胚性腫瘍特異的抗原CLDN6の通過に対して高い感度と特異性を持つ第2世代のキメラ型アンドロゲン受容体を備えているのです。CLDN6は、成人の組織で重く発現していますが、医療ニーズの高いがんで頻繁に発現しており、この腫瘍抗原はCAR-T細胞治療の理想的な候補となります。前臨床試験において、CARVacは、移植されたCAR-T細胞の生体内での増殖を促進し、その持続性と有効性を高めることが実証されています。
BNT211は、固形がんの患者さんにおけるCAR-T細胞の限界を克服することを目的としています。現在進行中のヒトでの第1/2相試験では、CLDN6陽性の再発または難治性の進行性固形がん患者を対象に、CLDN6 CAR-T細胞の単独療法およびCARVacとの併用療法の安全性と有効性を評価しています。CAR-T細胞のCLDN6の3つの用量レベルと単剤療法の用量拡大、および固定用量のmRNAワクチンとの併用療法を試験しています。その後の用量拡大コホートでは、卵巣がん、精巣がん、子宮内膜がん、また肉腫など他の希少なCLDN6陽性のがん種の患者さんが含まれる予定です。
スライド16は、AACRのデータの要約です。発表では、CLDN6 CAR-T細胞を単独で、7人に1回、8人に1回と2種類の投与量で、リンパドレナージ後にCARVacと併用した前治療の多い患者16人のデータが紹介されました。腫瘍の適応は、精巣がん8名、卵巣がん4名、子宮内膜がん、卵管がん、緑内障、胃がんが各1名でした。その結果、CAR-T細胞および単剤療法ともに忍容性の高い安全性プロファイルが示され、CARVacと併用した場合には、8名の患者さんにサイトカイン放出症候群グレード1~2が発生しましたが、トシリズマブで管理可能であり、神経毒性の兆候は認められませんでした。
これまでのところ、2つの用量制限毒性が観察されましたが、管理可能であり、患者さんは完全に回復しています。1つは、併用療法において用量レベル2で観察された血球貪食性リンパ組織球症です。もうひとつは、単剤治療のコホートで用量レベル2で観察された、高用量化学療法を最近終了した精巣がん患者および自家移植患者における長引く細胞減少症でした。の既往のある精巣癌患者において細胞減少の長期化を避けるため、その後、リンパ節除去化学療法を減らした新しいコホートが選択されました(聞き取れず)。
最大耐量はまだ達成されていません。有効性の予備データでは、全疾患制御率が86%、全奏効率が43%で、精巣がんおよび卵巣がんの患者さんでは部分奏効が認められるなど、臨床活性の有望な兆候が認められました。精巣がんの患者さん5名に1~10~8種類のCAR-T細胞投与量を投与したところ、客観的奏効率が80%、病勢コントロール率が100%と、心強い効果が認められました。完全奏効が1名、部分奏効が3名、病勢安定が1名でした。
このサブ解析には、さらに患者数を減らしたレジメンを受けた部分奏功の患者さん1名が含まれています。CARVacの添加は、CAR-Tの生着をサポートし、併用投与を受けた患者の生理学的拡大および生存経路のアップグレード制御を媒介しました。また、時間とともに反応が深まり、一部の患者ではCAR-Tの長期持続が認められ、CAR-Tの持続は注入後150日以上続きました。スライド17は、CAR-Tの生着状況ですが、16名の患者さん全員が、注入後10日から17日でピークを迎え、10~8回の投与レベルで細胞数が10~8個以上に達するなど、強固なCAR-T細胞の生着が認められました。
投与量の増加やCARVacワクチンの追加により、CAR-T細胞の拡大が徐々に改善され、臨床活性と反応につながったことが確認されました。スライド18は、臨床活性の予備的な兆候の概要を示しています。14人の患者が、注入後6週間の時点で、少なくとも1回のスキャンで有効性評価が可能でした。6名の患者さんが部分奏効を示し、さらに5名の患者さんが病勢の安定を示し、標的病変の縮小がみられました(灰色の菱形に緑の輪郭で示すとおり)。
1名の患者さんはベースラインからの変化がなく、2名の患者さんは臨床活性の徴候がなく、いずれも養子セット移植前に急速に進行していた。この結果、全患者の客観的奏効率は43%、病勢コントロール率は86%となりました。12週目には、部分奏効を示した6名の患者さんのうち4名が奏効の深化と持続を示し、1名は注入後18週目に完全奏効に達しました。高用量レベルの精巣がん患者さん4名全員は病勢コントロールが得られ、そのうち3名は客観的奏効を示しました。
また、最も低い投与量のCAR-TとCARVacの併用療法を実施した精巣がん患者様1名が部分奏効を示しました。スライドの一番下のグレーのバーには、さらに1名の精巣がん患者さんが、リンパ節減少療法後に部分奏効を示したことをご紹介したいと思います。この患者さんは、前回お話した14名の評価可能な患者さんには含まれていません。要約すると、最も心強いことに、最初の部分奏効はすべて2回目の評価で深化を示し、1名の部分奏効患者は完全奏効に移行している。
スライド19の左側のウォーターフォールプロットは、精巣がん患者を中心に、4名の精巣がん患者と2名の卵巣がん患者の奏効を示したものです。右側のプロットでは、奏功の期間をよりタイトに描いています。CARVacを使用せず、7段階の投与量のうち低い方の10段階のみを投与した1名の患者さんを除き、他のすべての患者さんに臨床的な有用性が認められました。達成されたすべての奏効は、奏効持続の兆候を示した。
この中には、最初の部分奏効が輸注後18週目に完全奏効に深化した患者さんも含まれています。スライド20は、腫瘍が退縮した2人の精巣がん患者の画像です。両者とも、BNT211を投与する前に、複数の前治療と再発を経験している。患者1は、2008年に診断された61歳の男性である。
彼は以前、6ラインの治療を受けており、CARVacを用いない用量レベル2のCAR-T治療後に反応が短くなった。大きな肺転移は時間の経過とともに完全に消失し、最新のスキャンの時点でも腫瘍はなく、注入後6カ月で血清腫瘍マーカーは[Inaudible]タンパク質が正常値となりました。患者2は、2020年に診断された56歳の男性精巣がん患者で、投与レベル1を受け、さらにCARVacによる治療を受けました。治療により、これらのスキャンでご覧いただけるように、15個以上の転移が大幅に縮小し、強固な反応に結びつきました。
12週目のスキャンの後、患者さんには新たな病変がありました。治療中の生検でCLDN6が陽性であったため、197日目にCAR-T細胞を再投与し、すでに腫瘍マーカーによる反応が確認されました。この安全性と活性のデータには非常に勇気づけられ、現在進行中の第1/2相試験からの新たなデータアップデートは2022年後半に予定されています。それでは、イェンス・ホルスタインが当社の決算について説明します。
イェンス・ホルスタイン — 最高財務責任者
オズレム、ありがとうございます。私のセクションでは、まずスライド22にある2022年第1四半期の主要なハイライトをご紹介します。2022 年第 1 四半期は特別な四半期となりましたが、これは主要な財務ハイライトをご覧いただくとお分かりいただけると思います。2022 年第 1 四半期の売上高は 64 億ユーロとなり、創業以来の記録的な数字となりました。
このトップラインの結果、第1四半期は48億ユーロの営業利益を計上し、完全希薄化後の1株当たり利益は14.24ユーロとなりました。現金に関しては、2022年度第1四半期を62億ユーロの現金および現金同等物と、約127億ユーロの売上債権で終えました。売上債権は主にファイザー社との提携に起因するもので、主に提携に基づく売上総利益の分配を契約上決済したことにより未決済となっています。2022年3月31日時点の売上債権のうち、4月中旬までに52億円を回収し、現金を改善させ、ひいては2022年第1四半期末以降の売上債権のポジションを減少させることができました。
スライド23の続きですが、2022年の第1四半期がいかに好調であったかということを指摘したいと思います。先にも述べましたが、2022年第1四半期に約64億ユーロのCOVID-19ワクチンの売上を計上しました。これは、当時出現したオミクロン・バリアントに続いて、2021年末に最初に発注した数量が増加した結果です。私たちの収益の流れについて、もう少し詳しく説明させてください。
COVID-19ワクチンの共同開発では、販売権に基づいて、当社、ファイザー、佛山製薬の間でテリトリーが配分されています。当社のCOVID-19ワクチンの売上には、提携先のテリトリーにおけるCOVID-19ワクチンの売上総利益の当社持分に関する46億ユーロの売上が含まれています。これらの収入はすでに純額となっており、当社がこれらの収入から100%の粗利益を生み出していることを意味します。当社が過去に言及し、当社の財務諸表およびSECへの提出書類でより詳細に説明しているように、当社の利益配分は、共同研究パートナーであるファイザーと当社との間で共有される予備的データに基づいてある程度推定されます。
2022年第1四半期の当社のCOVID-19ワクチンの売上は、当社のテリトリー内の顧客に対するCOVID-19ワクチンの直接販売による約12億ユーロの売上で、これは当時出現していたオミクロンバリアントに続いて2021年末に当社が行った注文が大きく寄与しています。また、2022年第1四半期のCOVID-19ワクチンの売上高には、当社の提携パートナーへの販売による6億ユーロが含まれています。繰り返しになりますが、当社は今年も非常に好調なスタートを切り、先に発表した2022年度のガイダンスを達成するための強固な基盤ができたと考えています。パンデミックの現状を鑑みると、次の四半期は第1四半期を下回ると予想しています。
それでは、スライド24の2022年第1四半期の業績についてご説明します。前のスライドで売上高についてご説明しましたが、次に売上原価についてご説明します。2022年第1四半期は約13億ユーロとなり、比較対象期間の2021年の2億ユーロに比べました。売上原価の増加は、主に自社テリトリーにおけるCOVID-19ワクチンの売上に関連する費用を計上したことによるもので、これには提携パートナーであるファイザー社に支払うべき売上総利益のシェアが含まれています。また、在庫評価減及び製造委託先との契約から生じる生産能力に関する費用も売上原価の増加に寄与しています。
研究開発費は、2021 年度の比較対象期間の約 2 億ユーロに対し、2022 年度第 1 四半期は約 3 億ユーロでした。この増加は主に、発売前のオミクロン・ワクチン製品の製造に関連する費用を発生期の研究開発費として計上したことと、従業員数が増加したことによるものです。これは、COVID-19ワクチンプログラムに関連する研究開発費が前年同期に比べ減少したことによ り一部相殺されています。一般管理費は、2021年の比較対象期間の3890万ユーロに対し、2022年第1四半期は9080万ユーロに達しました。
一般管理費の増加は、主に購買管理、コンサルティング、法務サービスにかかる費用の増加、および人員の増加によるものです。法人税等は、2021 年度の比較対象期間の 5 億ユーロの税金費用に対し、2022 年度第 1 四半期は 13 億ユーロの税金費用となりました。2022 年第 1 四半期の実効税率は 26.3%で、通期では 28%程度になる見込みです。2022年第1四半期の純利益は、2021年の比較対象期間の11億ユーロに対し、37億ユーロに達しました。
2021年度第1四半期の希薄化後1株当たり利益は、前年同期が4.39ユーロであったのに対し、14.24ユーロとなりました。2022年会計年度の見通しを再表示しているスライド24に移りますと、2022年第1四半期は非常に好調なスタートを切り、ここ数ヶ月のパンデミックの経過や政治的不確実性に由来する不確実性は認めざるを得ないものの、通期のガイダンスを再表示しています。2022会計年度中に納入される約24億回分のオーダーブックに変更がないことを考慮し、2022年通年のCOVID-19ワクチンの推定売上高を約130億~170億ユーロと確認します。また、2022年の費用および設備投資計画、ならびに年間実効税率についても、スライドにまとめましたので、改めてお知らせします。
最後に、最高戦略責任者のライアン・リチャードソンから、2022年の見通しについてご説明します。ありがとうございました。
ライアン・リチャードソン — 最高戦略責任者
Jens、ありがとうございます。スライド27、今年度中の優先事項の説明に移ります。私たちは引き続き、COVID-19ワクチンの供給と、次世代ワクチンのパイプラインの開発に注力しています。今年初めには、ドイツ政府との複数年のパンデミック対策契約を発表し、他の政府との協議も進めています。
がん領域では、固形がんを対象としたCAR-T細胞プログラムである進行中の第1/2相試験BNT211のデータ更新に加え、無作為化第2相試験からの最初の読み出しが期待されます。当社は、今後1年間にパイプライン全体で複数の登録試験を開始する準備を続けており、これらの計画については、年内にさらなる最新情報を提供します。感染症分野では、拡大する前臨床ポートフォリオを構築することに加え、2022年にはさらに4つのmRNAワクチンプログラムのファーストインヒト臨床試験を開始する予定です。さらに、自己免疫疾患、再生医療、循環器疾患などの新たな治療領域へのプラットフォームの拡大を加速しており、いくつかのプログラムではリード候補の選定を行う予定です。
これらの目標に対する重点的な実行を支えるため、当社は基盤整備、特にデジタルおよびAI能力の強化、そして今後数年間に想定されるさらなるパイプラインの拡大を支えるためのグローバル開発チームへの投資を行っています。スライド28では、当社のCOVID-19ワクチンの年間受注量は約24億回分で、第1四半期末までに約7億5千万回分の請求がなされています。BNT162b2については、生後6カ月から5歳までの小児における3回投与レジメンのデータを含め、年内には複数のデータ更新が行われる見込みです。当社は、包括的な変種適応ワクチンプログラムの一環として、16歳以上の成人における4回目の投与を評価しています。
さらに、今後数週間のうちに、オミクロン採用ワクチンと二価ワクチンの安全性と免疫原性のデータを開示する予定であり、これは現在進行中の規制当局との議論に役立つものです。スライド29は、2022年に予定されているパイプラインのマイルストーンです。今年は、帯状疱疹、結核、HSV-2、マラリアに対するmRNAワクチンを含む、7つのファースト・イン・ヒューマン試験を開始する予定です。1月には、このエキサイティングな新しいプラットフォームからの最初のプログラムであるBNT141 RiboMabプログラムの最初の患者を投与しました。
CD3 CLDN18.2二重特異性抗体をコードする2番目のRiboMabであるBNT142は、今後数カ月のうちに臨床に投入されるものと予想しています。非小細胞肺がんに対する当社のFixVacプログラムであるBNT116も、リジェネロンとの提携拡大の一環としてLibtayoとの併用で評価され、今年の後半には臨床に入る見込みです。さらに3つのプログラム、BNT161とファイザーと提携したインフルエンザmRNAワクチンから今年中にデータ更新があり、2022年後半には、メラノーマのフロントライン治療としてペムブロリズマブとの併用で評価している当社のINeSTプログラム、BNT122からデータ更新があると予想しています。最後に、オズレムが強調したBNT211 CAR-T細胞プログラムについては、今年中にさらなるデータ更新を期待しています。
スライド30を終える前に、6月1日に年次総会を開催することを投資家の皆様にお伝えしたいと思います。また、6月29日(水)には、初のバーチャル・キャピタル・マーケット・デーを開催する予定です。株主の皆さまの日頃のご支援に感謝申し上げ、質問をお受けします。
質疑応答
オペレーター
[最初の質問はモルガンスタンレーのマシュー・ハリソンさんからです。どうぞよろしくお願いします。お待たせしました。マシュー・ハリソン — モルガンスタンレー — アナリスト
素晴らしい こんにちは。質問を受けてくださってありがとうございます。ブースターの規制に関してどのような議論が必要なのか、また、特に米国での規制経路はどうなっているのか、現在の考えをもう少し詳しく教えてください。
単純なブリッジング試験で済むとお考えなのでしょうか、それとももっと複雑なものになるのでしょうか。ありがとうございました。
Uğur Şahin — CEO(最高経営責任者
そうですね。では、私が質問をお受けし、Ozlemが補足することができると思います。変異型適応症ワクチンの承認に向けた規制当局の道筋は、まだ明確に定義されていません。私たちは、FDAやEMAなどの規制当局と何度も会合を持ちました。
そして、二価ワクチンだけでなく、一価ワクチンのデータも見て、そのデータに基づいて判断したいと提案されました。ご存知のように、FDAは6月末にVRBPAC会議を予定しており、そこで来シーズンに望ましいワクチンについて、より明確なガイダンスを提供することを示しました。EMAも同様の声明を発表しています。そして、両当局とも、8月、9月、10月という時間枠の中で、ワクチンの認可を受けることを希望しているようです。
そうです。ですから、このプロセスは進行中です。一価ワクチンと二価ワクチンについて、低用量と高用量を含むデータを作成中です。そして、そのデータを同僚と議論するために利用できるようにするつもりです。
これで質問にお答えできると思います。次の質問は?
オペレーター
ありがとうございます。次の質問はJPモルガンのコーリー・カシモフからお願いします。どうぞ
お待たせしました。
コーリー・カシモフ — J.P.モルガン — アナリスト
おはようございます。おはようございます。この一般的な考え方のフォローアップをしたいのですが、今後数週間のうちにさまざまなCOVIDプログラムからのデータが予想されますし、先ほどお話になった規制当局の動向も不確かです。オミクロン・スペシフィック・ブースターと二価医薬品の相対的な価値提案について、短期的および長期的な観点からどのようにお考えか、お聞かせください。
ありがとうございました。
ウール・シャヒン(Uğur Şahin) — 最高経営責任者
ありがとうございます。すでに分かっていることは、オミクロン1回目の感染後の抗体価について、発表されたデータを参照したことです。このデータは、ワクチンを接種していない人たち、2回または3回接種した人たちのデータを作成し、それを評価したものです。しかし、これはオミクロンに暴露された後に起こっていることです。
BA.1オミクロンを接種すると、オミクロン変異体に対する抗体価が上昇するだけでなく、デルタ、アルファ、オリジナルウイルス変異体を含む他のすべての変異体に対する抗体も上昇し、両方の抗体反応を高めることがわかりました。これは、他のグループでも同じような効果があることを発表しています。重要なのは、オミクロンの感染にさらされることで、これはワクチン接種を受けた人にも起こることだと思いますが、主に記憶反応、つまり事前に確立された記憶反応を高めるということです。現時点では、オミクロン・ワクチンと他のワクチンを併用することに合理的な利点は見出せません。
しかし、一日の終わりには、少なくとも異なる個体でデータを作成することが重要です。そして、これまでのオミクロンの変異体だけでなく、新たに出現したBA.4やBA.5の変異体、さらに以前のSARS-CoV-2の変異体に対する抗体認可の力価を比較し、それらが将来的に影響を与えるかどうかにかかわらず、比較する予定です。
Cory Kasimov — J.P.モルガン — アナリスト
わかりました。ありがとうございました。
オペレーター
ありがとうございました。次の質問はゴールドマン・サックスのクリストファー・ゾップからです。どうぞ お待たせしました。
Christopher Zopf — Goldman Sachs — アナリスト
おはようございます。質問にお答えいただき、ありがとうございます。四半期決算おめでとうございます。同じトピックについて、先ほど行われたASIPの会話に基づいて、この決定のための枠組みを作り始めましたが、この決定を下すために彼らが求めているデータについて教えていただけますか?異なる変異体に対する中和力について少しお話されましたが、そんなに単純なことですか?
それは単純なことですか?それとも、安全性とは別に、他の側面も見るのでしょうか?また、オミクロン特異的なワクチンのデータが手に入ったら、中国のような他の規制の議論に影響を与える可能性があると予想されますか?ありがとうございました。
ウール・シャヒン(Uğur Şahin)–最高経営責任者
はい、もちろん安全性は評価されています。評価されます。そして、安全性の評価は、ブースターワクチンを接種する数百人の被験者に対して行われます。ですから、規制当局からのフィードバックも踏まえ、大きな価格が必要になるとは考えていません。
すでに述べたように、私たちは当局と何度も話し合いを持ちました。しかし、一価と二価のどちらが好ましいかについては言及されませんでした。これは6月末のVRBPACでの議論になるかと思います。そして、私は……、私たちがすでに生み出しているものに加えて、予想外のデータセットを要求されても驚かないだろうと思います。
運営担当者
ありがとうございました。次の質問に行きます。次のご質問は、ジェフリーズのアカシ・テワリさんからです。どうぞよろしくお願いします。
お待たせしました。
Akash Tewari — Jefferies — アナリスト
どうもありがとうございます。オミクロン・ブースターについて、貴社とModernaは異なるアプローチで話しているようですね。モデナは二価を、貴社とファイザーはナイーブでない患者のための修正スパイクを話しているようです。
特に28日目の抗体価について、モデナは野生型ブースターとオミクロン・ブースターの間に大きな違いはないと言っていますが、御社は少なくともαブースターで28日目に高い抗体価を示しています。また、今後の規制当局の動向は不透明であり、市場参入のためには確実なBEデータが必要ですが、2022年にオムロンブースターを発売しないシナリオもあり得るのでしょうか?ありがとうございます。
ウール・シャヒン(Uğur Şahin):最高経営責任者
それでは、今、さまざまな会社が沈んでいることに関係なく、私たちが置かれている全体的な状況を表現させてください。現在、オミクロンのパンデミックが進行中で、全感染症の99.8%または99.9%がオミクロンの亜種に媒介されている状況です。現在、複数のオミクロンの亜種が存在し、それぞれ異なるエスケーププロファイルを持っています。ヨーロッパでは、オミクロン2.9や2.12.1のような亜型が見られます。
また、アフリカや東洋では、BA.4やBA.5の亜型が見られ、これらは中和価の損失がさらに大きいようです。季節性ワクチンの決定は、現在流行している実際の亜種に沿ったものでなければなりません。そして、我々やModernaをはじめとする企業は、一価および二価のワクチンを含むオミクロン適応型ワクチンの評価を開始しました。つまり、すべての企業がこのデータを作成することになります。
そして、中和価を評価するために作成されたこのデータを、実際のばらつきと照らし合わせなければなりません。そして、それに基づいて、結論を出さなければなりません。それが今後の課題です。今後数週間で何が起こるか、新しい亜種が出現するかどうかは分かりませんが、当局が下す決定には、現在流通している亜種に関して進行中のものが反映されていなければならないことは確かでしょう。
司会
次の質問は、SVBのダイナ・グレイボッシュからです。
Daina Graybosch — SVB Leerink Partners — アナリスト
ご質問ありがとうございます。この件に関してもう1つお聞きしたいのですが、たぶん少し違う方向だと思います。オミクロン感染後の保存されたエピトープに対するメモリーB細胞応答を示す論文を発表されたとのことですが、同様の論文があったと思います。
たしか、ロックフェラーの科学者たちからも同じような論文が発表されていたと思います。しかし、この研究は感染後40〜50日というかなり早い時期に行われました。このような幅広いB細胞や中和抗体の耐久性は、以前のワクチン接種で得られた、より長い耐久性を持つ変異型スパイクに対する中和抗体と同程度になると、なぜ確信できるのでしょうか。
ウール・シャヒン(Uğur Şahin) — 最高経営責任者
ダイナ、私の意見では、抗体の耐久性は、主に最初の抗体価によって左右されます。つまり、血漿を含む体液区画や新しい表面で起きていることです。次に、メモリーB細胞の成熟過程である第二の反応が進行しています。感染直後は、私たちの論文で示したように、メモリーB細胞による反応が起こりますが、この反応には新しいナイーブなメモリーB細胞も加わってきます。
しかし、このナイーブメモリーB細胞は、突然変異が少なく、抗体の親和性も低くなります。このため、成熟が確立するまでに数週間から3ヶ月を要します。そして、新規エピトープに対する高親和性抗体を生成するために、2回目のブースターが必要になるかもしれません。これが免疫学が教えてくれたことであり、私たちが期待することでもあります。
つまり、抗体価は低下していきます。しかし、その一方で、オミクロン変異体から来る新しいエピトープにより適応した、新しいメモリーB細胞が生成されるでしょう。
Daina Graybosch — SVB Leerink Partners — アナリスト
それは参考になりますね。ありがとうございます。
オペレーター
ありがとうございました。次の質問はベレンバーグのシュウ・ジチアンからです。どうぞ 回線は開いています。
Shu Zhiqiang — Berenberg Capital Markets — アナリスト
素晴らしい。ありがとうございます。好調な四半期におめでとうございます。資本配分についてお聞きしたいのですが。
第1四半期時点でバランスシートに190億ユーロの資金がありますね。そのキャッシュをどのように使っていこうと考えているのか、特にこのバイオテクノロジー評価の低迷を背景に、BDやM&Aの機会についてお聞かせください。CLDN18.2 mRNAプログラムについて簡単に説明します。このターゲットに関するあなたのこれまでの経歴から、このアプローチは抗体アプローチとどのように異なっていると思われますか?ありがとうございました。
イェンス・ホルスタイン — 最高財務責任者
そうですね。ご質問をありがとうございました。まず私から、そしてウガーにバトンタッチします。ガイダンスは、ご覧のとおり、130億から170億という数字で再提示しました。
第1四半期を終えて、私たちはこの数字に非常に満足しています。つまり、64億円の売上高と収益性が、このガイダンスを裏付けるものだと考えています。年末の電話会議で述べたように、当社の投資の主な目的は、引き続き研究開発活動への投資であり、今後 も継続します。しかし、ご記憶のように、つい最近開始した自社株買いプログラムに15億ユーロを投資し、過去に長期に亘って在籍した株主にも還元することを発表しました。
また、株主の皆様には今年中に5億ユーロの配当金をお支払いしています。今後、M&Aなどに関しても、もちろん、取引や協業など、あらゆる種類の追加を検討し、過去と同様に進めていくつもりです。しかし、いつ、どこに、どれだけの投資を行うかについて、詳しいガイダンスをお伝えすることはできません。事態の推移を見極めなければなりません。
しかし、キャッシュポジションについては良好な感触を得ています。先ほど、キャッシュポジションが増加したことをお聞きになったかと思います。4月中旬にさらに52億ユーロを回収しました。ですから、現時点では100億円前後、あるいは100億円を超える水準にあると言えます。
ですから、キャッシュポジションは良好であり、今後数年間は資金を投資することができます。ウガー?Ugur、2つ目の質問を引き継ぎますか?
オズレム・トゥレシ — チーフ・メディカル・オフィサー
2つ目の質問、CLDN18.2リボマブの開発についてですが、私が引き継ぐことができます。すでにご指摘のように、私たちはCLDN18.2指向性抗体の臨床活性の経験があり、mRNAを使用して全身をコード化し、抗体を組換えタンパク質として製造する必要性を回避することは、多くの機会をもたらします。このような機会を利用して、リボマブを単剤で使用するだけでなく、他の治療法との併用も可能にしたいと考えています。
Shu Zhiqiang — Berenberg Capital Markets — アナリスト
素晴らしい。ありがとうございました。
オペレーター
ありがとうございます。もう1つ質問をお受けします。最後の質問はUBSのエリー・メルルさんからです。どうぞよろしくお願いします。
どうぞ。
発言者不明
エリーさんに代わってサラです。質問をお受けいただき、ありがとうございます。BNT211について、また、後期開発段階への移行についてですが、何を求めておられますか?また、自信を持って前進するために、どのようなことを期待されていますか?また、より大きなスケールで、他の治療法の選択肢の中で、どのような位置づけにあるとお考えでしょうか、また、どのような治療法なのでしょうか。ありがとうございました。
Ozlem Tureci — チーフ・メディカル・オフィサー
CLDN6に対する当社のCAR-T細胞療法であるBNT211については、まだ用量漸増の段階にあります。しかし、特に精巣がんや卵巣がんでは、すでに有望な臨床活性が確認されています。ですから、私たちがやりたいことは、データを集め続け、その集計結果に基づいて、今後どうするかを決めることです。CAR-T細胞療法は、その後の治療ラインに位置づけたいものです。
私たちがCLDN6 CAR-T細胞を評価している適応症、すなわち進行転移性精巣がん、卵巣がん、子宮内膜がん、肉腫などの希少がんには、かなりの医療ニーズがあると思います。そして、具体的にどのように位置づけるかは、この最初の試験の用量漸増と用量拡大の部分で得られるデータの集計によります。
オペレーター
ありがとうございました。では、最後にSylkeからご挨拶をお願いします。
Sylke Maas — インベスター・リレーションズ担当副社長
本日はありがとうございました。今後ともよろしくお願いいたします。ありがとうございました。
以上です。他の翻訳希望があればご連絡いただければ検討いたします。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>


