イーライリリー・アンド・カンパニー (LLY)2022年第2四半期決算説明会の日本語訳です。
ドル高の影響もありますが決算ミスで株価は下落してますね。有望な糖尿病薬の開発パイプラインもあるので将来的には期待していますが今は厳しそうですね。
ガイダンスでもEPSは良くないので低迷しそうです。ただ、中々株価は下がらない銘柄なのである意味買場が来るかもしれないですね。
CNBCの投資情報番組『Mad Money』でジム・クレイマーも注目しているので注目している人は多そうです。
決算が良ければ買って行くつもりでしたがしばらくは様子見ですね。
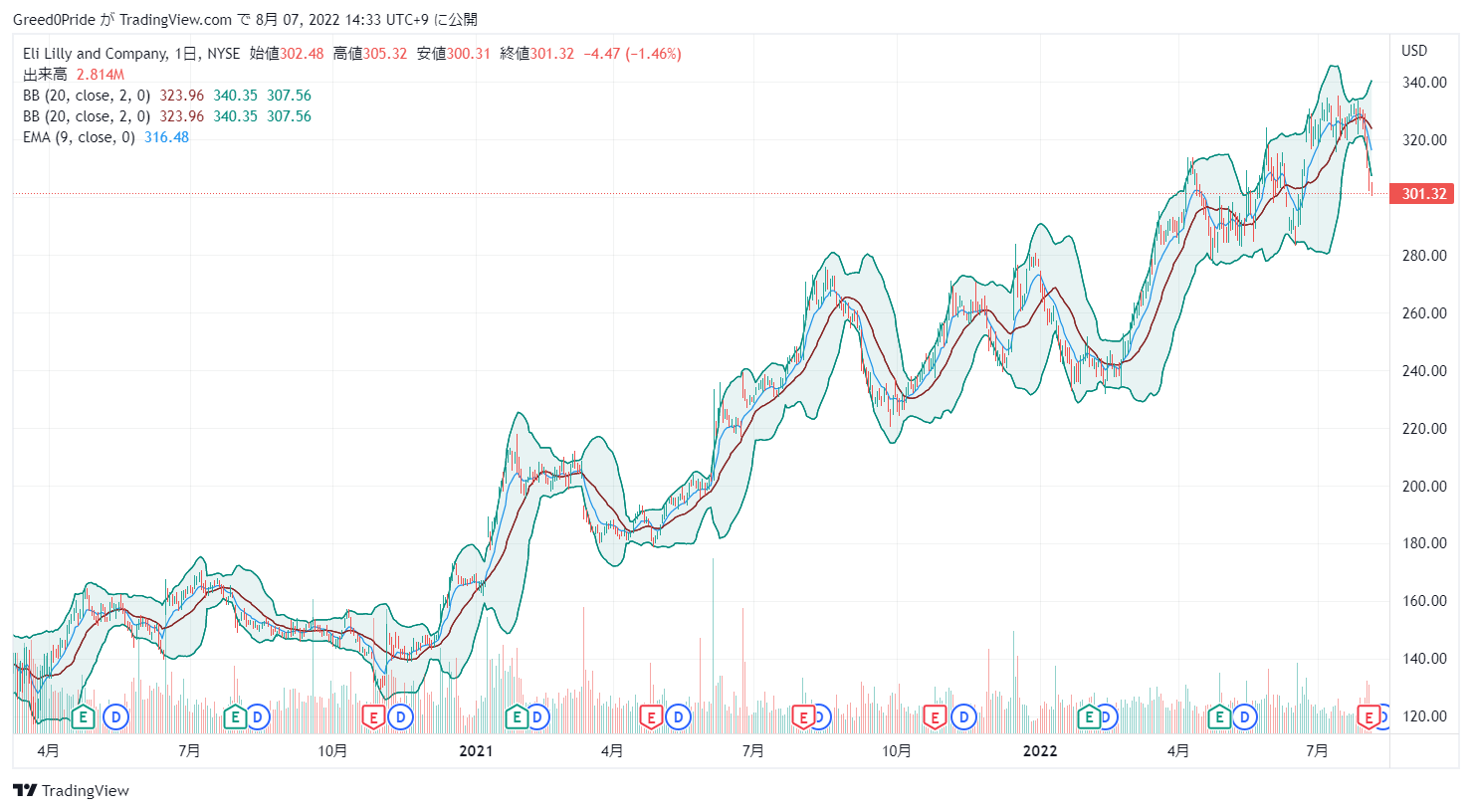
イーライリリー・アンド・カンパニー (LLY)株価
イーライリリー・アンド・カンパニー (LLY)2022年第2四半期決算説明会
Call participants:
Kevin Hern — Vice President, Investor Relations
Dave Ricks — Chairman and Chief Executive Officer
Anat Ashkenazi — Chief Financial Officer
Dan Skovronsky — Chief Scientific and Medical Officer
Geoff Meacham — Bank of America Merrill Lynch — Analyst
Mike Mason — President, Lilly Diabetes
Chris Schott — J.P. Morgan — Analyst
Seamus Fernandez — Guggenheim Partners — Analyst
Louise Chen — Cantor Fitzgerald — Analyst
Anne White — President of Lilly Neuroscience
Terence Flynn — Morgan Stanley — Analyst
Tim Anderson — Wolfe Research — Analyst
Steve Scala — Cowen and Company — Analyst
Ilya Yuffa — President of Lilly International
Andrew Baum — Citi — Analyst
Jake Van Naarden — Chief Executive Officer of Loxo at Lilly
David Risinger — SVB Leerink Partners — Analyst
Chris Shibutani — Goldman Sachs — Analyst
Carter Gould — Barclays — Analyst
Kerry Holford — Berenberg — Analyst
Mohit Bansal — Wells Fargo Securities — Analyst
Evan Seigerman — BMO Capital Markets — Analyst
Colin Bristow — UBS — Analyst
More LLY analysis
2022年08月04日 午前10時00分
オペレーター
リリー2022年第2四半期決算コンファレンスコールへようこそ。[この会議は録音されています。それでは、司会のケビン・ハーン(投資家向け広報担当副社長)に会議を引き継ぎたいと思います。どうぞよろしくお願いします。
ケビン・ヘルン — インベスター・リレーションズ担当バイス・プレジデント
ありがとうございます。イーライリリー・アンド・カンパニーの2022年第2四半期決算説明会にお集まりいただき、ありがとうございます。1時間の遅れをお詫びします。AT&T側で技術的な問題が発生しました。
それでは、お待たせいたしました。私は投資家向け広報担当副社長のケビン・ハーンです。本日の電話会議には、リリーの会長兼CEOのデイブ・リックス、最高財務責任者のアナト・アシュケナージ、最高科学・医学責任者のダン・スコブロンスキー博士、リリー・ニューロサイエンスの社長アン・ホワイト、リリー国際の社長イリヤ・ユファ、リリー社ロキソのCEOジェイク・バンナールデン、リリー糖尿病の社長マイク・メイソン、リリー免疫学とリリーUの社長パトリック・ヨンソン、が参加します。 また、IRチームのMike Springnether、Ken Zuluega、Lauren Zerki、そして今月からIRチームのリーダーを引き継ぐJoe Fletcherも参加しています。この電話会議では、現時点での予測にもとづく見通しを発表する予定です。実際の業績は、スライド3に記載されているものを含む、いくつかの重要な要素により、大きく異なる結果となる可能性があります。実際の業績と大きく異なる結果を生じうる要素は、当社が米国証券取引委員会 に提出した最新のフォーム 10-K およびその後のフォーム 10-Q、8-K に記載されています。
当社が提供する製品およびパイプラインに関する情報は、投資家の皆様の便宜を図るためのものです。また、この情報はプロモーションを目的としたものではなく、処方を決定するのに十分なものではありません。準備した発言に移行するにあたり、私たちのコメントは非GAAPベースの財務指標に焦点を当てることにご留意ください。それでは、Daveに電話をつなぎます。
デイブ・リックス — 会長兼最高経営責任者
ケビン、どうもありがとうございます。第2四半期には、米国でのMounjaroの承認と発売、donanemabとpirtobrutinibのFDAへの申請と受理、lebrikizumabの良好なトップライン結果、mikizumabのEUと日本での申請など、影響力のある多くのパイプラインのマイルストーンを達成しました。このようなパイプラインの進展は、当社のエキサイティングな長期的見通しの幅と深さを強調するものです。第2四半期におけるリリーのヘッドラインストーリーは、米国で発売されたMounjaroで、初期導入が好調に推移しています。
この新薬は、2型糖尿病の患者さんにA1c値と体重減少の効果をもたらす可能性があり、現場から大きな熱意が伝わってきており、私たちも期待しています。当社は引き続き、Mounjaroの幅広いオープンアクセスの獲得に注力しており、オープンアクセスが実現するにつれて、患者さんと当社事業に対するこの医薬品のインパクトが十分に発揮されることを期待しています」と述べています。第2四半期の業績と戦略的課題の進捗に目を向けると、トップラインの業績は恒常為替レートベースで比較的横ばいとなりました。これは、Verzenio、Jardiance、Trulicityといった主力製品の数量主導の力強い成長が、価格低下、世界の主要市場におけるAlimtaの特許切れ、昨年の中国におけるCialis権利の売却によって相殺されたからです。
当四半期の販売台数は、10%増と堅調に推移しました。アリムタ、中国でのシアリスの権利売却、COVID-19抗体からの収益を除くと、収益は2021年第2四半期比6%増となりました。第2四半期は、新薬が数量成長に18%寄与し、現在ではコア事業の収益の67%を占めており、堅牢なパイプラインとともに、当社の成長見通しの強さと耐久性を示す最も重要な指標であると考えています。当四半期の非 GAAP 型売上総利益率は 79.8%となり、前年同期から約 50bp 上昇しました。
非 GAAP 型営業利益率は、インプロセス研究開発費及び開発マイルストーン費用による約 680bp のマイナスの影 響を除くと、20.5%となりました。12 月に開催した投資家向け説明会では、今後 2 年間に上市される可能性のある 5 つの新薬について説明し、10 年間を通じてトップクラスの成長を促進する触媒となる可能性があると述べました。第1四半期決算発表以降、2型糖尿病治療薬「モンジャロ」の米国での承認・上市、欧州のCHMPにおける肯定的な評価など、5品目すべてにおいて重要なパイプラインの進展がありました。
早期症状のアルツハイマー病におけるdonanemabのFDA承認と優先審査指定。BTK阻害剤による治療歴のあるマントル細胞リンパ腫の患者に対するピルトプルチニブのFDA承認と優先審査指定。– また、lebrikizumab の中等度から重度のアトピー性皮膚炎における 52 週間の良好なデータが発表されました。また、円形脱毛症に対するオルミエントの米国、欧州、日本での承認も発表しています。
先月、当社は、既存製品の需要増とパイプラインにある新薬の需要増を支えるため、ここインディアナ州にある2つの新製造拠点に21億ドルを投資する計画を発表しました。今回の発表は、リリーが最近行ったマサチューセッツ州、ノースカロライナ州、アイルランドでの新施設への投資に続くもので、リリーの有効成分や遺伝子医薬などの新しい治療法のための製造ネットワークをさらに拡大するものです。これらの投資は、当社におけるポートフォリオの成長に対する当社の自信を強調するものです。最後に、第2四半期に9億ドル近い配当金を株主に分配しました。
スライド5では、第1四半期決算発表以降の主なイベントのリストをご覧いただけますが、これにはいくつかの重要な規制当局による臨床およびCOVID-19抗体のアップデートが含まれています。第2四半期に既に発表したように、当社は、患者さんにCOVID-19治療の選択肢を提供するための継続的な取り組みとして、米国政府と15万回分のベブテロビマブを約2億7500万ドルで供給する契約を締結しています。第2四半期に約1億3,000万ドル相当のベブテロビマブを出荷し、残りの注文分は第3四半期に出荷する予定です。
本日、米国政府との協力により、州、病院、その他の特定のプロバイダーが総販売代理店契約を通じてbebtelovimabを購入できるようにする予定であることを発表します。これは、米国政府が現在保有している供給量が枯渇することが予想される今月末に実施する予定です。
連邦政府による大規模な購入から、より多くの購入者へのCOVID-19抗体の販売・配布に移行するため、今後は売上高の見込みをフォワードガイダンスに組み込んでいく予定です。以前から申し上げているように、COVID-19抗体は当社の長期的な成長の大きな原動力にはならないと考えています。しかし、オミクロン変異体を中和する最後のモノクローナル抗体治療薬として、COVID-19のパンデミックに立ち向かうために、私たちはできる限りの貢献を続けていきます。それでは、第2四半期の業績について、より詳細なレビューを行うため、アナトに電話をつなぎます。
Anat Ashkenazi — 最高財務責任者(CFO
ありがとう、Dave。スライド6の要約は以下の通りです。
[オペレーターからの指示]デイブ・リックス — 会長兼最高経営責任者
その続きで、時間を見ましょう。
アナト・アシュケナージ — 最高財務責任者
スライド6は、2022年第2四半期の財務実績をまとめたものです。非GAAPベースの業績に絞ってコメントさせていただきます。前年同期比の財務比較に影響を与える注目すべき項目がいくつかありました。為替レートは今期の収益におよそ300ベーシスポイントの影響を与え、第2四半期の収益は4%、恒常為替レートベースでは1%減少しました。
2021年第2四半期には、中国におけるシアリスの権利を売却したため、1億7,000万ドルの一時的な収益影響がありました。また、今期は欧州と日本におけるアリムタの独占権喪失の影響をフルに受け、米国では複数の後発品参入の影響を受け始めています。
オペレーター
[オペレーターからの指示]Anat Ashkenazi — 最高財務責任者
お電話に出られた皆さん、どうぞよろしくお願いします。
オペレーター
[オペレーターからの指示]アナト・アシュケナージ — 最高財務責任者
続けます。皆さんに聞いていただけるといいのですが。
オペレーター
[オペレーターからの指示]アナト・アシュケナージ — 最高財務責任者
アリムタからの収益を除くと、昨年は中国でのシアリスの権利販売 [聞き取れず] がありました。
オペレーター
[オペレーターからの指示]アナト・アシュケナージ — 最高財務責任者
OKです。うまくいけば、私が最後の意図を繰り返すのを聞いていただけたと思います。アリムタからの収益、昨年第2四半期の中国におけるシアリスの売上、およびコビド抗体の売上を除くと、総収益は6%増加し、第2四半期における当社のコアビジネスの堅調なモメンタムを浮き彫りにしていますね。この成長率は下半期に加速されると考えています。
売上高に対する売上総利益率に話を移すと、2022年第2四半期は50ベーシスポイント増加し、79.8%となりました。この売上総利益率の増加は、主に製品ミックスと海外販売在庫に対する為替の有利な影響によるもので、実現価格の低下により一部相殺されました。インフレによる物流費及び製造費の増加は、当四半期の売上総利益率に小幅なマイナスの影響を及ぼしました。当四半期の営業費用合計は14%増加しました。これは、第1四半期の決算説明会で述べたとおり、SECのガイダンスに従 い、買収した仕掛研究開発費および開発マイルストーン費用を含んでいるためです。
買収した知的財産の研究開発費および開発マイルストーン費用は、第2四半期の経費増加の約1,200ベーシスポイントを占めています。マーケティング費用、販売費及び一般管理費は、主に為替のプラスの影響により、4%減少しました。研究開発費は8%増加しましたが、これは後期開発資産の開発費の増加によるもので、COVID-19抗体の開発費の減少により一部相殺されました。今期は、買収した知的財産の研究開発および開発マイルストーン費用として4億4000万ドル(EPSの0.46ドル)を計上しました。これは主に、変異型選択的PI3Kα阻害剤の開発、規制、商業的成功を条件とする、将来の義務の実質的すべての買い手に関連する費用に関するものです。
2021年第2四半期、買収したIPの研究開発費および開発マイルストーン費用は4300万ドル、EPSの0.04ドルでした。第2四半期の営業利益は、主に買収したIPの研究開発および開発マイルストーン費用の増加により、32%減少しました。売上高営業利益率は、これらの費用による約680ベーシスポイントのマイナスの影響を含めて、20.5%でした。その他の収益および費用は、前年同期の500万ドルの収益に対し、当四半期は約1,300万ドルの費用となりました。
第2四半期の実効税率は14.2%で、前年同期に比べ10ベーシスポイント低下しました。この減少は、研究開発費の資産計上に関する2017年税法の規定の実施に関連する有利な税効果により、控除対象外の開発マイルストーンの税効果で相殺されたことによるものです。ボトムラインでは、1株当たり利益は今期32%減の1.25ドルとなりました。前年同期比減少の最も大きな要因は、買収したIPの研究開発費および開発マイルストーン費用の影響で、前年同期が0.04ドルだったのに対し、今年第2四半期は0.46ドルのマイナス影響となりました。
スライド 8 では、価格、料率、数量と売上高の伸びの影響を定量的に示しています。今期、米国の売上は6%増となりました。5月の広範な後発品参入により大幅に減少したアリムタとCOVID-19抗体からの収益を除くと、米国での収益は11%増加しました。
この数量主導の成長は、Trulicity、Verzenio、Jardianceに牽引されたものです。第2四半期は8%の純価格下落を経験しましたが、これはHumalog、Alimta、Forteoの実現価格が、リベートセグメントの増加、事業の若干の拡大、契約率の上昇、今年の注射用インスリン生薬のリスト価格の引き下げにより低下したことによります。Taltzの実現価格の低下も、リベートや割引の見積もりを変更した影響によるもので、主に基準期間の有利な調整と、それほどではありませんが、既存のアクセスの継続的なプルスルーが要因となっています。2022 年上半期の米国における純価格下落率は 4%でした。
は4%であり、通期では引き続き一桁台半ばの純価格下落を見込んでいます。欧州に移ります。第2四半期の売上は、恒常通貨ベースで1%増加しました。2021年6月に独占権を失ったアリムタの収益を除くと、主にトゥリシティ、ジャルディアンス、Taltz、Verzenioの数量増に牽引されて、収益は恒常通貨ベースで12%増加しました。
日本では、2021年6月にジェネリック医薬品の参入が予定されているシンバルタとアリムタを中心に、特許切れ製品の大幅な減少の影響を受け、第2四半期の売上高は恒常通貨ベースで22%減少しました。日本では、主要な成長製品が売上高全体の69%を占め、第2四半期は為替変動の影響を受けずに11%成長しました。当社は引き続き、2023年以降に日本での成長が回復すると見込んでいます。中国では、NRDLフォーミュラリーアクセスの影響により実現価格が低下しましたが、Verzenio、Tyvyt、Trulicity、Taltzなど特定の新製品の数量増加により一部相殺され、売上高は恒常通貨ベースで32%減少しました。
また、Humalogについては、数量ベースの調達の影響により価格が低下しました。アクセスの改善により、価格下落を補って余りある数量増が期待されます。中国でCOVID-19が発生し、その後ウイルスの拡散を抑制するための保護措置がとられたため、第2四半期は特に輸液製品で予想以上に数量が減少しました。また、タイビットについては、競争激化の影響を受けています。
その他の地域の売上は、主に主要な成長製品の売上増加により、恒常通貨ベースで3%増加しました。通期では、米国、EU、日本でそれぞれ一桁台半ば、中国で二桁台の正味価格下落を引き続き見込んでおり、結果として全世界で一桁台後半の価格下落になると思われます。スライド9に記載のとおり、主要な成長製品が引き続き全世界で力強い数量成長を牽引しています。これらの製品は、当四半期において18%の数量増加を達成し、引き続き当社の全体的な業績と見通しを下支えしています。
スライド10は、当社の主要な成長製品の貢献度を示しています。今期、これらのブランドは20%、恒常為替レートベースでは約24%成長し、43億ドルの売上高を計上、当社の中核事業の売上高の67%を占めました。これらの製品については、引き続きさらなる成長の機会があると考えています。例えば、Verzenioがアジュバントという適応症に牽引され、最近の新薬の市場シェアの加速を含め、力強い軌道に乗っていることは非常に喜ばしいことです。
インクレチン注射剤については、現在、米国のブランド糖尿病市場における処方比率は25%に過ぎず、2型糖尿病治療における血糖コントロールと体重減少のための早期使用により市場拡大が見込まれることから、さらなるクラスアップの大きなチャンスと捉えています。Trulicityは、多くの国際市場において、市場の成長および一部の市場における競合品のGLPの利用が制限されていることから、需要が加速しています。私たちはこの需要増に対応する一方で、成長を管理し、患者さんへの影響を最小限に抑えるための行動を一部の国で実施しています。
このTrulicityの見通しは、当社のガイダンスに含まれています。リリーは、GLP-1の中で最も治療期間が長いTrulicityと、2型糖尿病やその他の代謝性疾患の治療において、このクラスの薬剤の選択肢として革新的なステップを提供できるMounjaroの両方を手に入れることができて、とても嬉しく思っています。2型糖尿病に対するMounjaroのFDA承認に伴う興奮と大きな関心を踏まえて、早期上市に向けた最新情報を簡単にご説明したいと思います。米国での承認後
5月中旬に米国で承認された後、6月中旬に本格的な発売を開始しました。当社のコマーシャルチームは、2型糖尿病患者を対象としたMounjaroの上市に向けて、患者中心のアプローチを展開するため、準備を整え、活力を与え、各チャネルで高いレベルのエンゲージメントを観察しています。本日発表したMounjaroの業績は、患者さんが好調なスタートを切れるよう、サンプル受付や自己負担金支援プログラムを大幅に活用したことを反映しています。同業者間の交渉は予想通り進んでおり、Mounjaroのアクセス確立に向けて規律あるアプローチをとり、Trulicityで達成したのと同じ幅広いオープンアクセスを提供することに注力しています。
また、Mounjaroの処方動向(最新のIQVIAデータでは、2型糖尿病治療薬インクレチンの新規ブランドでの市場シェアが20%を超えています)にも注目しています。また、Mounjaroの発売以来、2型糖尿病注射剤インクレチンクラスのリリー新薬のシェアが約12ポイント伸びていることも喜ばしいことです。Mounjaroへのアクセスを確立するために、Co-payカードが多く利用されていることから、今後数四半期は、売上高よりも処方動向の方が、発売後の浸透度をより正確に測ることができると思われます。Mounjaroの初期導入量は、当社が想定するシナリオの上位に位置するものであり、満足しています。
米国でのMounjaroの上市については、供給面での制約はないと考えており、米国での上市状況を見ながら、米国での上市の適切なタイミングを判断していくことになります。なお、当社は過去数年間、Mounjaroの生産量を支えるために、ノースカロライナ州の新しいRTPサイド(2023年稼働予定)など、グローバルな製造能力を増強するための大規模な投資を行ってきました。
スライド12では、資本配分に関する最新情報をお伝えしています。上半期には、研究開発費、事業開発費、設備投資などを組み合わせ、将来の成長を促進するために45億ドルを投資しました。また、約18億米ドルを配当金として株主に還元し、15億米ドルの自社株買いを行いました。当社の資本配分の優先順位は一貫しており、主要な販売製品および上市予定の新製品に資金を供給し、パイプラインに投資し、将来の成長見通しを高めるための外部革新の機会を追求し、余剰資本を株主に還元しています。
スライド 13 は、2022 年度の財務見通しの更新です。通期の売上見通しは変更ありません。前回ガイダンスを更新して以来、為替による逆風が4億ドル追加され、通期では当初のガイダンスと比較して約7億ドルの為替逆風の影響が含まれています。この逆風は、COVID-19抗体ベブテロビマブからの追加収益予測で相殺されます。
この中には、本年6月に発表した米国政府との合意による275百万米ドルが含まれています。また、先ほどDaveが述べた米国政府以外からの販売開始による収入も見込まれます。今後、第3四半期は米国アリムタの最初のフル四半期の影響となります。
さらに、2021年第3四半期の売上は、迫り来るCOVID-19の売上から恩恵を受け、当四半期のトップライン成長に対しておよそ2.5ポイントの逆風となるでしょう。売上総利益率、販売管理費、研究開発費の見通しに変更はありません。販売費および一般管理費については、下半期の主要な成長製品への追加的な商業投資を含んでいます。また、買収したIPR&Dおよび開発マイルストーンの費用として、上半期の費用合計を反映し、約6億1,000万ドル を見込んでいます。
第3四半期の時点では、買収したIPR&Dや開発マイルストンの重要な費用は発生しておらず、このガイダンスには下半期の潜在 的あるいは未決定の事業開発取引による影響は含まれていません。GAAPベースの営業利益率は、為替レートによるマイナスの影響、及び買収したIPR&Dや開発マイルストーンの費用により、100ベーシスポイント減少し、それぞれ約27%及び29%となりました。非GAAPベースのその他の収益・費用の範囲は変更されていません。報告ベースでは、第2四半期の持分法による投資損失の影響を受け、その他の収益・費用は5億ドルから6億ド ルの範囲にとどまる見込みです。
上半期の当社の税率およびEPSには、税務上の研究開発費の資産計上を義務付ける2017年税法における規定の有利な影響がまだ含まれています。通年の財務ガイダンスでは、この規定が議会によって延期または廃止され、2022年から適用されることを想定しています。この規定が今年から有効に延期・廃止されない場合、報告税率および非GAAP税率は約10%から11%になると予想しています。これらの変更にともない、報告されている EPS のガイダンスを 0.34 ドル引き下げ、1 株当たり 6.96 ドルから 7.11 ドルとし、非 GAAP 方式の EPS のガイダンスを 0.25 ドル引き下げ 7.90 ドルから 8.05 ドルとしています。
非GAAPベースのEPSガイダンスを0.25ドル引き下げた理由は、買収したIPR&Dおよび一部の製品の開発マイルストーン費用によるEPSへの影響が、ベブテロビマブの追加販売による影響と相殺されるためで、為替レートの影響のみによるものです。それでは、研究開発の進捗状況について、ダンにお話しを伺います。
Dan Skovronsky — 最高科学・医学責任者
Anatさん、ありがとうございます。リリーの研究開発全体を見渡すと、最先端の科学を、患者さんの人生を変えるような医薬品に変えることができる可能性を持っていることに、私は非常に勇気づけられます。この可能性は、私が今日重点的に発言する後期開発段階のポートフォリオで現実のものとなりつつあります。また、早期段階のプロジェクトにおいても、その可能性はますます明白になってきており、今後の四半期において、これらの資産のいくつかについて最新情報をお伝えできることを楽しみにしています。
6月のADAではSurmount-1の詳細な結果などを発表しましたが、本日のR&Dアップデートは、前回の決算発表以降の後期段階の進展に焦点を当てたいと思います。スライド14は8月1日時点のパイプラインの一部を、スライド15は今年の重要なイベントの候補を示したものです。この2つのスライドを治療領域別に説明します。まず、免疫学です。
Olumiantは、パートナーであるIncyte社とともに、米国、EU、日本において、成人の重症円形脱毛症に対するファーストインディジーズの全身治療薬として承認されたことを誇りに思っています。円形脱毛症はアンメット・メディカル・ニーズの高い疾患であり、この疾患と闘う人々にとって、本薬剤が意味することを大変嬉しく思います」と述べています。また、中等度から重度のアトピー性皮膚炎の患者さんを対象としたlebrikizumab単剤での第3相維持療法試験のトップラインデータを発表しました。このデータでは、レブリキズマブ反応者の80%が52週間にわたり、皮膚クリアランスと重症度の改善を維持したことが示されています。
2週間に1回の投与と4週間に1回の投与の両方が、一貫して持続的な奏効を示すことをデータが裏付けています。4週間に1回の維持投与が可能であることは、患者さんや医療従事者にとって重要な差別化ポイントになり得ると考えています。リリーは、2022年にlebrikizumabをFDAに申請し、その後、世界中の他の規制当局に申請することを計画しています。Almirallは、欧州におけるアトピー性皮膚炎に対するlebrikizumabの開発および商業化の権利を有しており、2022年のEMAへの申請を計画しています。
ミリキズマブにシフト DBW会議において、第3相維持療法試験Lucent-2の結果を発表しました。本試験では、12週間の導入期においてミリキズマブによる治療が奏効した患者さんについて、1年後の臨床的寛解を達成した割合は、プラセボに無作為に割り付けられた患者さんの4分の1に対し、ミリキズマブの維持療法を受けた患者さんの50%であることが示されました。また、米国では
本年初めに発表した潰瘍性大腸炎に対するミリキズマブの承認申請に加え、EUおよび日本での申請も完了しました。また、免疫分野では、SLEを対象としたBTLAアゴニスト抗体のフェーズ2が開始され、当社の新しい[Inaudible]阻害剤がフェーズ1で示されたことも注目されます。IL-2コンジュゲートは、現在Rezpegaldesleukinという非専有名で登録されています。糖尿病に話を移します。
Mounjaroが米国で承認されたことに感激しています。Mounjaroは、成人の2型糖尿病の治療薬として、最初で唯一のGIPおよびGLP-1受容体アゴニストです。欧州では、CHMPから肯定的な見解を得ており、今期末のEMAによる完全承認に期待しています。当社は、ADAにおいて、肥満症または過体重の参加者の体重管理治療薬としてtirzepatideを評価したSurmount-1の刺激的な詳細結果を発表し、同時にNew England Journal of Medicine誌に掲載されました。
新しいデータには、探索的分析として、約40%の患者が15ミリグラムの用量で少なくとも25%の体重減少を達成したのに対し、プラセボ投与群では1%未満であったことが示されています。さらに、血圧と脂質の有意な低下、除脂肪体重の3倍近い脂肪量の減少が確認されました。また、試験開始時に糖尿病予備群の患者さんでは、95%以上が正常なグルコースレベルに戻ったという心強いデータも得られました。Surmount-1の有効性、安全性、忍容性のデータは、我々の期待を上回るものでした。
Tirzepatideの既存の堅牢なデータセットに基づき、当社は現在FDAと協力しており、Surmount-1に基づき、Surpassプログラムのデータと合わせて、慢性体重管理の登録に進む可能性があるかどうかを評価するための会議を近く開催する予定です。重要な更新があれば、投資家の皆様に引き続きお伝えしていきます。ティルゼパチドの臨床プログラムは引き続き拡大しており、閉塞性睡眠時無呼吸症候群の治療薬としてティルゼパチドを評価する第3相試験を開始しました。また、Surpass-Earlyと呼ばれる新しい試験も開始しました。この試験は、2型糖尿病の経過の初期に開始した場合のティルゼパチドの長期安全性と有効性を、標準治療と比較して評価するものです。
本年末には、ティルゼパチドとセマグルチド2.4ミリグラムの体重減少を比較するSurmount-5試験を開始する予定です。そして、今年の後半には、Surmount-MMOというフェーズ3の罹患率・死亡率・肥満度に関する試験を開始する予定です。次に、週1回投与の基礎インスリンFc(通称BIF)についてです。この試験は、初めて基礎インスリンを開始する成人の2型糖尿病患者を対象に、デグルーデックと比較してBIFを評価するものです。
当社のフェーズ2のGGG三阻害剤は、現在、非専売名レタトルチドとしてリストアップされています。また、デュアル・アミリン・カルシトニン受容体作動薬(DACRA)とPNPLA3 siRNAの2つの製品が、臨床第1相試験を開始しました。がん領域では、BTK阻害剤による前治療歴のあるマントル細胞リンパ腫患者に対するピルトブルチニブの申請をFDAが受理し、加速承認経路の下で優先審査指定したことを本日発表いたします。この困難な疾患には治療オプションの改善が必要であり、この可能性のある新薬が2023年初頭に患者さんに提供される可能性があることを心強く思っています。
がん領域では、変異型選択的PI3キナーゼα阻害剤をフェーズ1開発へ移行しました。そして最後に、神経科学に話を移します。また、早期症状のアルツハイマー病治療薬であるdonanemabの申請がFDAに受理され、加速承認経路の下での優先審査の指定が与えられたことをお知らせします。2023年半ばまでに実施される第3相確認試験「Trailblazer-ALZ 2」のトップラインの結果を待ち望んでおり、この結果が良好であれば、従来の承認申請の基礎となります。
また、現在、N3pG4を非専有名称であるRemternetugと呼んでいることにお気づきでしょうか。今後数週間のうちに、Remternetugの第3相プログラムを開始する予定です。ご覧の通り、第2四半期もリリーのパイプラインの進展にとって生産的な四半期となりました。それでは、Daveに電話を戻して、閉会の挨拶をお願いします。
デイブ・リックス — 会長兼最高経営責任者
ありがとう、ダン。質疑応答に入る前に、第2四半期の進捗状況について簡単にまとめたいと思います。主要な成長製品の業績が好調で、現在、コアビジネスの67%を占めていることは心強いことです。Mounjaroのような革新的な医薬品の上市に取り組む中で、この比率は時間とともに高まっていくと考えています。
買収したIPR&Dと開発マイルストーン費用の影響を除けば、売上高の伸びと事業のさらなる効率化の推進により、営業利益率の拡大が期待できます。今期は、2型糖尿病のMounjaroと円形脱毛症のOlumiantの承認により、当社のパイプラインに大きな進展が見られました。また、ドナネマブとピルトブルチニブが FDA に承認され、レブリキズマブのトップラインが良好で、ミリキズマブも追加申請されるなど、次の成長触媒となりうる製品に進展が見られました。最後に、配当と自社株買いを通じて、9億ドルを株主に還元しました。
将来に向けては、アンメットニーズの高い領域で画期的な治療薬を開発し、最近発売した医薬品が必要とする患者さんに届くよう、優れた治療を行うことに注力しているため、長期的な成長の見通しがあると確信しています。最後に、コメントさせていただきます。ケビン・ハーンが当社のIRチームの責任者として電話をかけるのはこれが最後です。質疑応答の司会を彼に任せる前に、株主、取締役会、そしてもちろん経営陣と従業員を代表して、彼に感謝の意を表したいと思います。
この4年半、彼は素晴らしい仕事をしてくれました。ストリートとの関係を強化し、会社のメッセージを株主に伝える大使として、また、株主の視点を経営陣に伝える大使として。彼は、米国コマーシャル・グループのリーダーとして、新たな任務 に就くことになりますが、その成功を祈っています。では、最後の質疑応答はケビンにお願いします。
ケビン・ヘルン — インベスター・リレーションズ担当副社長
ありがとう、デイブ。この間はありがとうございました。絶対に寂しくなります。できるだけ多くの方から質問をお受けしたいと思いますので、お一人様2点まででお願いします。
ロイス、Q&Aセッションの指示をお願いします。それから、最初の電話の方の準備ができました。
オペレーター
[最初の質問はバンク・オブ・アメリカのジェフリー・ミーチャムさんからです。質疑応答
Geoff Meacham — Bank of America Merrill Lynch — アナリスト
2つだけ簡単なものを。1つはMounjaroについてです。導入がかなり早いことは承知していますが、新規参入のソース、つまりGLPの素人か経験者かについて教えてください。それから、2023年までのペイヤーダイナミクスの予想について教えてください。また、Tirzepatideについては、肥満症に関する薬事規制の議論が進んでいると思いますが、NASHや睡眠時無呼吸症候群などの適応症を検討する際に、糖尿病やその他の適応症の安全性データベースを利用できるとお考えですか?
Kevin Hern — 投資家向け広報担当副社長
ジェフリー、ありがとうございます。まずはMounjaroについてマイクから。それからダン、規制当局のアプローチ、食欲、肥満についてコメントをお願いします。マイク?
マイク・メイソン — リリー 糖尿病担当 プレジデント
はい、ありがとうございます、ジェフリー。ご質問ありがとうございます。まず、Mounjaroが非常に好調な立ち上がりで、私たちは非常に興奮しています。
また、Mounjaroの72%が新規患者さんからの参入であるということで、ビジネスのソースとしても期待しています。Mounjaroの発売以来、総処方数、新規ブランド名、NTSのいずれにおいても、クラスの成長が加速しています。スイッチの28%のうち、Trulicityは30%で、70%が他のGLPです。その結果、先ほどAnatが指摘したように、リリーのインクレチンのシェアが伸びてきています。
NBRxによって、注射剤市場におけるリリーのシェアは12%増加しました。また、新規治療開始も10%増加しています。ですから、私たちは非常に満足しています。クラスと市場シェアを同時に拡大することができました。
2つ目の質問である支払者のダイナミクスについては、予想通りです。私たちは、非常に規律正しい行動を心がけています。短期的な成功ではなく、長期的な成功に向けた準備をすることに重点を置いています。そして、それが私たちのやっていることです。
ですから、今のところ期待通りに進んでいます。Express Scripts、Cigna、Humanaのフォーミュラで、コマーシャルとパートDの両方にアクセスすることができます。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、マイク。ダン?
Dan Skovronsky — 最高科学・医学責任者
Geoffrey、ご質問ありがとうございます。ご指摘の通り、私たちはティルゼパチドに関連する多くの適応症を追求する予定です。その中には、患者層が重複しているものもあります。
私たちが追求する適応症のほとんどは、肥満が既往症としてある患者さんで、閉塞性睡眠時無呼吸症候群や肥満の人の心不全など、時には原因となる疾患がある患者さんがベースとなっています。また、2型糖尿病と肥満が混在し、NASHのような多くの患者さんを対象とする適応症もあります。ですから、同じような提案の安全性試験を申請する際に利用することができます。もちろん、これらのプログラムの中には、時期をずらして実施されるものもあります。
ですから、これらの適応症で有効性データを取得する頃には、サーマウント・プログラムの残りの部分もほぼ完了していることでしょう。しかし、現在のところ、Surmountだけでなく、シェアベース・プログラム全体から、かなり大規模で堅牢な安全性データベースが得られています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、ダン。ジェフリー、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話はJPモルガンのクリス・ショットです。
Chris Schott — J.P.モルガン — アナリスト
私からは2つだけ。肥満の機会についてです。サーマウントのデータについて、あなたが得ているフィードバックの中で最高のものだと思います。支払者が肥満に対してどのようにアプローチするかという点で、何か変化がありますか?質問の中心は、肥満治療薬の広範な適用を考える前に、CV罹患率死亡率のデータを本当に見る必要があると予想していますか?それとも、この試験で明らかになったプロファイルを考慮すると、支払者はこの種の製品の保険適用にもっと興味を示す可能性があるとお考えですか?2つ目の質問は、Daveへのものです。
私はちょうど医療改革に携わっているところです。あなたがこのような質問に答えるのが好きなのは知っています。しかし、あなた方がこのプロセスに深く関わっていることは確かだと思います。最新の法案についてのお考えをお聞かせください。また、この法案が業界に及ぼす影響について、もう少し具体的に教えてください。
ケビン・ヘルン — インベスター・リレーションズ担当バイス・プレジデント
クリス、ありがとうございます。まずマイクから、次に医療保険制度改革についてデイブに伺います。
マイク・メイソン — リリー糖尿病センター長
はい、素晴らしい質問です。Surmount-1のデータは、肥満症を治療する患者さんや医師にとって驚異的なデータでした。私たちは — 雇用主や政府に対して、肥満治療薬へのアクセスを向上させるための効果が複合的に作用すると考えています。1つは、私たちが作成したデータです。
明らかに、私たちが出している最初のデータは、体重の減少だけでなく、脂質や血圧などの要素も含まれています。これまでのところ、私たちのデータは素晴らしいものです。Surmount-1からSurmount-4まで、より良いデータを出せば出すほど、短期的には私たちを助けてくれるでしょう。長期的には、CVや心不全、睡眠時無呼吸症候群など、肥満に関連する多くの疾患が共存しており、より良いデータが得られれば、肥満と重なる部分が多いこれらの適応症に道を開くことができると考えています。
ですから、私たちはこれらの試験と、試験が完了したときのデータを楽しみにしています。そして最後に、消費者の関心を高めることができれば、雇用主や政府に対して、この製品にアクセスできるようにするためのプレッシャーを与えることができます。私たちはこの3つの分野で強力な計画を持っており、肥満に関する最初のデータ公開に興奮しています。肥満症とトリゼパチドの長期的な展望については、非常に強気で臨んでいます。
Kevin Hern — インベスターリレーションズ担当副社長
ありがとう、マイク。デイブ?
デイブ・リックス — 会長兼最高経営責任者
はい、Chris、ご質問ありがとうございます。この電話会議に出席している皆さんは、このパッケージの中身をよく理解していると思います。確率を推測するのは難しいですが、何かが一線を越える可能性は1ヶ月前よりもずっと高くなっていることは間違いないでしょう。議会のプロセスを経て、上院と下院で何らかの変更が行われれば、多少の調整が行われるかもしれません。
しかし、もし……私たちが見ているものが通過したら、それがあなたの質問なのかもしれませんね。ご存知のように、私たちはパートD改革に賛成してきました。特に年間の自己負担額に上限を設けたり、ドーナツホールの概念をなくすなど、よい段階的な改革だと思います。残念ながら、期待していたネット価格での患者負担の考え方は改善されていません。
しかし、それ自体は、私たちは支持します。CPI調整については、この電話会議に出席している誰もが知っているように、商業市場ではすでに多くのCPIキャップが行われているので、それほど問題ではありません。CPIが現在の水準にある以上、医薬品の価格は経済の他の部分ほど速くはないと思います。しかし、交渉の部分が問題です。
そして、短期的には、私たちの会社にとってというより、おそらく業界にとって、あまり意味がないと思います。いずれにせよ、26年にならないと始まりません。しかし、中期的には、もちろんライフサイクルが短くなる製品も出てくるでしょう。リリーの製品がそれに巻き込まれるかどうかは、これからわかります。
しかし、おそらく私にとって最も有害なことは、低分子化合物、特にがんのように段階的な開発が必要な疾患における低分子化合物は、ステージから始めて、アジュバントまで、あるいは一部の希少疾患まで、本当に必要とされていない、価値がかなり低いという信号を投資家や資本配分者に送ることになる、ということでしょう。ですから、私たちは他の革新的な分野に資源を集中させます。そのような分野はたくさんあります。他のセクターもそうでしょう。
そして、おそらく将来、より優れた経口抗がん剤や希少疾病用医薬品を望んでいる患者さんにとっては、本当に惜しいことだと思います。この点については、おそらく十分に語られていないと思いますので、その点を強調したかったのです。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、Dave。クリス、ご質問ありがとうございました。次の方どうぞ。
オペレーター
次の電話はグッゲンハイムのシェイマス・フェルナンデスです。
Seamus Fernandez — Guggenheim Partners — アナリスト
素晴らしい ここで2つほど質問をさせてください。Dave、あなたが口頭で述べたコメントについて、もう少し詳しく知りたかったのです。経口糖尿病薬の開発に向けた取り組みに、どのような影響があるとお考えですか?また、低分子ではなく、よりペプチドに特化した複雑な経口治療薬の方が有益なのでしょうか?また、低分子ではなく、よりペプチドに特化した複雑な経口治療薬の方が有利でしょうか?
この法律が、低分子の観点からも、GLP-1の経口製剤の上市を目指すことを示唆しているかどうか、興味があります。それから、グルカゴンのメカニズムについてですが、CCCは2つのフェーズ2の臨床試験に参加していますが、オキシントモジュリンは糖尿病のフェーズ1にしか参加していません。CCCを進めることを正式に決定されたのでしょうか、それとも肥満領域での次世代アセットとしてMazdutideがまだ候補に挙がっているのでしょうか?
Kevin Hern — 投資家向け広報担当副社長
Seamus ありがとうございます。次にDave、そしてDanにお願いします。
Dave Ricks — 会長兼最高経営責任者
ありがとう、シェーマス。この点については、ポイントを見つけることができたと思います。各プロジェクトを1つずつ評価する必要があります。
しかし、おそらく10年先には、この法案が通過した場合、業界で開発される低分子経口製剤の数は、そうでなかった場合よりも少なくなると思います。私にとっては、それが残念なことです。特に、GLPの場合、体重減少がより大きな利益をもたらすことを受け入れることができれば、先ほどの信念体系のようなものがひっくり返り、血圧の低下が心血管リスクによいように、慢性体重管理が健康によいことを人々が受け入れることができるようになると思います。そして、これらの製品は1つずつ評価され、大きなチャンスは前進し、うまくいくと思います。
政府機関向けビジネスではライフサイクルが短くなるため、それを考慮する必要がありますが、その点については検討します。私が申し上げたのは、より狭い範囲での収益機会では、かなり難しくなるということです。また、一部の疾患では医薬品開発の方法によって、新しい適応症が前倒しで開発できないことがあります。このことはよく考えられていなかったと思いますし、長期的な影響もあるでしょう。
もうひとつ、この法案によって連邦政府は3,000億ドルを調達し、産業界は少なくとも0.5兆ドルの負担を強いられますが、そのうち患者利益支援に回るのはわずか5,000万ドル、つまり10%です。私たちが製薬会社(Lilly)を率いていたときのもう一つの方針は、製薬会社から出るものはすべて患者のために還元することでした。この点についても議論する必要があります。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、Dave。ダン?
Dan Skovronsky — 最高科学・医学責任者
グルカゴンを含む分子についてのご質問、ありがとうございます。オキシントモジュリンのMazdutideはグルカゴンとGLP-1を組み合わせたもので、レタトルティドはグルカゴンGLP-1とGIP-1を組み合わせたGGGとなります。GGGはフェーズ2で、オキシントモジュリンはまだフェーズ1ということですね。
どちらも次世代減量薬として有力だと思います。しかし、ここではっきりさせておきたいのは、非常に高い借り物であるということです。Surmount-1で見た本当に目覚ましい結果を超える大きなステップアップを求めているのです。どちらもその可能性があると思いますが、どちらを第3相に進めるかは、もっとデータを見る必要があります。
ちょうど数年前にティルゼパチドの第2相試験を行ったときと同じように、第3相試験に進むにはステップアップが必要であると指摘しました。
Kevin Hern — 投資家向け広報担当副社長
ダン、ありがとうございます。シーマス、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話はカンターのルイーズ・チェンです。
ルイーズ・チェン — キャンター・フィッツジェラルド — アナリスト
最初の質問は、肥満治療薬についてです。ノボのSelect試験からTirzepatideへの読み替えの可能性はありますか?また、米国でのアウトカムベースの研究をどのように構成したいのか、何かお考えがありますか?次に、アルツハイマー病に関しては静かですが、ドナネマブの市場機会について、特に年末に予定されているいくつかのフェーズ3試験の前に、何か最新の考えをお持ちでしょうか?
Kevin Hern — インベスターリレーションズ担当バイスプレジデント
ありがとう、ルイーズ。Select試験についてのご質問はダンに、アルツハイマー病についてのご質問はアンにお願いします。
Dan Skovronsky — チーフサイエンティフィック&メディカルオフィサー
ご質問ありがとうございます。もちろん、私たちは常に競合他社の臨床試験での成功に目を向けています。患者さんのために優れた医薬品を開発できるよう、優れたデータを求めています。私は、中間解析に合格したが、有効性については試験を中止しなかったと発表したことは、問題ないと思います。
ティルゼパチドとセマグルチドでは、メカニズムが異なること、様々なアウトカムに対する有効性の程度が異なること、試験デザインが異なること、ある程度異なる集団であることを忘れてはならないと思います。ですから、Surmount-MMO試験のデザインは変えませんし、おそらく成功するという考えも変えません。もちろん、かなり劇的な体重減少から始まって、肥満による罹患率や死亡率に効果があるはずです。また、第3相試験で報告されたすべての心血管系指標には、非常に顕著な血圧の低下が含まれており、これは有益であるはずです。
LDLの低下、HDLの増加、トリグリセリドの低下、これらすべてが心血管系のアウトカムに貢献するはずです。私たちは、この試験について、今後も期待し、確信しています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、ダン。Anneさん?
アン・ホワイト — リリー・ニューロサイエンス社 社長
はい。ルイーズ、アルツハイマー病についてのご質問ありがとうございます。ですから、事実はボトムラインです。ですから、私たちは、ドナネマブとアルツハイマー病のポートフォリオの中長期的な機会について、引き続き確信しています。
今、私たちが注目しているのは、加速承認ルートを通じて、適切な患者さんにドナネマブを迅速に提供すること、そして、第3相のデータによって再検討することです。そして、特に従来のFDAの承認があれば、FDAは、あるいはCMSは、適応外治療の適用を制限し続けることはないだろうと、私たちは楽観的な見方を持ち続けています。さて、競合他社の読み上げについて言及されました。以前の電話会議で指摘したように、医薬品と試験デザインの違いから、これらの読み出しの一部で結果が異なる可能性があります。
ご存知のように、私たちはユニークなデザインの薬剤を開発し、迅速かつ深いプラーククリアランスを実証しています。ですから、他の薬が主要評価項目を外したとしても、私たちは落胆することはありません。ですから、他の企業が主要評価項目を外したとしても、私たちは落胆することはありません。しかし、短期的には、もちろん、現在のCMSとCDの早期承認の下では、患者さんへのアクセスが非常に制限されることは認めざるを得ません。
しかし、加速承認によって、フェーズ3のデータに基づいてCMSと迅速に交渉し、できればその時点で再考を促すことができますし、補足的なBLAを通じて従来の承認を加速することもできます。ですから、承認の可能性と早期承認に続いて、私たちが短期的に行うことは、診断エコシステムの構築、医師の紹介プロセスや輸液システムの支援に時間を使うことです。第3相試験の準備のために、やるべきことはたくさんあると思います。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、アン。ルイーズ、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話はモルガン・スタンレーのテレンス・フリンです。
テレンス・フリン — モルガンスタンレー — アナリスト
私からは2つ。マイクさんは、償還の観点からMounjaroの長期的な成功を目指すという話をされたと思います。私たちのためにそれを定義し、より細かい点を指摘してください。つまり、長期的にTrulicityを上回る正価を目指すと考えるべきでしょうか。それから、市場への供給能力についてですが、当然ながら、上市は予想のハイエンドとおっしゃいました。
この点については、米国での供給に対する信頼性という点で、コメント中に少し触れておられたと思います。しかし、世界全体の供給力についてはどのようにお考えですか。また、長期的に必要であれば、供給を増やすための柔軟性についてお聞かせください。
ケビン・ヘルン — インベスター・リレーションズ担当バイス・プレジデント
ありがとう、テレンス。Mounjaroに関するご質問は、アクセスと価格の両方について、そして世界的な供給見通しについて、マイクにお伺いしたいと思います。
マイク・メイソン — Lilly Diabetes 社長
わかりました。テレンス、ご質問ありがとうございます。長期的には、私たちの目標は明らかに正味価格を最適化することですが、同時にTrulicityのような幅広いアクセスを確保することです。この2つが私たちの目標です。
もちろん、正味価格の交渉について具体的なことは公にはしていません。しかし、私たちはその進展に満足しています。私たちは、新製品発売前にアクセスを加速させるべく、規律正しく行動しています。あまりに積極的になりすぎると、早期にアクセスできるようになったものの、そのために高額な費用を支払うことになるため、注意が必要です。
ですから、私たちは常に自制しています。私たちは、優れたプロファイルを持つ優れた製品を持っています。支払者はそれを見ていますが、それはプロセスであり、私たちは今、そのプロセスを経ているのです。Mounjaroの供給面では、Anatが言ったように、私たちは成功のための計画を立てていました。
そのため、さまざまな打ち上げシナリオを用意しています。そして、このレベルのアップテイクを考慮した長いシナリオも用意しました。Anatが話したように、Mounjaroの米国での打ち上げに供給上の制約はないと考えています。
私たちの製造チームは、サプライチェーン全体の製造能力を高めるために、何年も前から24時間体制で取り組んできました。製造拠点はいくつもあり、日々、初期生産能力を最適化しています。また、今後数年間で生産能力を拡大するための投資も行っています。ノースカロライナ州のリサーチ・トライアングル・パークには、2023年に稼働する新しい親会社の工場があり、その後ろにもノースカロライナ州のコンコードにもうひとつ工場があります。
また、「Mounjaro」の原料を作り直すために2つの製造施設を建設中で、これらは後日登場する予定です。もちろん、私たちは成功のための計画を立てており、製造チームはできるだけ多くの過去の供給を得るために、24時間体制で取り組んでいます。
Kevin Hern — 投資家向け広報担当副社長
マイク、ありがとう。テレンス、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次はウォルフリサーチのティム・アンダーソンです。
Tim Anderson — Wolfe Research — アナリスト
肥満のアウトカム試験についてですが、おそらくMACEを主要評価項目とする心血管アウトカム試験なのでしょうか?その場合、Novoの…17%を示すように設計されているのですが、どの程度の有益性を示すように検出力が設定されるのでしょうか?また、肥満症におけるノボ社製品との比較試験について、試験デザイン、主要評価項目、そしておそらく最も重要なことですが、結果が出る時期について、何かご意見がありますか?
Kevin Hern — 投資家向け広報担当副社長
ありがとう、Tim。最初の質問はSurmount-MMOに関するもので、次にマイクがNovoとの[Inaudible]のヘッド・トゥ・ヘッドの試験について質問します。
Dan Skovronsky — チーフサイエンティフィック&メディカルオフィサー
はい、ご質問ありがとうございます。興味深いご指摘ですね。あなたの質問には、体重を減らすことで多くの健康上の利点が得られるという見解が含まれていると思います。
肥満は、従来から心血管アウトカム試験やMACE試験で測定されているものだけでなく、様々なものの危険因子となります。ですから、おそらく、私たちはこれをCVOTではなく、肥満における病的死亡アウトカム、MMOと呼んでいます。しかし、それ以上に、主要評価項目やパワーアップの前提に関する詳細には、意図的に触れていません。そのため、まだ開示されていません。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、ダン。マイク?
Mike Mason — Lilly Diabetes 社長
はい。ティルゼパタイドとセマ2.4ミリグラムを比較した臨床試験は、これまでありませんでした。そのため、ティルゼパチドの体重減少効果や患者さんにとってのベネフィットを総合的に実証する良い機会であったと考えています。ヘッド・ツー・ヘッド・スタディがゴールド・スタンダードです。
医療従事者と話すたびに、彼らはヘッド・ツー・ヘッド・スタディを高く評価し、そこから多くのものを得ています。医療従事者と話すたびに、彼らはヘッド・ツー・ヘッド・スタディを高く評価し、そこから多くの情報を得ています。ですから、これは正しいことだと思いますし、そうできることをうれしく思います。この試験は、肥満や過体重で体重に関連するコアモビリティを持つ人を対象に、ティルゼパチドとセマ2.4を比較するヘッド・トゥ・ヘッドの試験になります。
それ以外のデザインやタイムラインについては、clinicaltrials.govへの掲載が近づいた時点で、後日、詳しくお知らせします。
Kevin Hern — 投資家向け広報担当副社長
マイク、ありがとうございます。ティム、ご質問ありがとう。次の方、お願いします。
オペレーター
次の電話は、コーウェンのSteve Scalaです。
スティーブ・スカラ — コーウェン・アンド・カンパニー — アナリスト
2つほど質問があります。まず、リリー社は準備書面において、一部の地域で競合のGLP-1製剤の入手が制限されていると述べています。どの地域で、どの程度の問題があるのか、もう少し具体的に教えてください。それから、ダンに質問です。あなたは、臨床試験の中間報告について、臨床腫瘍学委員会から多くの電話を受けた経験があると思います。
例えば、心血管系のアウトカムに関するトゥリシティの試験(REWIND)です。問題は、その時のDSMBとスポンサーとの情報交換の深さはどの程度なのか、ということです。例えば、中間報告を超えて試験が継続されている場合、会話は「試験が継続されている」という3文字だけなのでしょうか?それとも、もっと広範囲なのでしょうか?あるいは、それによるのでしょうか?もし、依存するのであれば、それは何によって決まるのでしょうか?DSMBが、分子のさらなる開発という観点から何らかの指針を示さないのは、少なくとも私には逆効果のように思われます。それが私の質問です。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、Steve。米国外のTrulicityの需要と供給に関するご質問はイリヤに、2つ目のご質問はダンにお願いします。イリヤさん?
イリヤ・ユファ — リリー・インターナショナル社長
はい、スティーブ、ご質問ありがとうございます。まず、私たちが見てきたのは、多くの国際市場でTrulicityの需要が加速していることです。そして、おそらく3つの要因があると思います。1つは、大きな商業的成功です。
糖尿病治療薬のポートフォリオでは、Trulicityの成長と利用を促進することに非常に成功しています。同時に、市場の成長も加速しています。また、一部の市場では、セマグルチドが十分に入手できないため、Trulicityに対する需要が高まっています。また、一部の市場では、セマグルチドが十分に入手できないため、トゥリシティに対する需要が高まっています。
そのため、現地の状況は非常にダイナミックであると評価しており、この増幅された需要に対応するため、できる限り増産しているところです。しかし同時に、これらの市場の一部では、成長を管理し、患者への影響を最小限に抑えることを確認する必要があります。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、イリヤ。ダン?
Dan Skovronsky — 最高科学・医学責任者
はい、ありがとうございます。ご質問の趣旨は理解できますし、私たちは、他の企業が行うかもしれないこと、あるいは見るかもしれないことについて、特に意見を述べることはないと思いますが、私たちがDSMBをどのように運営し、業界全体としてDSMBについてどう考えているかについてお話しします。ここには、2つの原則があります。
第一に、もちろん、独立性です。これは、スポンサーが運営するものではありません。これは、患者の安全性を考える上で重要なことだと思います。私たちは、スポンサーが見ているデータを見ることはありませんし、原則的に議論に加わることもありません。
もうひとつは、DSMBが決定を下すべきルールをあらかじめ設定しておくことです。それは非常にシンプルなルールかもしれません。場合によっては、主要評価項目で一定のアルファ値で統計的有意差を出すというようなルールもあれば、より複雑なルールで、副次的または部分集団にわたる一貫性や主要評価項目での有効性をより高く評価するというようなルールもあります。試験やスポンサーによって異なる、説得力のある効果を確信できるように。
確信があります。3つ目は、DSMBがスポンサーに返す勧告は、多くの場合、事前に指定されたものであるということです。つまり、この基準に合致していればDSMBに伝える。これは私たちに伝えるものです。
そうでない場合は、こうしてくださいということです。そして、それらは通常、進行中の研究の完全性を損なったり、意図しない盲検化を引き起こしたりするような色彩のない事実の問題です。DSMBがどのように機能するかを理解するのにお役に立てれば幸いです。多くの企業では、研究の中止など、DSMBにとって驚くべき勧告があった場合、多くの場合
多くの場合、スポンサー、あるいはスポンサーの1人か2人の代表者が盲検化されていない状態で、DSMBの結論を確認してから行動を起こしますが、これは単純な試験の継続のような決定では典型的なことではありませんね。
Kevin Hern — 投資家向け広報担当副社長
スティーブ、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話は、エバコアのウマー・ラファットです。
ケビン・ヘルン — インベスター・リレーションズ担当バイス・プレジデント
ウマー?
オペレーター
回線が切れたようです。シティグループのアンドリュー・バウムに代わります。
Andrew Baum — Citi — アナリスト
2つほど質問をさせてください。Mounjaroの最初の1つは、あなたがユニークなラベルを持っている、滴定中に第二形態の受胎を必要とする、これは最近の最高裁判所は、行対体重を覆すことはありません結果を考えると、妊娠のリスクの面で自信を強調した。どのようにこのことについて考えている、それは潜在的に製品のアキレス腱かどうか、適応症としてロールバックすることができる追加の薬理学の研究を通じてかどうか?FDAのレビューを見ると、コースデータよりもむしろ薬理学的な懸念があるように思えますが?次に、ポジティブな面です。ピルトブルチニブの申請に関して、マントルに対する承認が得られると仮定します。
したがって、MCN–NCCNによるCLLの治療ガイドラインに含まれることになると思います。そこで、第3相臨床試験プログラムの成熟を待っている間、マントル細胞による迅速な承認が、CLL市場への浸透を加速させる可能性があるとお考えか、お聞かせいただけますでしょうか。
Kevin Hern — 投資家向け広報担当副社長
アンドリュー、ありがとうございます。最初の質問は、Mounjaroのラベリングと社会情勢についてマイクに、そしてピルトブルチニブに関する質問はジェイクにお願いします。
マイク・メイソン — リリー・ダイアベテス社 社長
アンドリュー、ありがとうございます。質問をありがとうございます。皆さん、私たちのラベルMounjaroは、経口避妊薬を使用している女性に対し、本剤の投与開始時および各用量漸増時の4週間は、経口避妊薬以外の避妊法に切り替えるか、追加するよう助言しています。そのため、医療従事者はこのことを理解しています。
Mounjaroの大きなメリットを考えると、このことはHCPや消費者のMounjaroへの関心にまったく影響を与えていません。市場でのデータを見ると、7月22日までのIQVIAのデータがありますが、これはフルプロモーションのちょうど5週間目にあたります。Mounjaroはすでに市場シェア20%に達しています。ですから、これはまったく問題視していません。
今後の取り組みや評価については、現時点では投資家の皆様に報告することはありません。しかし、この問題はMounjaroのアップテイクにまったく影響を与えていないのです。
Kevin Hern — インベスターリレーションズ担当バイスプレジデント
ありがとう、マイク。ジェイク?
Jake Van Naarden — リリー社ロキソの最高経営責任者
はい、ご質問の件です。方針として、私たちは、実際に受領する予定の、あるいは受領すると予想される適応症と一致する会社主催のガイドラインの要請を提出します。BTK前治療歴のある再発難治性マントル細胞リンパ腫ということで、この設定でもそうするつもりです。NCCNやその他のガイドラインのプロセスは完全に独立しており、私たちは全く関与していません。
私たちが表示した適応症以外のものをどの程度選択するかは、本当に私たちの手には負えませんし、推測することも困難です。そしてもちろん、私たちは受け取った表示適応症に基づいてのみ、製品のプロモーションを行うつもりです。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、ジェイク。アンドリュー、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話はSVB証券のデービッド・ライジンガーです。
デービッド・ライジンガー — SVBリーリンク・パートナーズ — アナリスト
ムンジェロについて質問します。まず、株式売却益の割合について教えてください。リリーのTrulicityとMounjaroを合わせたシェアが12ポイント上昇したというコメントでした。
そこで、何がスタート地点で、今日の数字はどこなのかを理解したかったのです。それから、新規治療開始が10%増加したというコメントもありました。それについて、XからYまでの数字を教えてください。それから、米国での好調な売れ行きについて、リリー社ではどの程度、米国外でのMounjaroの上市を控えているのでしょうか。
現在直面している製造供給の制約のために、リリーは米国外のMounjaroの上市をどの程度制限する予定ですか?
Kevin Hern — 投資家向け広報担当副社長
ありがとうございます。シェア獲得に関するご質問はマイクに、OUSの上市に関するご質問はイリヤにお願いします。
マイク・メイソン — リリー・ダイアベテス社 社長
わかりました。Dave、ありがとう。先ほど電話でお話したパーセンテージについて、もう少し詳しくご説明します。私たちが見ているのはIQVIAのデータで、私たちの分析ではその始まりは6月3日です。
ADAの翌週、つまり6月14日の週にローンチミーティングを行いました。それ以来、フル稼働でプロモーションを行っています。現在の状況を比較すると、IQVIAのデータは7月22日までありますので、プロモーションは5週間です。インクレチン注射剤の市場において、7月22日時点と6月13日時点のNBRxの数量、新規ブランド品の数量とシェアを比較しています。
その後、MounjaroのNBRxのシェアは20.5%に達しました。TrulicityのNBRxのシェアは8.4ポイントしか下がっていません。リリーの注射剤インクレチンとNBRxのシェアは12.2%になりました。そして、同じ時期、同じ市場のMTSでは、リリーの注射用インクレチン・NBRxのシェアが全体で10%増加しています。
イリヤ・ユファ — リリー・インターナショナル社長
はい。デイビッド、Mounjaroの米国外での発売に関するご質問と、それに関する私たちの考えについてありがとうございました。米国外での発売について、私たちがどのように考えているのか、重要なポイントのひとつがあります。
それは、薬事承認やそのプロセス、そして価格や償還の問題です。多くの市場で償還を受けるまでに1年かかることもあります。そのため、発売初年度の販売数量はやや限定的です。
私たちは、Mounjaroの米国での発売を心強く思っていますし、米国外での発売と、米国外の市場において当社の糖尿病に関する専門知識と強みを活用することを楽しみにしています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、イリヤ。デイビッド、お電話ありがとうございました。
Dave Ricks — 会長兼最高経営責任者
デイビッド、質問の構成からすると、供給上の制約に直面しているということですが、それを明確にするためです。もちろん、新しい市場に製品を投入する前に、新しい患者さんと供給を完全に開始できることを確認したいと思います。また、競合他社の動きから、ある市場で何が必要かを1年後に予測するのは困難です。
ですから、供給がないわけではありません。需要が不安定なのです。私たちは、一連の打ち上げを開始する前にそれを知っておきたいと考えているのです。しかし、私たちは米国で打ち上げを行い、その供給に全力を尽くしています。
しかし、米国ではすでに発売しており、その供給を確約しています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、デイブ。次の方、お願いします。
オペレーター
次の電話はゴールドマン・サックスのクリス・シブタニです。
クリス・シブタニ — ゴールドマン・サックス — アナリスト
2つ質問させてください。1つ目はMounjaroについてですが、患者のソースがどこに絞られているかという相対的な傾向についての情報をありがとうございました。予想通りでしょうか?また、これはどこに向かうとお考えですか。まだ発売して間もないため、このような質問となりました。2つ目の質問は、Verzenioについてです。実は、あまり注目されていないようですが、業績は好調で、論理的にはアジュバントの設定であるように思われます。
この好調の要因は何だとお考えですか。また、これまでの好調な業績をもたらしているこれらの傾向について、今後の見通しをお聞かせください。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、クリス。Mounjaroについてのご質問はMikeに、Verzenioについてのご質問はJakeにお願いします。
マイク・メイソン — リリー・ダイアベテス社 社長
ええ、いい質問ですね。私たちは、私たちが考えていた通りの結果を得ていると思います。より多くの新規患者さんがこのクラスに加わることになります。
医療関係者と話しているのはそのような患者さんで、私たちもそのような患者さんを得ています。ですから、私たちはこのことに驚いていませんし、新しいGLPの上市で期待されることの典型的な例です。Mounjaroのような新製品が出た場合、特に内分泌専門医の場合、必ずしもナイーブな患者さんを診るわけではないことが予想されます。すでにGLPを服用している患者さんがたくさんいるのです。
ですから、Mounjaroの話をすると、現在のGLPでうまくいっていない患者さんや目標に達していない患者さんを、実際に切り替えることができるチャンスだと喜んでくれます。そのため、初期には、ナイーブな患者さんに対して、スイッチの患者さんの割合が高くなると思います。現在、72%が未経験者です。Trulicityを見ると、88%もあります。
ですから、素朴派の割合が時間とともに増えていくことを期待しています。Mounjaroの発売以来、TrulicityとMounjaroのパフォーマンスには非常に満足しています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、マイク。ジェイクは?
Jake Van Naarden — リリーのLoxoの最高経営責任者です。
はい、Verzenioについてのご質問ありがとうございます。私たちも、今年のこれまでの経過に満足しています。ご質問の「なぜ」と「これから」についてですが、「なぜ」については、主に、「なぜ」と「これから」だと思います。
その理由については、MonarchE試験の臨床データそのものに大きく起因していると思います。このデータは実証可能であり、医師や患者さんはそれを見て、すぐにこの薬を診療に取り入れたいと思うのだと思います。さらに、これは私たちが期待していたことですが、特に、これまで他のCDK4/6阻害剤を使用していた医師が、アジュバント療法でVerzenioを使用し、経験を積んだ後、これまで使用していなかった転移性疾患領域で使用するようになり、転移性疾患領域でのシェアが拡大しています。これは、私たちが期待していたことの一部です。
今年に入ってから、それが少しづつ起こっているようです。とはいえ、これからどうするかという点では、2つだけ申し上げたいことがあります。1つは、私たちはまだmonarchEのデータを知らない医師と交流を続けています。これはもちろん、良いことでもあり悪いことでもあります。
というのも、その薬に適した患者さんがいて、その人たちがその薬を使うべきだからです。しかし、現在ある適応症で成長を続けるチャンスでもあります。その点、過去にもお話ししたように、MonarchEの登録試験集団に適応を拡大する機会があることを期待していますし、過去にお話ししたように、全生存期間の分析を待っているところでした。そう、私たちはこの状況に満足しているのです。
この勢いを持続させるために、今後多くの機会があると見ています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、ジェイク。クリス、ご質問ありがとうございました。ネクストコール、お願いします。
オペレーター
次の電話はバークレイズのカーター・グールドです。
Carter Gould — Barclays — アナリスト
まず最初に、初期のMounjaroの数字で、現金給与の要素がどの程度顕著だったのか、またそれがどのように変化していくと予想されるのかについてお話いただけますか?それから、薬価の話に戻りますが、別の角度から見ると、コンプライアンスの改善を考えると、Lillyは医療費負担の減少による主な受益者の一人であると思われます。その影響について、あるいは、今日のコンプライアンスが米国とそうでない他の市場とでどのように異なるかについて、教えていただけますか。
ケビン・ヘルン — インベスター・リレーションズ担当副社長
ありがとう、カーター。Mounjaroに関する最初の質問はMikeに、薬価制度改革とその影響に関するフォローアップについてはDaveにお願いします。
Mike Mason — Lilly Diabetes社長
カーター、ご質問ありがとうございます。現金払いの面では、現金払いの割合が、市場でのアクセスの割合に追随していくと考えています。これまでのところ、先ほど申し上げたように、ヒューマナ、エクスプレス・スクリプツ、National Preferred Formulary、シグナでは、パートDとコマーシャル・アクセスの両方があります。これらを合計すると、全米の生活の20%強になります。
これがおそらく、現金報酬の最も良い見積もりだと思います。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、マイク。Daveさん?
Dave Ricks — 会長兼最高経営責任者
はい。カーター ご指摘の通り、私たちは、この和解案に含まれるパートD改革を単独で支持することになると思います。理由はたくさんあります。1つは、パートDに支払う業界の負担をより公平に分配することです。
現在、ドーナツホールの計算方法は、数年前にさかのぼると、私たちは多くの決算説明会で、ドーナツホール内の業界からの貢献が本当に不均衡であることを説明しなければなりませんでした。糖尿病や循環器系でよく使われる薬は、かなり大きな打撃を受けています。しかし、これは平準化されます。そのため、大災害に見舞われる薬剤はより多く支払われ、薬剤の種類に関係なく、よりバランスのとれた貢献ができるようになりました。
もうひとつ、ご指摘のとおり、これは主にVerzenioのような製品に影響すると思いますが、Catastrophicに放り込まれた患者さんには、今日5%の上限なしの貢献があります。患者さんが治療を中断するだけでなく、コンプライアンス率についても言及されましたが、例えば、米国よりも欧州の経口がん治療薬の方が優れています。しかし、経済的負担のために、医師やその家族が自分にとって適切な薬物療法を受ける資格すらないと判断してしまうため、より多くの開始が見られるようになると思います。そして、よりターゲットを絞った治療法ではなく、化学療法に移行してしまうかもしれません。
つまり、アメリカの医療を向上させるだけでなく、Lillyが製造する医薬品の見通しを立てることができる別の方法を提示することになるのです。ですから、これらは良いことなのです。先ほど申し上げたように、バランスとしては、交渉の面ではまだ好ましいものではありませんが、これらはポジティブな要素です。
ケビン・ヘルン — インベスター・リレーションズ担当副社長
ありがとう、Dave。カーター、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話はベレンバーグのケリー・ホルフォードです。
ケリー・ホルフォード — ベレンバーグ — アナリスト
価格についてお聞かせください。今期、特に米国で多くの薬剤の実現価格が下がっていることは明らかですが、GLP-1市場でそれがどのように進展しているのか、具体的にお話しいただけますか?Mounjaroの上市後、Trulicityのリベートが特に上昇しましたか?また、今後どのような期待をお持ちですか?これは、昨日の競合他社の調査でも、高いリベートとネガティブなチャネルミックスというトレンドがありました。この点について、皆さんのご意見を伺いたいと思います。
それから、アナトに簡単な質問をします。2017年の税制廃止の可能性について、いつ頃より明確になるとお考えでしょうか?
ケビン・ヘルン — インベスターリレーションズ担当バイスプレジデント
そうですね。ケリー、ありがとう。インクレチンの市場価格動向についてはマイクに、税制改革についてはアナトに質問をします。マイク?
マイク・メイソン — リリー・ダイアベテス社 社長
ええ、いい質問ですね。新製品がフォーミュラリーに加わった場合、当然、支払者は追加のリベートを要求してくると思います。ですから、私たちが規律正しくあるべきということと、なぜそのような議論をあまり急がせたくないかということの一環として、そのような要素も含まれているのです。
ですから、Mounjaroの発売によってGLPの価格設定が大きく変わることはないと思いますが、国からの圧力や契約交渉の一部にはなると思います。
ケビン・ヘルン — インベスター・リレーションズ担当バイス・プレジデント
ありがとう、マイク。アナト?
Anat Ashkenazi — 最高財務責任者(CFO
税金についてですが、最近の上院の書簡で明らかになったように、研究開発費の資産計上の変更をアピールすることについて、幅広い超党派の支持を得ているようです。これは実現する可能性があります。私たちは今年末までに実現すると考えていますが、推測するに、おそらく年末になると思います。
Kevin Hern — 投資家向け広報担当副社長
Anatさん、ありがとうございます。ケリー、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話者は Wells Fargo の Mohit Bansal です。
Mohit Bansal — Wells Fargo Securities — アナリスト
Select-Early試験について1つだけ質問させてください。糖尿病予備軍に有効であることを証明するために、試験期間と、コントロールに対するデルタの点で何を示す必要があるのでしょうか。また、そのような患者には経口GLPの方が良い薬ではないでしょうか?
Kevin Hern — 投資家向け広報担当副社長
ありがとう、Mohit。では、ダンさん、Select-Early、糖尿病前治療の試験、それから経口GLPの方がいいのかどうかという質問です。
Dan Skovronsky — チーフサイエンティフィック&メディカルオフィサー
はい、これは初期の糖尿病試験です。しかし、エンドポイントのデザインはまだ公表していないと思います。しかし、糖尿病予防に関しては、非常に興味深い分野であることは間違いないと思います。
現在、糖尿病–糖尿病の予防を示すために必要なことについては、FDAのガイダンスがあり、そのような主張をすることができます。これは非常に高いハードルです。どの薬が糖尿病になるリスクを減らすことができるのか、どの薬が適応になる前に糖尿病を予防することができるのか、この分野では理解が進むと思います。このクラスの薬剤、特にティルゼパチドは、この分野で大きな可能性を秘めていると思います。
Surmount-1のデータでは、試験開始時に糖尿病予備軍だった人の大部分(95%以上)が、試験終了時には正常なグルコースレベルになっていることを示しましたが、これは本当に有望です。これは非常に有望です。このような主張をするためには、薬物洗浄を含む長期的なデータが必要です。
Mike Mason — Lilly Diabetes 社長
多分、私は…それについて少しコメントを加えることができます。この研究は、糖尿病患者、つまり糖尿病と診断された人を対象にしています。そして、Tirzepatideのような製品を治療コースのかなり早い段階で投入した場合に、糖尿病の進行にどのような影響を与えることができるかを検証したいと思います。つまり、ナイーブな患者さんを治療のごく初期に開始し、標準的な治療と比較する研究です。
GLPやGIPの効果で体重を減らし、β細胞の機能とインスリン感受性を改善すれば、2型糖尿病に大きな影響を与えることができると考えています。それが、この試験で検証していることです。これは、私たちがとても楽しみにしている研究のひとつです。また、自動注射器による週1回の注射が良い体験であることを多くの人が理解し、実際に経口剤を好む消費者もいますが、MounjaroやTrulicityのように自動注射器による週1回の注射を実際に消費する人もいるので、注射の分野だけでなく、もっと早くから週1回の注射が使われ始めています。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、マイク。Mohit、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次の電話はBMOキャピタル・マーケッツのエヴァン・セイガーマンです。
エヴァン・セイガーマン — BMOキャピタル・マーケッツ — アナリスト
ドナネマブの早期承認申請がFDAに受理されましたが、iADRSスケールが完全承認のためのエンドポイントとして認められるかどうか、FDAから明確にされましたか?また、N3pG4を第3相に移行させるためのポイントについてお話いただけますか?
Kevin Hern — 投資家向け広報担当副社長
エヴァン、ありがとうございます。では、ダンにお願いします。
Dan Skovronsky — チーフサイエンティフィック&メディカルオフィサー
はい、アルツハイマー病の質問を2つありがとうございます。1つ目は、遺伝子治療薬の早期承認申請についてで、第3相試験の主要評価項目であるiADRSの受容性について、より深い洞察を得る機会になるでしょうか。加速承認は、第2相試験で確認されたドナネマブの認知的または機能的な利点の理解を条件としているわけではないので、実際には機会とはならないかもしれません。
その代わり、加速承認はアミロイドレベルを下げることを証明することが条件となります。だから、よくわからないのです。この点については、確認試験であるTrailblazer-2に関連していることは明らかですが、深い議論に入ることになります。2つ目の質問は、N3pG 4分子のレムテルネグに関するものです。
これは次世代の抗プラーク抗体で、ドナネマブが狙うのと同じグルタミン酸残基を攻撃するように設計されています。私たちは、この分子が患者さんのプラークを除去する強力な能力を持っていることを確認しています。ドナネマブの欠点は抗薬物抗体であることですが、この分子にはその欠点がないことも確認されています。このように、ドナネマブには抗薬物抗体がなく、プラークのクリアランスが強力であることから、患者さんによりわかりやすく伝えるために、別の剤型に変更することも可能だと考えています。
ですから、それを検討していくつもりです。
Kevin Hern — 投資家向け広報担当副社長
ありがとう、ダン。エヴァン、ご質問ありがとうございました。次の方、お願いします。
オペレーター
次はTruist SecuritiesのRobyn Karnauskasです。
ケビン・ヘルン — インベスター・リレーションズ担当副社長
ロビン?はい おそらく、次の発信者に移ることができますか?
オペレーター
次のお電話はUBSのコリン・ブリストウです。
Colin Bristow — UBS — アナリスト
そして、ケビン、いつも素晴らしい仕事をありがとうございます。事業開発についてですが、今日2つの案件が発表されました。興味のある分野、ディールサイズについて、最新の考えを聞かせてください。また、潜在的なターゲットから、市場背景を考慮した上での取引に対する意欲について、どのようなフィードバックを得ているのでしょうか?次に、ドナネマブについてですが、最近の考えはいかがでしょうか?また、第3相臨床試験の成功が保険償還の観点からどのように見られるかについて、CMSとのやり取りはありましたか?
Kevin Hern — 投資家向け広報担当副社長
ありがとうございます。BDの質問についてはAnatに、ドナネマブの質問についてはAnneにお願いしたいと思います。
Anat Ashkenazi — 最高財務責任者(CFO
事業開発の側面から、関心のある分野と市場で見られるものについてですが、最近の評価の変化を考慮すると、私たちの関心のある分野は、過去数四半期にあったものとほとんど変わりはありません。そのため、前臨床および臨床開発のさまざまな段階にあるこれらの領域における画期的な技術革新の可能性や、これらの領域での拡大についてお話した新しい治療法の領域について検討しています。ここ1年半から1年半の間に、既存のポートフォリオを補完し、コア領域のイノベーションと付加価値を高めるために、パイプラインに追加できるような、より初期段階の機会にも目を向けています。バリュエーションについては、ここ半年ほどで変化してきましたが、事業開発の機会を追求するという点では、歴史的に制限される要因ではありませんでした。
私たちが投資を行うのは、本当に画期的な機会を見つけるためなのです。また、ターゲットとの関わり方についてご質問をいただきましたが、そうした考え方が変わったかどうかについては、パートナーシップや買収を検討する際に、誰もが価値を見いだしたいと思っていますし、機会があれば、良い場所にたどり着くことができる傾向があります。
Kevin Hern — インベスター・リレーションズ担当バイス・プレジデント
ありがとう、アナト。Anneさん?
Anne White — リリー・ニューロサイエンス社 社長
ドナネマブについてのご質問ありがとうございます。ドナネマブのデータパッケージは、Trailblazer-ALZとALZ 2の両方を含んでおり、CMSがCDにおける高いエビデンスレベルと表現しているものを満たすのに十分であると、私たちは考えています。Trailblazer-ALZ試験は、明らかに、主要評価項目を達成した最初のアルツハイマー病治療薬試験です。もしTrailblazer-ALZ 2でも、私たちが期待するような臨床的有用性の直接的証拠が得られたら、CMSと協議して、この治療法への迅速かつ広範なアクセス方法を検討するつもりです。
私たちは、このプロセスを通じてCMSと関わりを持ち、今後もそうしていきます。そして、CMSは今後も話し合いを続けることに前向きです。NCDでは、ドナネマブの有望性を指摘し、Trailblazer-2フェーズ3プログラムを理解することに大きな関心を示しています。そのため、再審査の時期については、より明確になると思います。
23年半ばには、彼らとデータを共有することができます。彼らは、迅速な再審査を約束すると公言しています。しかし、その時期については、彼らがデータを手に入れ、来年、次のステップを彼らと話し合い、改めてお知らせする必要があると考えています。
ケビン・ヘルン — インベスター・リレーションズ担当副社長
コリン、ご質問ありがとうございました。もう質問はありません。デイブ、終了です。
Dave Ricks — 会長兼最高経営責任者
OK。素晴らしい。今日はありがとうございました。また、通話中の技術的な問題についてお詫びしたいと思います。
すぐに復旧させます。本日のご参加と、当社へのご関心に感謝いたします。また、新リーダー、ジョー・フレッチャーを含むIRチームへのフォローアップをお願いします。また、本日の電話会議で取り上げられなかった質問があれば、ぜひお寄せください。
それでは、良い一日をお過ごしください。
以上です。他の翻訳希望やご感想をいただけると嬉しいです。
*誤訳などがあるかもしれませんでの参考程度にしていただき投資は自己判断でお願いします。
ブログ運営の励みになりますので、お手数ですが、応援の1日1クリックをよろしくお願い致します。
↓↓<応援クリックお願いします>



[…] 前回の2022年第2四半期決算説明会はこちらです。 […]